Clear Sky Science · fr
Différences spécifiques au groupe d’épendymome de la barrière hémato‑encéphalique révélées par une approche multi‑omique
Pourquoi les gardiens du cerveau comptent chez les enfants atteints de cancer
Le cerveau humain est farouchement protégé par un système de sécurité naturel appelé barrière hémato‑encéphalique, une couche serrée de cellules qui contrôle strictement quelles substances peuvent pénétrer le tissu cérébral depuis le sang. Cette barrière est essentielle à la santé, mais elle complique aussi l’accès des médicaments anticancéreux aux tumeurs cérébrales — en particulier chez les enfants. Cette étude pose une question a priori simple mais aux grandes implications cliniques : les différents sous‑types d’une tumeur cérébrale pédiatrique appelée épendymome se situent‑ils derrière des barrières de nature différente, et cela pourrait‑il aider à expliquer pourquoi de nombreux médicaments échouent ?
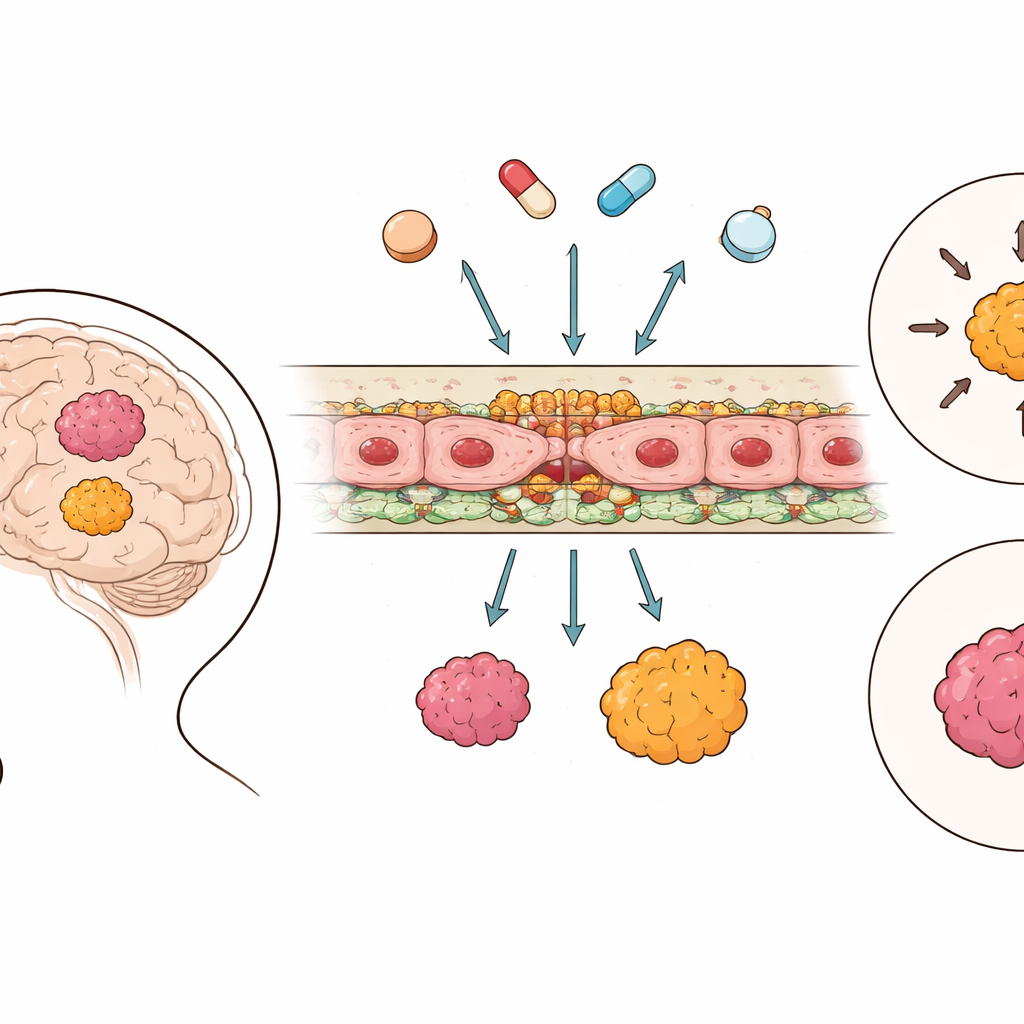
La paroi protectrice du cerveau
La barrière hémato‑encéphalique est constituée des cellules qui tapissent les minuscules vaisseaux cérébraux, reliées entre elles par des jonctions spécialisées et équipées de « pompes » moléculaires capables de renvoyer des médicaments dans la circulation. En utilisant des données génétiques à grande échelle provenant de 364 tumeurs d’épendymome et de 225 échantillons de cerveau sain, les chercheurs ont répertorié l’activité des gènes impliqués dans ces jonctions et dans les systèmes de transport. Ils ont constaté que, contrairement à de nombreux autres cancers cérébraux, le tissu d’épendymome montrait en réalité une activité plus élevée des composants clés des jonctions que le cerveau sain, suggérant que la barrière entre le sang et la tumeur est souvent plus serrée plutôt que plus perméable. En revanche, les pompes d’efflux des médicaments et d’autres transporteurs présentaient des profils plus hétérogènes, spécifiques aux groupes, plutôt qu’une tendance simple tout‑ou‑rien.
Pas seulement la localisation ou l’âge, mais le type de tumeur
Ensuite, l’équipe a examiné si des différences normales de développement ou d’anatomie cérébrale pouvaient expliquer ces schémas. En entraînant des scores par réseaux neuronaux résumant l’activité des gènes de jonctions et de transporteurs, ils ont confirmé des caractéristiques connues dans les cerveaux sains : la fermeté de la barrière évolue avec l’âge et diffère entre des régions telles que le cortex et le cervelet. Cependant, ces tendances liées à l’âge et à la région ne se retrouvaient pas dans les tumeurs. Dans les principaux groupes intracrâniens d’épendymomes, les scores liés à la barrière étaient similaires quel que soit le site d’origine de la tumeur ou l’âge du patient. Cela indique que l’identité moléculaire de la tumeur elle‑même — son sous‑groupe — est le principal facteur déterminant du comportement local de la barrière.
Zoom sur les cellules de la barrière
Les mesures en masse peuvent masquer quelles cellules sont réellement responsables de l’activité génique observée. Pour résoudre cela, les chercheurs se sont tournés vers le séquençage d’ARN unicellulaire et d’un noyau unique provenant de plusieurs cohortes de patients et d’un nouvel ensemble de validation. Ces données plus fines ont révélé que la plupart des gènes liés à la barrière sont concentrés dans un sous‑ensemble distinct de cellules vasculaires au sein du microenvironnement tumoral. Cette sous‑population endothéliale spécialisée exprimait fortement des gènes classiques de jonction tels que CLDN5 et d’autres marqueurs de barrière, tandis que les cellules tumorales, immunitaires et de soutien en exprimaient très peu. Les résultats ont été renforcés par des mesures protéiques et des imageries avancées, qui ont montré ces protéines tapissant physiquement les vaisseaux tumoraux, confirmant que les signatures génétiques reflètent une barrière structurale réelle.
Tester la barrière dans des modèles murins
Parce que de nouveaux médicaments sont souvent évalués dans des modèles murins avant d’atteindre les patients, l’équipe a vérifié si des xénogreffes dérivées de patients de différents groupes d’épendymome reproduisaient les caractéristiques humaines de la barrière. Dans ces modèles, les cellules tumorales issues de patients poussent dans le cerveau de souris, où les vaisseaux sanguins sont en grande partie d’origine murine. Les analyses d’ARN et de protéines ont de nouveau montré une forte expression des jonctions dans les cellules vasculaires, mais avec quelques différences entre les modèles et entre la tumeur et le cerveau environnant. L’imagerie avec agents de contraste et traceurs fluorescents a suggéré que, globalement, la barrière dans ces tumeurs restait relativement intacte, et que des différences subtiles entre modèles et sous‑groupes pouvaient influencer la facilité avec laquelle les molécules passent du sang au tissu tumoral.
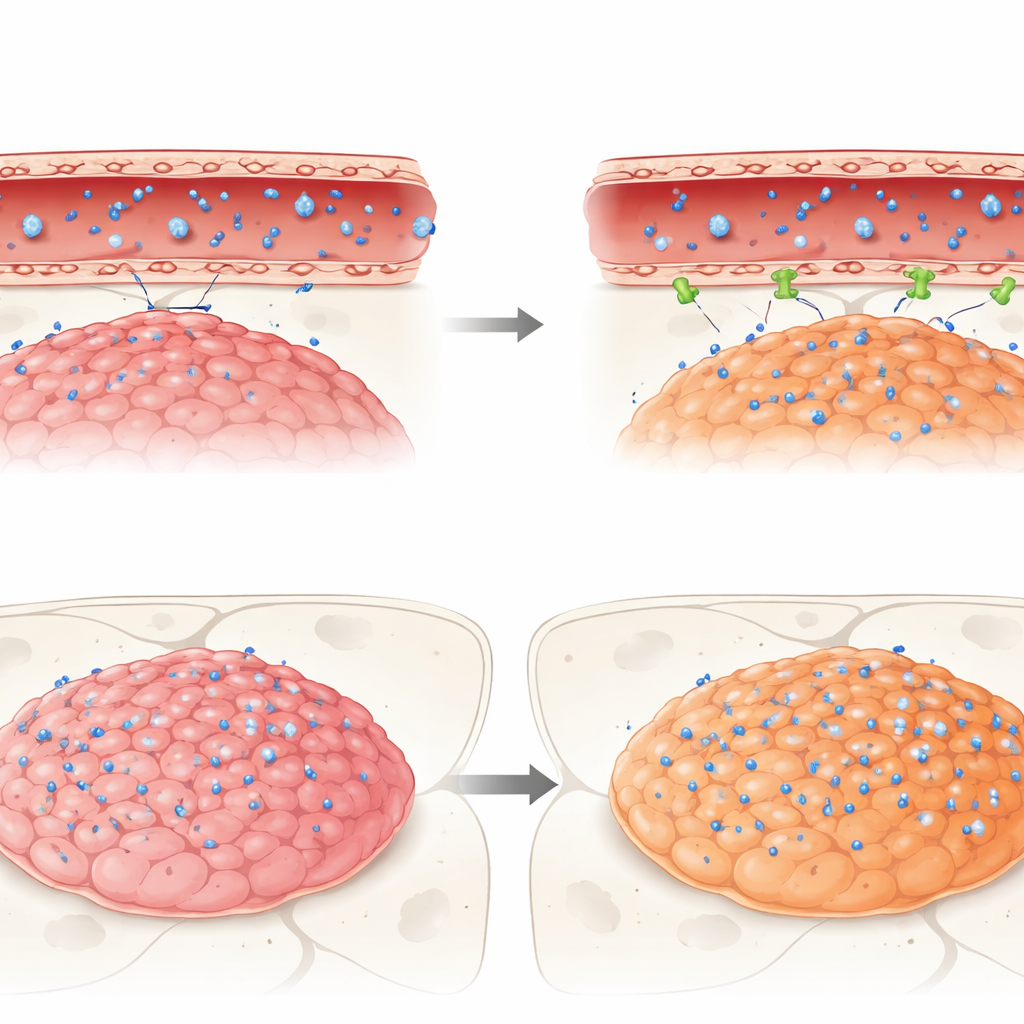
Que se passe‑t‑il lorsque de vrais médicaments tentent de traverser
Enfin, les chercheurs ont suivi le parcours de trois médicaments anticancéreux d’intérêt clinique — idasanutlin, témsirolimus et étoposide — dans ces tumeurs murines. Les trois étaient actifs contre les cellules d’épendymome en culture, mais in vivo ils se heurtaient à la barrière. L’idasanutlin, bien que chimiquement apte à traverser les membranes cellulaires, atteignait des niveaux très faibles dans la tumeur et dans le cerveau sain par rapport au sang, suggérant une forte exclusion par la barrière. En revanche, le témsirolimus et l’étoposide, tous deux connus pour être expulsés par certaines pompes, s’accumulaient davantage dans les tumeurs d’un sous‑groupe agressif (positif pour la fusion ZFTA) que dans un autre groupe (PFA) ou que dans le cerveau sain adjacent. Même ainsi, aucun des médicaments n’atteignait dans les tumeurs des concentrations comparables à leurs niveaux efficaces observés in vitro, soulignant combien la barrière peut discrètement saper des thérapies prometteuses.
Ce que cela signifie pour les traitements futurs
Pour un non‑spécialiste, le message central est simple : les tumeurs d’épendymome ne se trouvent pas toutes derrière le même type de porte cérébrale. Au contraire, chaque sous‑groupe moléculaire s’accompagne de sa propre version de la barrière hémato‑encéphalique — souvent étonnamment serrée — qui façonne l’accès des différents médicaments à leurs cibles. En combinant plusieurs couches de données issues de patients et de modèles murins, ce travail montre qu’il est essentiel de comprendre et de mesurer ces caractéristiques de barrière spécifiques aux sous‑groupes pour concevoir des essais cliniques plus intelligents. Plutôt que de partir du principe qu’un médicament qui tue des cellules en culture fonctionnera dans le cerveau d’un enfant, les thérapies futures pourraient devoir être choisies — et éventuellement associées à des stratégies modulant la barrière — en fonction de la façon dont sont construits les « gardiens » de chaque tumeur.
Citation: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Mots-clés: épendymome, barrière hémato‑encéphalique, tumeurs cérébrales pédiatriques, administration de médicaments, multi‑omique