Clear Sky Science · ru
Группоспецифичные различия гематоэнцефалического барьера при эпендимоме выявлены с помощью мультиомного подхода
Почему «стражи» мозга важны для детей с раком
Человеческий мозг надежно защищен природной системой безопасности — гематоэнцефалическим барьером, плотным слоем клеток, который строго регулирует, какие вещества могут проникать из крови в мозговую ткань. Этот барьер необходим для поддержания здоровья, но он также значительно затрудняет попадание противоопухолевых препаратов в опухоли мозга — особенно у детей. В исследовании поставлен внешне простой, но клинически важный вопрос: скрываются ли разные подтипы детской опухоли эпендимомы за разными по свойствам барьерами, и может ли это объяснить, почему многие лекарства не работают?
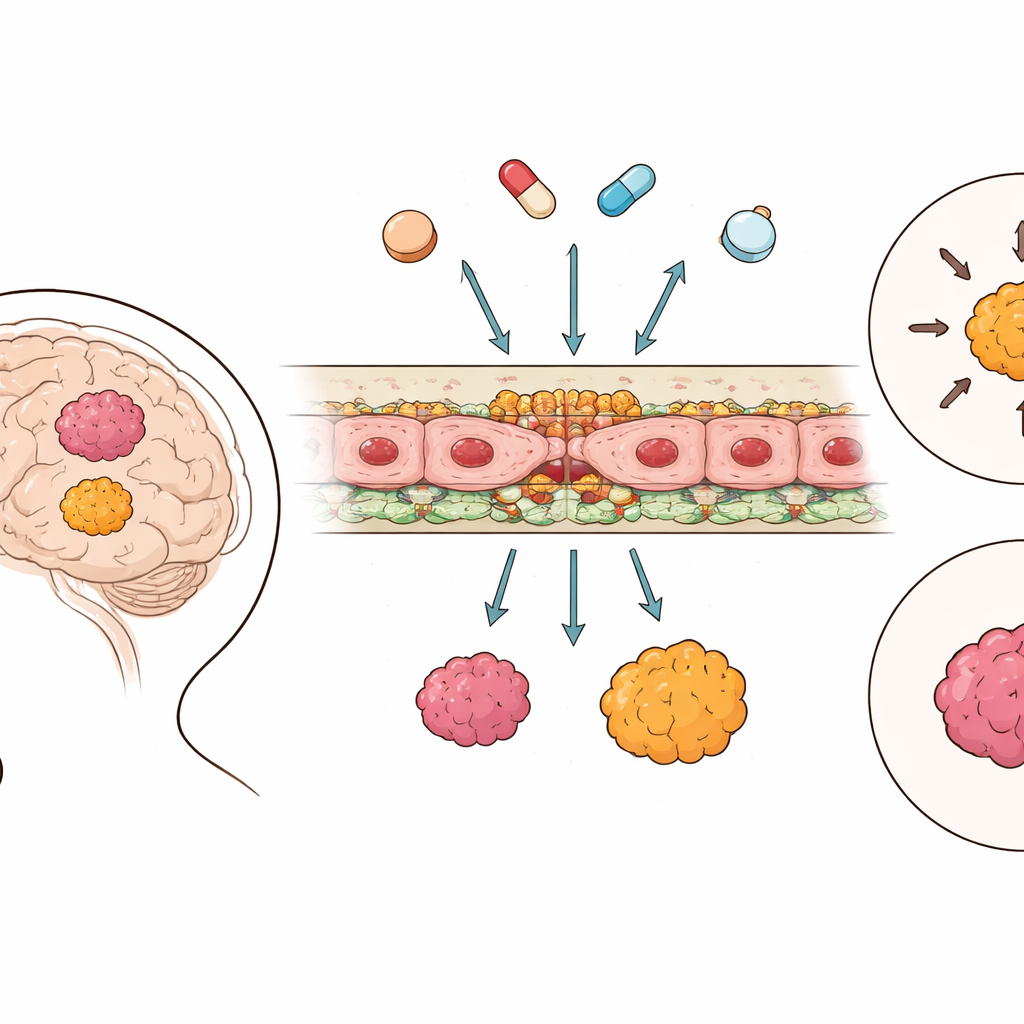
Защитная стена мозга
Гематоэнцефалический барьер формируют клетки, выстилающие крошечные сосуды мозга; они крепко соединены специализированными контактами и оснащены молекулярными «насосами», которые выбрасывают лекарства обратно в кровоток. Используя крупномасштабные генетические данные из 364 опухолей эпендимомы и 225 образцов здоровой ткани мозга, исследователи систематизировали активность генов, отвечающих за эти соединения и системы транспорта. Они обнаружили, что, в отличие от многих других опухолей мозга, ткань эпендимомы часто демонстрирует более высокую активность ключевых компонентов контактов по сравнению со здоровым мозгом, что указывает на то, что барьер между кровью и опухолью зачастую более плотный, а не более проницаемый. Напротив, транспортеры и насосы, выкачивающие лекарства, показали более смешанные, зависящие от группы, паттерны, а не простой «вкл/выкл» эффект.
Не только местоположение или возраст, но и тип опухоли
Далее команда проверила, можно ли объяснить эти закономерности нормальными различиями в развитии или анатомии мозга. Построив нейросетевые оценки, суммирующие активность генов контактов и транспортеров, они подтвердили известные особенности здорового мозга: плотность барьера меняется с возрастом и различается между областями, такими как кора и мозжечок. Однако эти возрастные и региональные тренды не переносились на опухоли. В основных внутричерепных группах эпендимомы показатели, связанные с барьером, выглядели схожими вне зависимости от того, в какой части мозга возникла опухоль и сколько лет пациенту. Это свидетельствует о том, что молекулярная идентичность опухоли — её подпороговая группа — является главным фактором, определяющим поведение локального барьера.
Углубление в клетки барьера
Обобщенные измерения могут скрывать, какие именно клетки ответственны за наблюдаемую генную активность. Чтобы разобраться, исследователи обратились к одно- и одноядерному РНК-секвенированию из нескольких когорт пациентов и новому валидационному набору. Эти более детализированные данные показали, что большинство генов, связанных с барьером, сосредоточены в отдельной подгруппе сосудистых клеток в микроокружении опухоли. Эта специализированная эндотелиальная субпопуляция выражала классические гены контактов, такие как CLDN5, и другие маркеры барьера, тогда как клетки опухоли, иммунные и поддерживающие клетки выражали их очень слабо. Выводы были подтверждены измерениями белков и продвинутой визуализацией, которые показали, что эти белки физически выстилают опухолевые сосуды, подтверждая, что генетические сигнатуры отражают реальную структурную перегородку.
Тестирование барьера в моделях на мышах
Поскольку новые препараты часто оценивают в мышиных моделях перед клиническим применением, команда проверила, воспроизводят ли ксенотрансплантаты, полученные от пациентов с различными группами эпендимомы, черты человеческого барьера. В этих моделях клетки опухоли пациентов растут в мозге мышей, где сосуды в основном мышиного происхождения. Анализы РНК и белков вновь показали выражение контактных компонентов в сосудистых клетках, хотя с некоторыми различиями между моделями и между опухолью и окружающим мозгом. Визуализация с контрастными агентами и флуоресцентными трассерами показала, что в целом барьер в этих опухолях остается относительно целым, и что тонкие различия между моделями и подгруппами могут влиять на то, насколько легко молекулы переходят из крови в опухолевую ткань.
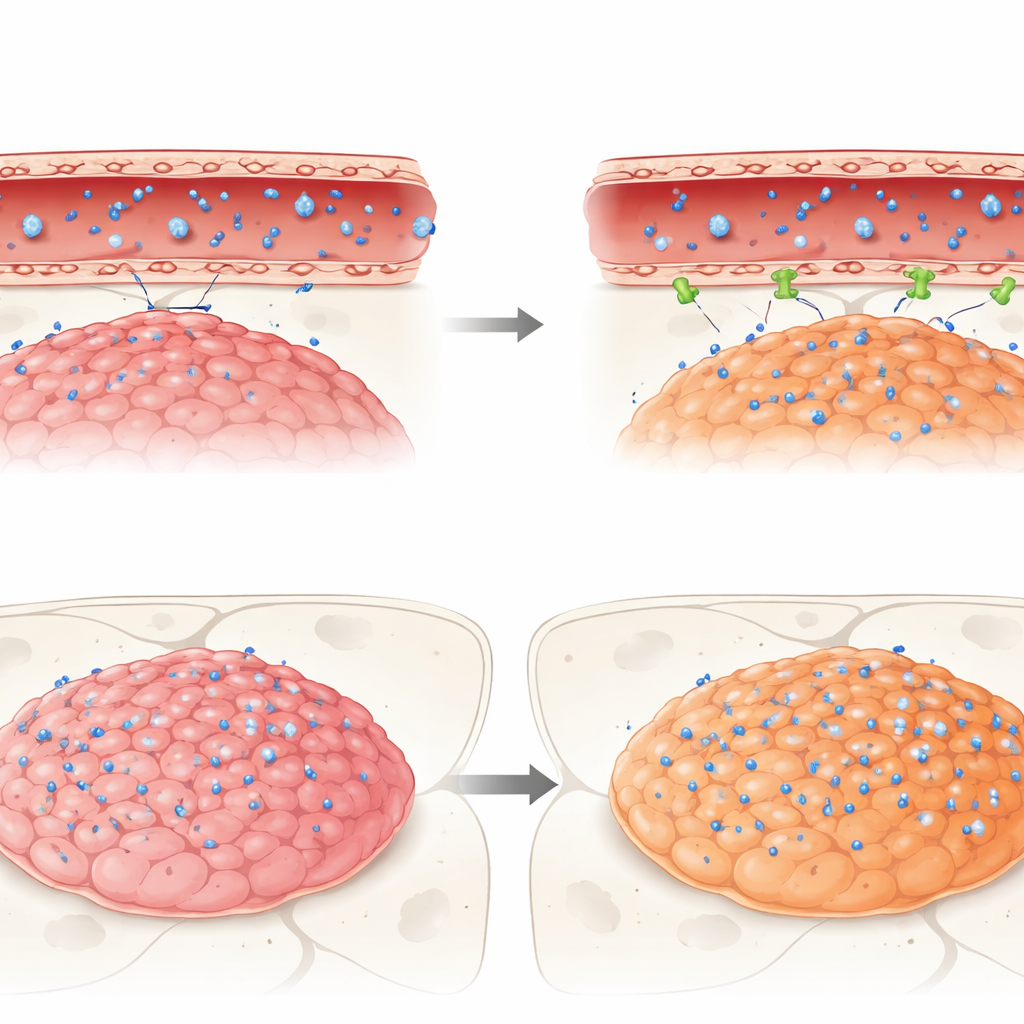
Что происходит, когда настоящие лекарства пытаются пройти через барьер
Наконец, исследователи проследили путь трех клинически значимых противоопухолевых препаратов — идасанутлин, темсиролимус и этопозид — в этих мышиных опухолях. Все три проявляли активность против клеток эпендимомы в культурах, но в живом мозге им противостоял барьер. Идасанутлин, хотя по химическим свойствам способен пересекать клеточные мембраны, достигал очень низких концентраций и в опухоли, и в нормальном мозге по сравнению с кровью, что указывает на сильное исключение барьером. Напротив, темсиролимус и этопозид, оба известные как субстраты определенных насосов, накапливались в опухолях одной агрессивной подгруппы (ZFTA-фьюжн-положительной) больше, чем в другой группе (PFA) или в прилежащем здоровом мозге. Тем не менее ни одно из препаратов не достигало в опухолях концентраций, сопоставимых с их эффективными уровнями in vitro, что подчеркивает, как барьер может тихо подрывать перспективные терапии.
Что это значит для будущих лечений
Для неспециалиста основной вывод прост: эпендимомы не все окружены одним и тем же типом «ворот» мозга. Каждая молекулярная подгруппа имеет свою версию гематоэнцефалического барьера — часто удивительно плотную — которая определяет, насколько хорошо разные лекарства достигают своих мишеней. Объединив несколько слоев данных от пациентов и мышиных моделей, работа показывает, что понимание и измерение этих группоспецифичных черт барьера необходимо для проектирования более разумных клинических испытаний. Вместо предположения, что препарат, убивающий опухолевые клетки в чашке Петри, сработает в мозге ребенка, будущие терапии, возможно, придется подбирать — и, при необходимости, сочетать со стратегиями модификации барьера — с учетом того, как устроены «стражи» конкретной опухоли.
Цитирование: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Ключевые слова: эпендимома, гематоэнцефалический барьер, педиатрические опухоли головного мозга, доставка лекарств, мультиомика