Clear Sky Science · sv
Subgruppsspecifika skillnader i blod‑hjärnbarriären hos ependymom avslöjade med en multi‑omik‑strategi
Varför hjärnans väktare spelar roll för barn med cancer
Den mänskliga hjärnan skyddas av ett naturligt säkerhetssystem kallat blod‑hjärnbarriären, ett tätt lager av celler som strikt kontrollerar vilka ämnen som kan gå från blodet in i hjärnvävnad. Denna barriär är avgörande för hälsa, men gör det också mycket svårare att få cancerläkemedel in i hjärntumörer—särskilt hos barn. Denna studie ställer en förenklat enkel fråga med stora kliniska konsekvenser: lever olika subtyper av en pediatrisk hjärntumör som kallas ependymom bakom olika slags barriärer, och kan det förklara varför många läkemedel misslyckas?
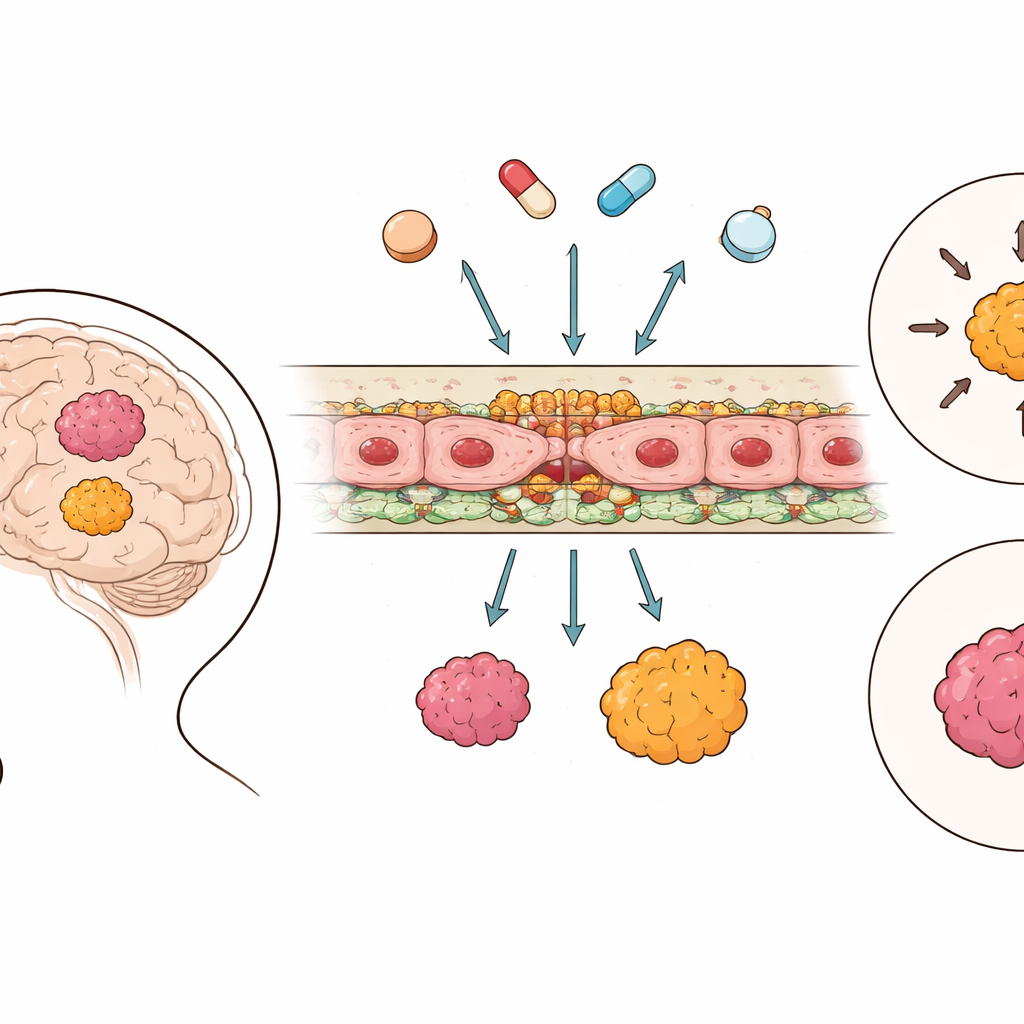
Hjärnans skyddande vägg
Blod‑hjärnbarriären byggs av celler som klär de små hjärnskillarna och som är förenade av specialiserade junctions, samt utrustade med molekylära ”pumpar” som kan fösa tillbaka läkemedel till blodomloppet. Genom att använda storskaliga genetiska data från 364 ependymomtumörer och 225 prover av frisk hjärna katalogiserade forskarna aktiviteten hos gener som är involverade i dessa junctions och i transportsystem. De fann att, till skillnad från många andra hjärncancerformer, visade ependymomvävnad faktiskt högre aktivitet i viktiga junction‑komponenter än frisk hjärna, vilket tyder på att barriären mellan blod och tumör ofta är tätare snarare än läckande. Däremot följde pumpar för läkemedelsefflux och andra transportörer mer blandade, gruppspecifika mönster i stället för en enkel av/på‑trend.
Inte bara läge eller ålder, utan tumörtyp
Nästa fråga var om normala skillnader i hjärnans utveckling eller anatomi kunde förklara dessa mönster. Genom att träna neurala nätverk som summerar junction‑ och transporter‑genaktivitet bekräftade de kända egenskaper i friska hjärnor: barriärens täthet förändras med ålder och skiljer sig mellan områden som cortex och cerebellum. Dessa ålders‑ och regionsmönster överfördes dock inte till tumörerna. Över de stora intrakraniella ependymomgrupperna såg barriärrelaterade poäng likartade ut oberoende av var i hjärnan tumören uppstått eller patientens ålder. Det pekar på tumörens molekylära identitet—dess subgrupp—som huvudorsak till hur dess lokala barriär beter sig.
Zooma in på barriärcellerna
Bulkmätningar kan dölja vilka celler som faktiskt ansvarar för den observerade genaktiviteten. För att reda ut detta använde forskarna single‑cell och single‑nucleus RNA‑sekvensering från flera patientkohorter och en ny valideringsuppsättning. Dessa mer detaljerade data visade att de flesta barriärrelaterade gener är koncentrerade till en distinkt undergrupp av blodkärlsceller i tumörens mikro‑miljö. Denna specialiserade endoteliala subpopulation visade stark expression av klassiska junction‑gener såsom CLDN5 och andra barriärmarkörer, medan tumörceller, immunceller och stödjeceller uttryckte mycket lite. Resultaten stärkts av proteinmätningar och avancerad bildgivning, som visade att dessa proteiner fysiskt beklädde tumörens blodkärl och bekräftade att de genetiska signaturerna speglar en verklig strukturell barriär.
Test av barriären i musemodeller
Eftersom nya läkemedel ofta utvärderas i musmodeller innan de når patienter, undersökte teamet om patient‑deriverade xenograftmodeller av olika ependymomgrupper återger mänskliga barriärdrag. I dessa modeller växer tumörceller från patienter i mössens hjärnor, där blodkärlen till stor del är mus‑deriverade. RNA‑ och proteinanalyser visade återigen stark junction‑expression i kärlceller, men med vissa skillnader mellan modeller och mellan tumör och omgivande hjärna. Avbildning med kontrastmedel och fluorescerande spårämnen antydde att barriären i dessa tumörer i stort förblev relativt intakt, och att subtila skillnader mellan modeller och subgrupper kan påverka hur lätt molekyler passerar från blod till tumörvävnad.
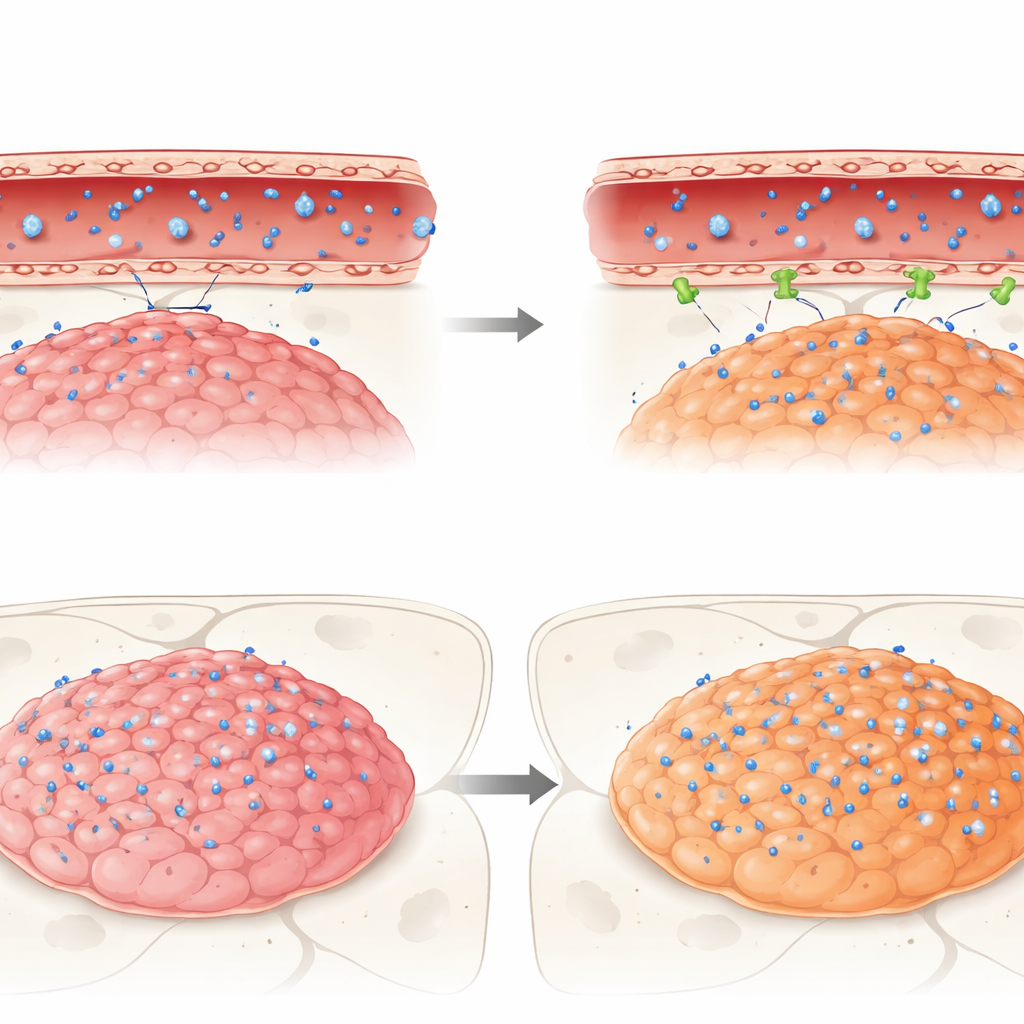
Vad som händer när verkliga läkemedel försöker passera
Slutligen följde forskarna tre kliniskt relevanta anticancermediciners—idasanutlin, temsirolimus och etoposid—resa in i dessa mus‑tumörer. Alla tre var aktiva mot ependymomceller i odlingsskålar, men i levande hjärnor mötte de barriären. Idasanutlin, även om det kemiskt var lämpat att korsa cellmembran, nådde mycket låga nivåer i både tumör och normal hjärna jämfört med blod, vilket tyder på stark utestängning av barriären. I kontrast ackumulerades temsirolimus och etoposid, båda kända för att kunna pumpas ut av vissa transportörer, mer i tumörer som tillhör en aggressiv subgrupp (ZFTA‑fusion‑positiv) än i en annan grupp (PFA) eller i den intilliggande friska hjärnan. Ändå nådde inget av läkemedlen koncentrationer i tumörer som motsvarade deras effektiva nivåer in vitro, vilket understryker hur barriären kan tyst sabotera lovande behandlingar.
Vad detta betyder för framtida behandlingar
För en lekman är huvudbudskapet tydligt: ependymomtumörer sitter inte alla bakom samma typ av hjärnport. I stället har varje molekylär subgrupp sin egen version av blod‑hjärnbarriären—ofta förvånansvärt tät—som formar hur väl olika läkemedel når sina mål. Genom att kombinera flera datalager från patienter och musmodeller visar detta arbete att förstå och mäta dessa subgruppsspecifika barriäregenskaper är avgörande för att utforma smartare kliniska prövningar. I stället för att anta att ett läkemedel som dödar tumörceller i en skål också kommer att fungera i ett barns hjärna, kan framtida terapier behöva väljas—och eventuellt kombineras med strategier som modifierar barriären—baserat på hur varje tumörs väktare är uppbyggda.
Citering: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Nyckelord: ependymom, blod‑hjärnbarriär, pediatriska hjärntumörer, Läkemedelsleverans, multi‑omik