Clear Sky Science · it
Differenze del sangue-cervello specifiche per sottogruppi di ependimoma svelate da un approccio multi-omico
Perché i guardiani del cervello sono importanti per i bambini con il cancro
Il cervello umano è protetto da un sistema di sicurezza naturale chiamato barriera emato-encefalica, uno strato compatto di cellule che controlla rigorosamente quali sostanze possono entrare nel tessuto cerebrale dal flusso sanguigno. Questa barriera è vitale per la salute, ma rende anche molto più difficile far arrivare i farmaci antitumorali ai tumori cerebrali, soprattutto nei bambini. Questo studio pone una domanda apparentemente semplice ma di grande rilevanza clinica: i diversi sottotipi di un tumore cerebrale pediatrico chiamato ependimoma sono “protetti” da tipi diversi di barriere, e questo potrebbe aiutare a spiegare perché molti farmaci falliscono?
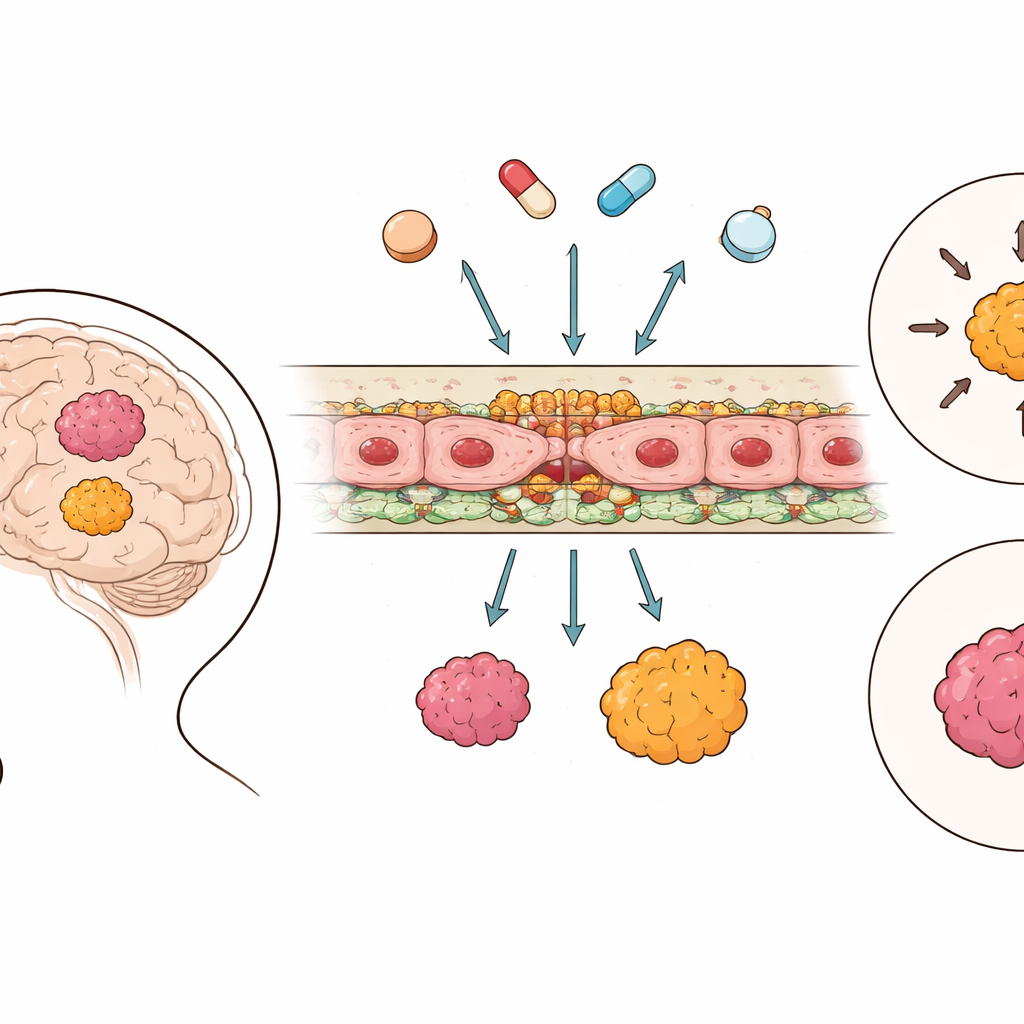
Il muro protettivo del cervello
La barriera emato-encefalica è costituita dalle cellule che rivestono i piccoli vasi cerebrali, tenute insieme da giunzioni specializzate e dotate di “pompe” molecolari in grado di rimandare i farmaci nel circolo sanguigno. Utilizzando dati genetici su larga scala provenienti da 364 tumori ependimomi e 225 campioni di cervello sano, i ricercatori hanno catalogato l’attività dei geni coinvolti in queste giunzioni e nei sistemi di trasporto. Hanno riscontrato che, a differenza di molti altri tumori cerebrali, il tessuto ependimale mostrava in realtà un’attività più elevata dei componenti chiave delle giunzioni rispetto al cervello sano, suggerendo che la barriera tra sangue e tumore è spesso più stretta anziché più permeabile. Al contrario, le pompe di efflusso dei farmaci e altri trasportatori seguivano schemi più variegati e specifici per sottogruppo invece di un semplice andamento acceso/spento.
Non è soltanto posizione o età, ma il tipo di tumore
Successivamente, il gruppo ha valutato se le differenze normali nello sviluppo o nell’anatomia cerebrale potessero spiegare questi schemi. Addestrando punteggi basati su reti neurali che riassumono l’attività dei geni delle giunzioni e dei trasportatori, hanno confermato caratteristiche note nei cervelli sani: la tenuta della barriera varia con l’età e differisce tra regioni come la corteccia e il cervelletto. Tuttavia, queste tendenze legate all’età e alla regione non si ritrovavano nei tumori. Nei principali gruppi intracranici di ependimoma, i punteggi correlati alla barriera apparivano simili indipendentemente dal punto del cervello in cui il tumore era insorto o dall’età del paziente. Ciò indica che è l’identità molecolare del tumore stesso—il suo sottogruppo—a essere il principale motore del comportamento della barriera locale.
Ingrandire le cellule della barriera
Le misure in bulk possono mascherare quali cellule sono effettivamente responsabili dell’attività genica osservata. Per risolvere questo punto, i ricercatori si sono rivolti al sequenziamento dell’RNA a cellula singola e a singolo nucleo proveniente da più coorti di pazienti e da un nuovo set di validazione. Questi dati più dettagliati hanno rivelato che la maggior parte dei geni correlati alla barriera è concentrata in un sottogruppo distinto di cellule dei vasi sanguigni presenti nel microambiente tumorale. Questa sottopopolazione endoteliale specializzata mostrava una forte espressione di geni classici delle giunzioni come CLDN5 e di altri marker della barriera, mentre le cellule tumorali, immunitarie e di supporto esprimevano molto poco. I risultati sono stati rafforzati da misurazioni proteiche e imaging avanzato, che hanno mostrato queste proteine allinearsi fisicamente sui vasi sanguigni tumorali, confermando che i segni genetici riflettono una vera barriera strutturale.
Testare la barriera in modelli murini
Poiché i nuovi farmaci vengono spesso valutati in modelli murini prima di arrivare ai pazienti, il gruppo ha esaminato se i xenotrapianti derivati da pazienti di diversi gruppi di ependimoma riproducessero le caratteristiche della barriera umana. In questi modelli le cellule tumorali prelevate dai pazienti crescono nel cervello dei topi, dove i vasi sanguigni sono per lo più di origine murina. Le analisi di RNA e proteine hanno nuovamente mostrato una forte espressione delle giunzioni nelle cellule vascolari, ma con alcune differenze tra modelli e tra tumore e cervello circostante. L’imaging con agenti di contrasto e traccianti fluorescenti ha suggerito che, nel complesso, la barriera in questi tumori rimaneva relativamente intatta e che differenze sottili tra modelli e sottogruppi possono influenzare quanto facilmente le molecole passano dal sangue al tessuto tumorale.
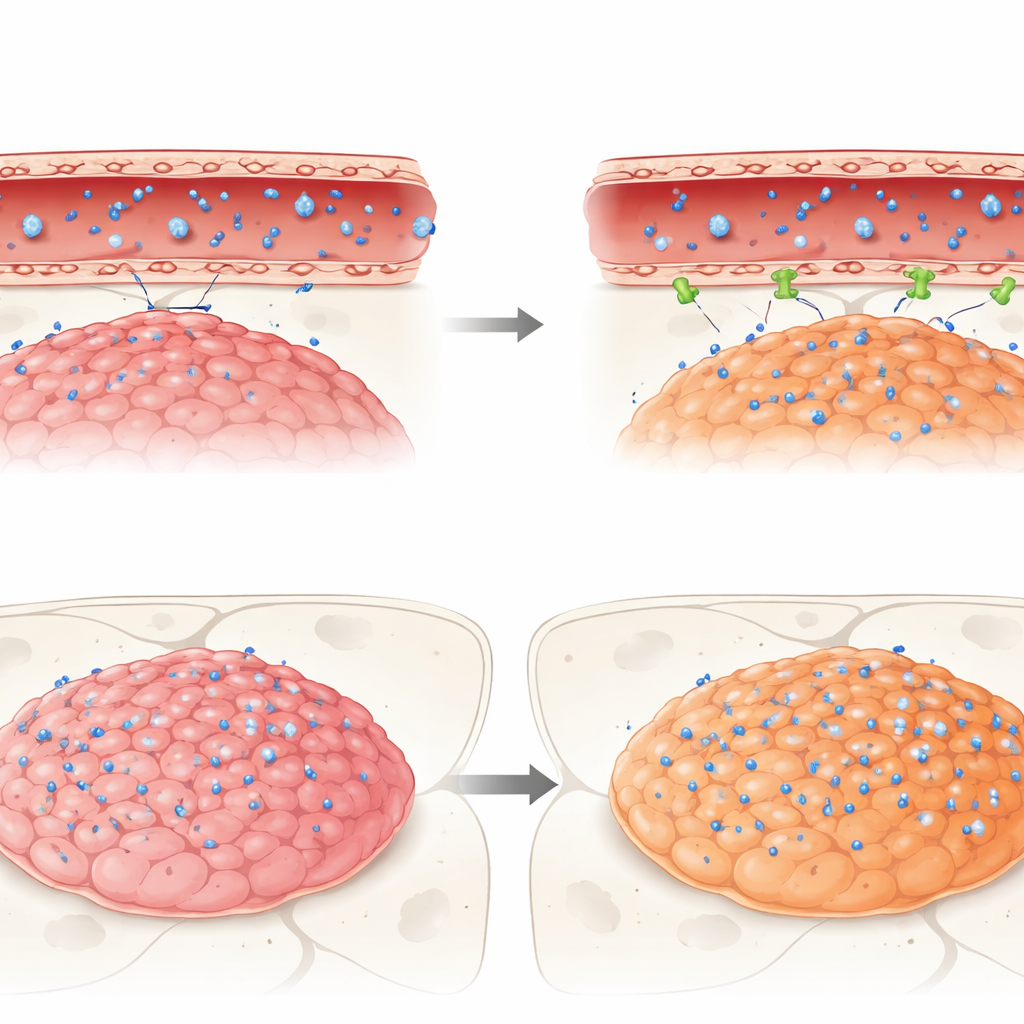
Cosa succede quando i farmaci reali provano a attraversare
Infine, i ricercatori hanno seguito il percorso di tre farmaci anticancro clinicamente rilevanti—idasanutlin, temsirolimus ed etoposide—verso questi tumori murini. Tutti e tre erano attivi contro le cellule di ependimoma in coltura, ma nei cervelli viventi si sono scontrati con la barriera. Idasanutlin, pur essendo chimicamente adatto ad attraversare le membrane cellulari, ha raggiunto livelli molto bassi sia nel tumore sia nel cervello normale rispetto al sangue, suggerendo una forte esclusione da parte della barriera. Al contrario, temsirolimus ed etoposide, entrambi noti per essere estrusi da determinate pompe, si sono accumulati maggiormente nei tumori appartenenti a un sottogruppo aggressivo (ZFTA fusion–positivo) rispetto a un altro gruppo (PFA) o al cervello sano adiacente. Anche così, nessuno dei farmaci ha raggiunto nei tumori concentrazioni comparabili ai livelli efficaci osservati in vitro, sottolineando come la barriera possa silenziosamente compromettere terapie promettenti.
Cosa significa questo per i trattamenti futuri
Per un lettore non specialista, il messaggio centrale è semplice: i tumori ependimali non sono tutti protetti dallo stesso tipo di “porta” cerebrale. Ogni sottogruppo molecolare porta con sé la propria versione della barriera emato-encefalica—spesso sorprendentemente stretta—which influenza quanto bene diversi farmaci possono raggiungere i loro bersagli. Integrando più livelli di dati provenienti da pazienti e modelli murini, questo lavoro mostra che comprendere e misurare i tratti della barriera specifici per sottogruppo è essenziale per progettare trial clinici più intelligenti. Invece di presumere che un farmaco che uccide le cellule tumorali in vitro funzioni nel cervello di un bambino, le future terapie potrebbero dover essere scelte—e possibilmente abbinate a strategie di modifica della barriera—sulla base di come sono costruiti i “guardiani” di ciascun tumore.
Citazione: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Parole chiave: ependimoma, barriera emato-encefalica, tumori cerebrali pediatrici, somministrazione di farmaci, multi-omica