Clear Sky Science · ar
اكتشاف فروق خاصة بمجموعة الإبينديموما في حاجز الدماغ بواسطة نهج متعدد - أومكس
لماذا يهم حراس الدماغ للأطفال المصابين بالسرطان
الدماغ البشري محمي بشدة بواسطة نظام أمني طبيعي يُسمى حاجز الدم-الدماغ، وهو طبقة محكمة من الخلايا تتحكم بدقة في المواد التي يمكن أن تدخل نسيج الدماغ من مجرى الدم. هذا الحاجز ضروري للصحة، لكنه يجعل كذلك من الصعب جداً إدخال أدوية السرطان إلى أورام الدماغ — لا سيما لدى الأطفال. تطرح هذه الدراسة سؤالاً بسيطاً بمظهره لكنه ذو تبعات سريرية كبيرة: هل تعيش أنواع فرعية مختلفة من ورم دماغي طفولي يُدعى الإبينديموما خلف أنواع مختلفة من الحواجز، وهل يمكن أن يفسر ذلك سبب فشل العديد من الأدوية؟
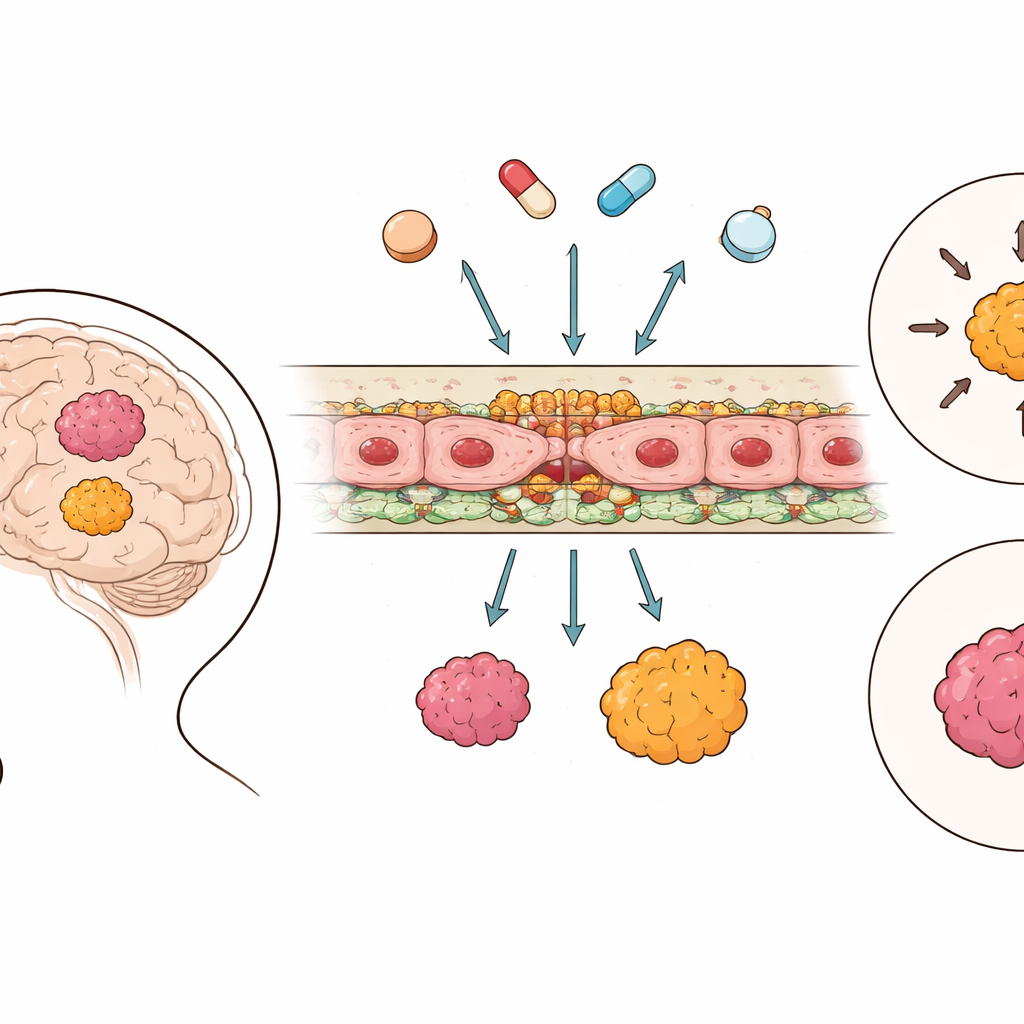
الجدار الواقي للدماغ
يتكون حاجز الدم-الدماغ من خلايا مبطنة للأوعية الدموية الدقيقة في الدماغ مرتبطة ببعضها بواسطة وصلات متخصصة، ومزودة بـ«مضخات» جزيئية يمكنها طرد الأدوية مرة أخرى إلى مجرى الدم. باستخدام بيانات جينية واسعة النطاق من 364 ورم إبينديموما و225 عينة من دماغ صحي، قام الباحثون بفهرسة نشاط الجينات المشاركة في هذه الوصلات وأنظمة النقل. وجدوا أنه، على خلاف ما يحدث في كثير من سرطانات الدماغ الأخرى، أظهر نسيج الإبينديموما نشاطاً أعلى لمكونات الوصلات الرئيسية مقارنة بالدماغ الصحي، ما يوحي بأن الحاجز بين الدم والورم غالباً ما يكون أكثر إحكاماً بدلاً من أن يكون متسرباً. بالمقابل، اتبعت مضخات طرد الأدوية والناقلات الأخرى أنماطاً أكثر خلطاً ومحددة حسب المجموعة بدلاً من اتجاه بسيط تشغيل/إيقاف.
ليس مجرد موقع أو عمر، بل نوع الورم
سأل الفريق بعد ذلك ما إذا كانت الاختلافات الطبيعية في تطور الدماغ أو تشريحه قد تفسر هذه الأنماط. عن طريق تدريب درجات شبكات عصبية تلخص نشاط جينات الوصلات والناقلات، أكّدوا ميزات معروفة في الأدمغة السليمة: تتغير إحكامية الحاجز مع العمر وتختلف بين مناطق مثل القشرة والمخيخ. غير أن هذه الاتجاهات العمرية والمنطقية لم تمتد إلى الأورام. عبر المجموعات الرئيسية للإبينديموما داخل القحف، بدت درجات المتعلّقة بالحاجز متشابهة بغض النظر عن مكان نشوء الورم في الدماغ أو عمر المريض. هذا يشير إلى أن الهوية الجزيئية للورم نفسه — مجموعته الفرعية — هي المحرّك الرئيسي لكيفية تصرف حاجزه المحلي.
التدقيق في خلايا الحاجز
يمكن أن تُخفي القياسات الكمية الإجمالية أي الخلايا المسؤولة فعلياً عن النشاط الجيني المرصود. لحل ذلك، لجأ الباحثون إلى تسلسل RNA أحادي الخلية ونوى الخلية من مجموعات مرضى متعددة ومجموعة تحقق جديدة. كشفت هذه البيانات الأكثر تفصيلاً أن معظم الجينات المتعلقة بالحاجز مركّزة في فرع فرعي متميز من خلايا الأوعية الدموية داخل بيئة الورم. أظهرت هذه الشعبة البطانية المتخصصة تعبيراً قوياً لجينات الوصلات الكلاسيكية مثل CLDN5 وعلامات حاجز أخرى، بينما عبّرت خلايا الورم والخلايا المناعية وخلايا الدعم قليلاً جداً. دعمت القياسات البروتينية والتصوير المتقدم هذه النتائج، حيث أظهرت هذه البروتينات مبطنة فعلياً لأوعية الورم الدموية، مؤكدة أن البصمات الجينية تعكس حاجزاً بنيوياً حقيقياً.
اختبار الحاجز في نماذج الفئران
لأن الأدوية الجديدة غالباً ما تُقيّم في نماذج الفئران قبل أن تصل إلى المرضى، اختبر الفريق ما إذا كانت الزرعات المأخوذة من المرضى لمجموعات إبينديموما مختلفة تعيد إنتاج خصائص الحاجز البشري. في هذه النماذج، تنمو خلايا الورم المأخوذة من المرضى في أدمغة الفئران، حيث تكون الأوعية الدموية في الغالب مشتقة من الفأر. أظهرت تحليلات RNA والبروتين مرة أخرى تعبيراً قوياً للوصلات في خلايا الأوعية، لكن مع بعض الاختلافات بين النماذج وبين الورم والدماغ المحيط. أوضح التصوير باستخدام عوامل التباين وآثار متوهجة أن الحاجز في هذه الأورام ظل عموماً محافظاً نسبياً، وأن الفروق الطفيفة بين النماذج والمجموعات الفرعية قد تؤثر في مدى سهولة مرور الجزيئات من الدم إلى نسيج الورم.
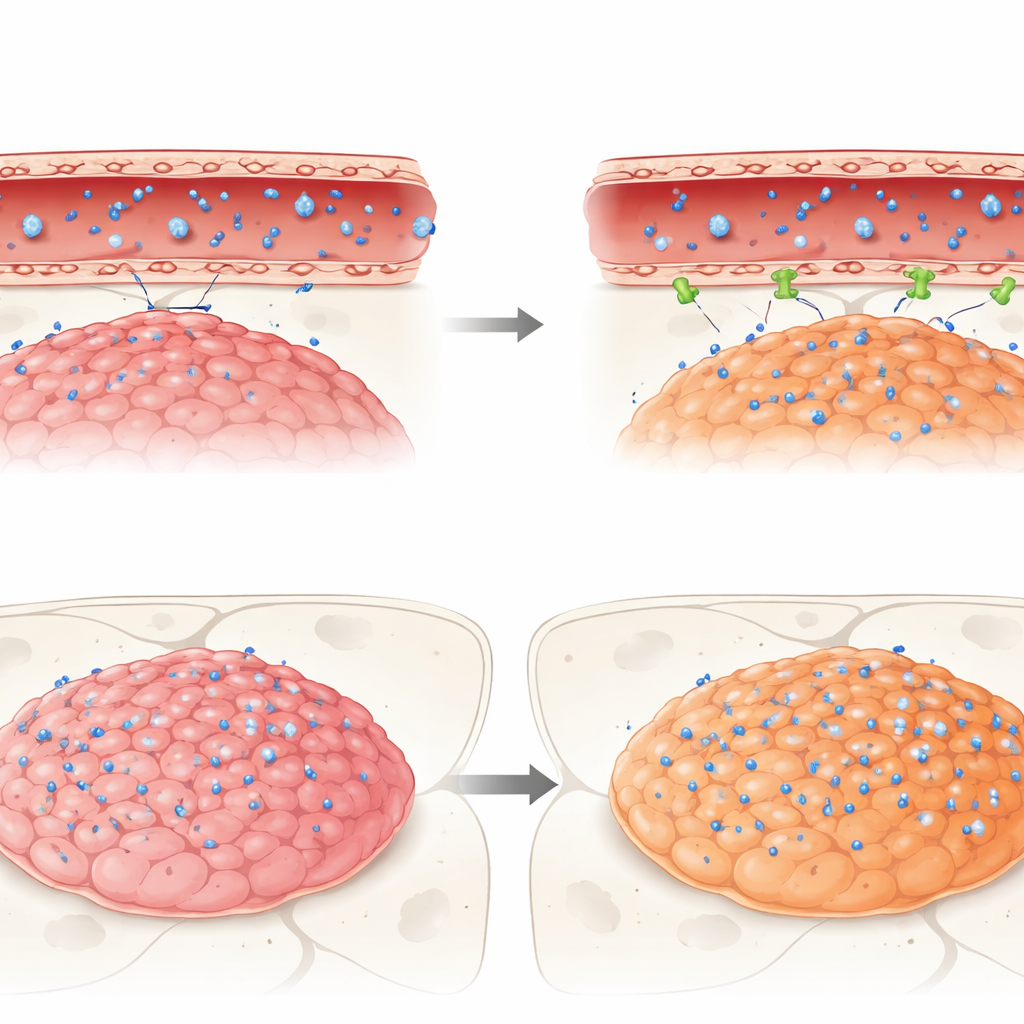
ماذا يحدث عندما تحاول أدوية حقيقية العبور
أخيراً تابع الباحثون مسار ثلاثة أدوية مضادة للسرطان ذات صلة سريرية — إيداسانوتلين، تمسيروليموس وإيتوبوسايد — إلى هذه الأورام في الفئران. كانت كل الأدوية الثلاثة فعالة ضد خلايا الإبينديموما في الأطباق، لكنها واجهت الحاجز في الأدمغة الحية. وصل إيداسانوتلين، رغم كونه مؤهلاً كيميائياً لعبور أغشية الخلايا، إلى مستويات منخفضة جداً في كل من الورم والدماغ الطبيعي مقارنة بالدم، مما يشير إلى استبعاد قوي بواسطة الحاجز. بالمقابل، تراكم كل من تمسيروليموس وإيتوبوسايد — والمعروف أنه يتم طردهما بواسطة مضخات معينة — أكثر في أورام تنتمي إلى مجموعة عدوانية واحدة (موجبة للاندماج ZFTA) مقارنة بمجموعة أخرى (PFA) أو الدماغ السليم المجاور. ومع ذلك، لم تصل أي من الأدوية إلى تراكيز في الأورام تطابق مستوياتها الفعالة التي لوحظت في المختبر، مما يبرز كيف يمكن للحاجز أن يقوض الصفقات العلاجية الواعدة بهدوء.
ما الذي يعنيه هذا للعلاجات المستقبلية
للقارئ العام، الرسالة الأساسية واضحة: أورام الإبينديموما لا تجلس جميعها خلف نفس نوع بوابة الدماغ. بدلاً من ذلك، تأتي كل مجموعة جزيئية بنسختها الخاصة من حاجز الدم-الدماغ — وغالباً ما تكون ضيقة بشكل مفاجئ — والتي تشكل مدى قدرة الأدوية المختلفة على الوصول إلى أهدافها. من خلال دمج طبقات بيانات متعددة من المرضى ونماذج الفئران، تُظهر هذه الدراسة أن فهم وقياس خصائص الحاجز الخاصة بكل مجموعة فرعية أمر أساسي لتصميم تجارب سريرية أذكى. بدلاً من افتراض أن دواءً يقتل خلايا الورم في طبق سيعمل في دماغ طفل، قد تحتاج العلاجات المستقبلية أن تُختار — وربما تُقرن باستراتيجيات تعديل الحاجز — استناداً إلى كيفية بناء حراس كل ورم.
الاستشهاد: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
الكلمات المفتاحية: الإبينديموما, حاجز الدم-الدماغ, أورام الدماغ لدى الأطفال, توصيل الدواء, متعدد - أومكس