Clear Sky Science · tr
Q-CaDD: Epidermal growth factor receptor için kuantum hesaplama ve makine öğrenmesiyle in silico yöntemleri hızlandırma
Geleceğin kanser ilaçları için yeni bilgisayar araçlarının önemi
Yeni ilaç tasarlamak, olası moleküller yığınında iğne aramaya benzer. Epidermal Büyüme Faktörü Reseptörü (EGFR) adlı bir proteinin yol açtığı kanserlerde, araştırmacıların bu proteine güçlü bağlanan ancak hastalar için güvenli kalan bileşikleri bulması gerekir. Bu makale, günümüz makine öğrenmesini yükselen kuantum hesaplama fikirleriyle harmanlayan ve yüz binlerce aday molekülü daha verimli elekten geçirmeyi, potansiyel olarak daha güvenli ve etkili ilaç adaylarını öne çıkarmayı amaçlayan bilgisayar tabanlı bir çerçeve olan Q-CaDD’yi tanıtıyor.
Kanserle ilişkili bir proteinden dijital bir arama problemine
EGFR hücre yüzeyinde yer alır ve hücrelerin nasıl büyüyüp bölüneceğini kontrol etmeye yardımcı olur. Non-small cell akciğer kanserinde olduğu gibi işlev bozukluğu olduğunda hücreler kontrolsüz çoğalabilir. EGFR’yi engelleyen ilaçlar zaten mevcut, ancak kanserler direnç geliştirebilir ve her hasta iyi yanıt vermez. Yeni bileşikleri laboratuvarda tek tek test etmek yerine Q-CaDD, kimyasal alanı toplu olarak keşfetmek için bilgisayar simülasyonlarını kullanır; hem EGFR’ye bağlanan hem de düşük toksisite işaretleri gösteren molekülleri arar. Bu yaklaşım, ilaç keşfinin erken adımlarını daha hızlı, daha ucuz ve daha yönlendirilmiş hale getirmeyi amaçlar.
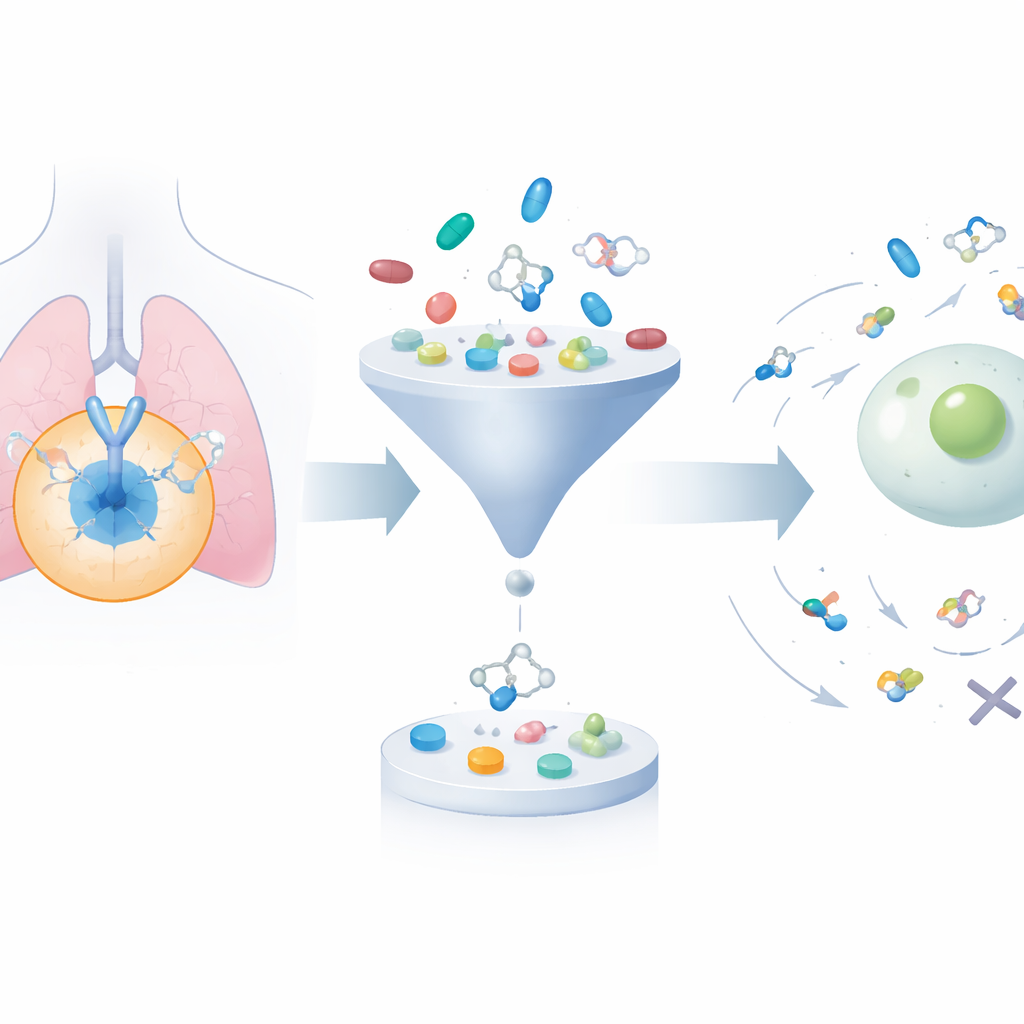
Kocaman bir molekül kütüphanesini büyütmek ve budamak
Çerçeve, halka açık veritabanlarından yaklaşık 24.000 bilinen EGFR engelleyici molekülü toplayarak başlar. Ardından generatif bir algoritma kullanarak yapıları sistematik şekilde değiştirir ve yaklaşık 200.000 ilişkili aday üretir. Çok hacimli, çok yağlı veya vücutta düzgün davranma olasılığı düşük bileşikleri elemek için iki iyi yerleşmiş “ilaç benzeri” filtre uygulanır ve küme 50.000’den aza düşürülür. Sonrasında bir docking programı her molekülü EGFR üzerindeki üç boyutlu bağlanma ceplerine sanal olarak uydurarak her birinin ne kadar güçlü bağlanabileceğini tahmin eder. Bu, hem kimyasal olarak makul hem de hedefle iyi etkileşmesi öngörülen bileşiklere odaklanmayı sağlar.
Bilgisayarlara toksik uyarı işaretlerini öğretmek
EGFR’ye bağlanma hikâyenin yalnızca yarısıdır; umut verici bir bileşik aynı zamanda sağlıklı dokulara zarar vermemelidir. Toksisiteyi tahmin etmek için çalışma, çeşitli hücresel yolakları etkileyen 10.000’den fazla kimyasalı kaydeden büyük bir halka açık veri seti olan Tox21’e başvurur. Yazarlar iyi anotasyonlu ve birkaç kanser türüyle biyolojik olarak ilişkili olduğu için androjen reseptörüyle bağlantılı bir yol üzerine odaklanır. Her Tox21 molekülü, yapısal özelliklerini ve diğer kimyasallarla benzerliklerini yakalayan sayısal bir parmak izine çevrilir. Bu parmak izleri, sinir ağları, karar ağaçları, klasik bir destek vektör makinesi ve bileşikleri farklı bir matematiksel uzayda karşılaştırmak için basit bir kuantum devresi kullanan kuantum-esinlenimli bir destek vektör makinesi dahil olmak üzere birkaç öngörücü modele beslenir.
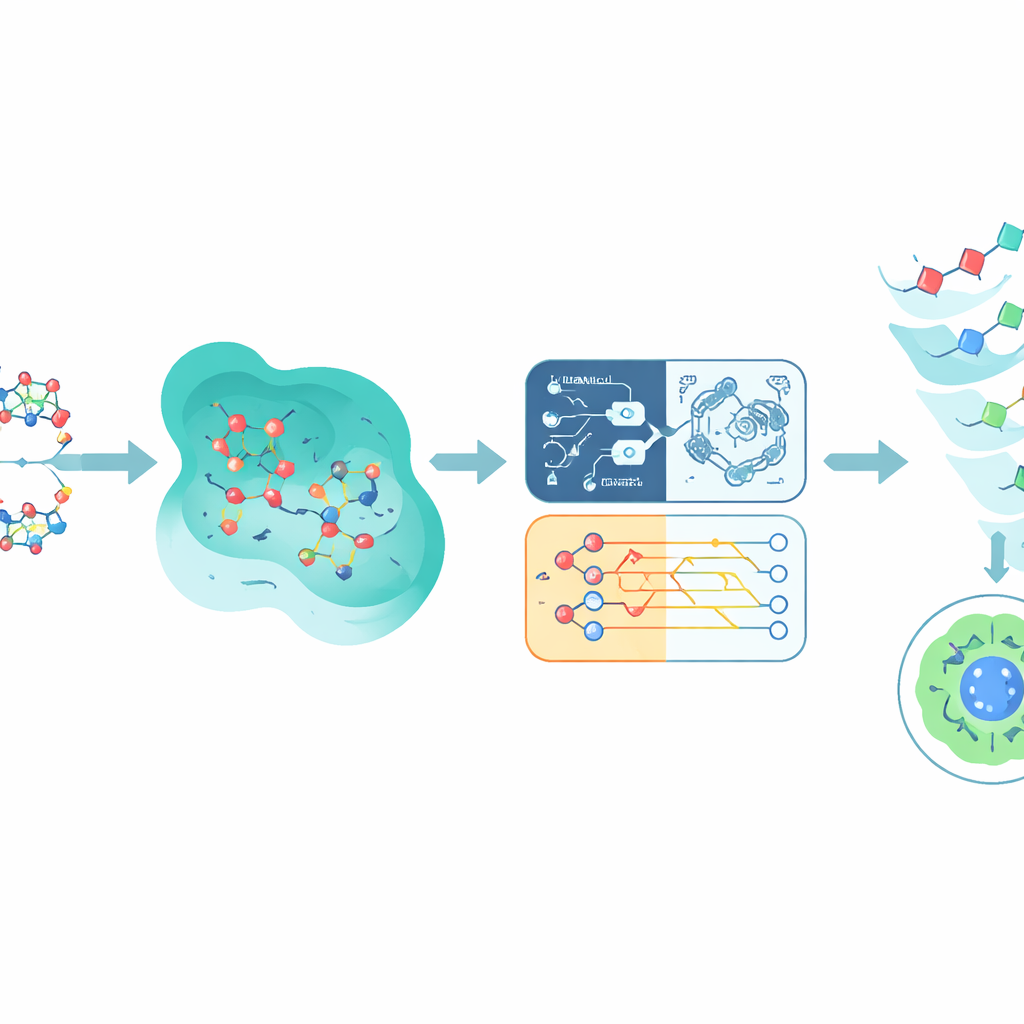
Kuantum ve klasik tahminleri harmanlamak
Tek bir modele yatırım yapmak yerine Q-CaDD, dördünün çıktısını bir araya getiren bir topluluk (ensemble) kullanır; en büyük ağırlığı sinir ağına verirken, yine de kuantum modelinden gelen daha zayıf ancak farklı sinyali dahil eder. Daha önce görülmemiş Tox21 verileri üzerinde test edildiğinde, bu birleşik yaklaşım ROC eğrisi altındaki alan adı verilen standart bir sıralama skoru ile ölçüldüğünde daha az ve daha toksik bileşikleri ayırt etmede herhangi bir tek modelden daha iyi performans gösterir. İyileşme mütevazı olmakla birlikte ve kuantum kısmı gerçek bir kuantum çipi yerine simülatörde çalıştırılsa da, sonuçlar kuantum-esinlenimli yöntemlerin mevcut makine öğrenmesi boru hatlarına erken aşamalarda bile faydalı nüans katabileceğini öne sürer.
Bilgisayar puan kartlarından gelecekteki laboratuvar testlerine
Toksisite modellerini doğruladıktan sonra yazarlar Q-CaDD’nin tam boru hattını filtrelenmiş EGFR odaklı kütüphaneye uygular. Toksisite konusunda sert bir evet-hayır kararı vermekten kaçınır, bunun yerine sürekli risk puanlarını korur ve bunları bağlanma gücünün docking tahminleriyle birleştirir. Bu, referans bir ilaçtan daha güçlü bağlanıyor gibi görünen ve düşük öngörülen toksisiteyi koruyan bazı aday molekülleri içeren öncelik listesi üretir. Bu moleküller yeni ilaçlar olarak iddia edilmez; laboratuvar testlerine değer adaylar olarak işaretlenirler. Çalışmanın uzman olmayanlar için ana çıkarımı, kuantum bilgisayarların ilaç keşfini zaten devrimleştirdiği değil; klasik ve kuantum-esinlenimli araçların dikkatle tasarlanmış hibritlerinin, mevcut donanım sınırlamalarına gerçekçi kalarak aramayı keskinleştirmeye ve araştırmacıları daha iyi ilaç adaylarına daha hızlı yönlendirmeye şimdiden yardımcı olabileceğidir.
Atıf: Badarala, L. Q-CaDD: accelerating in silico methodologies with quantum computation and machine learning for Epidermal growth factor receptor. Sci Rep 16, 14436 (2026). https://doi.org/10.1038/s41598-026-44978-4
Anahtar kelimeler: kuantum ilaç keşfi, EGFR inhibitörleri, makine öğrenmesi toksisite, sanal tarama, küçük hücre dışı akciğer kanseri