Clear Sky Science · ru
Q-CaDD: ускорение in silico методик с помощью квантовых вычислений и машинного обучения для рецептора эпидермального фактора роста
Почему новые компьютерные инструменты важны для будущих противораковых препаратов
Проектирование новых лекарств похоже на поиск иголки в стоге сена возможных молекул. Для опухолей, обусловленных белком под названием рецептор эпидермального фактора роста (EGFR), исследователям нужно найти соединения, которые прочно связываются с этим белком и при этом безопасны для пациентов. В этой статье представлен Q-CaDD — компьютерная платформа, которая объединяет современное машинное обучение с идеями развивающихся квантовых вычислений, чтобы эффективнее просеивать сотни тысяч кандидатных молекул и отмечать те, которые потенциально могут стать более безопасными и эффективными лекарствами.
От белка, связанного с раком, к цифровой задаче поиска
EGFR расположен на поверхности клеток и помогает контролировать их рост и деление. Когда он работает неправильно, как часто бывает при немелкоклеточном раке лёгкого, клетки могут бесконтрольно размножаться. Препараты, блокирующие EGFR, уже существуют, но раковые клетки могут приобретать устойчивость и не каждый пациент отвечает на лечение. Вместо того чтобы испытывать новые соединения по одному в лаборатории, Q-CaDD использует компьютерные симуляции для массового исследования химического пространства, ища молекулы, которые одновременно связываются с EGFR и демонстрируют низкую токсичность. Такой подход призван сделать ранние этапы открытия лекарств быстрее, дешевле и более целенаправленными.
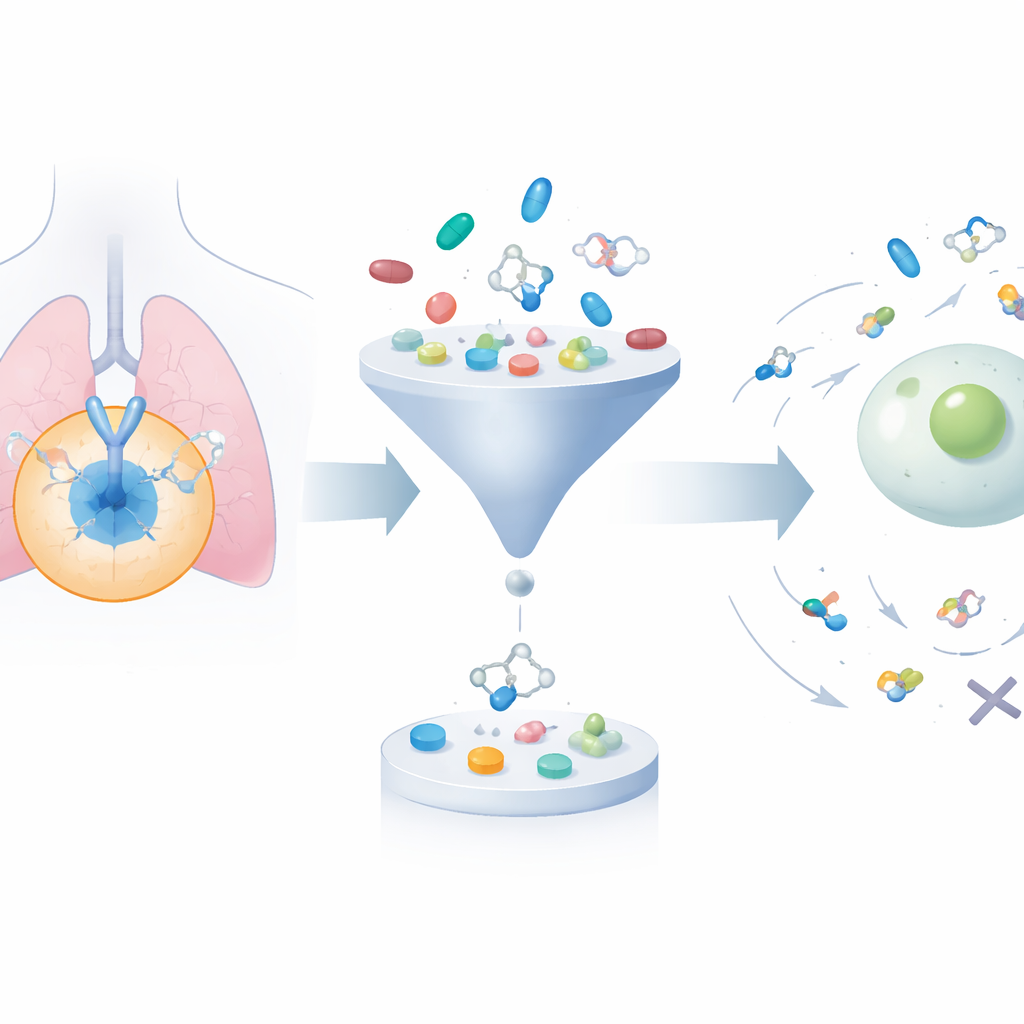
Расширение и сокращение обширной библиотеки молекул
Платформа начинается со сбора около 24 000 известных молекул, блокирующих EGFR, из публичных баз данных. Затем используется генеративный алгоритм для систематической модификации их структур, что даёт примерно 200 000 родственных кандидатов. Применяются два общепринятых фильтра «drug-likeness», чтобы отсеять соединения, слишком громоздкие, слишком липкие или иным образом вряд ли пригодные для организма, сокращая набор до менее чем 50 000. Далее программа докинга виртуально помещает каждую молекулу в трёхмерную щель на EGFR, где реальные лекарства связываются, оценивая, насколько сильно каждое соединение может прикрепляться. Это сужает внимание к соединениям, которые и химически разумны, и, по прогнозам, хорошо взаимодействуют с мишенью.
Обучение компьютеров распознавать признаки токсичности
Связывание с EGFR — это лишь часть истории; перспективное соединение также не должно вредить здоровым тканям. Для оценки токсичности исследование обращается к большой публичной базе данных Tox21, в которой записано, как более 10 000 химикатов влияют на различные клеточные пути. Авторы сосредотачиваются на одном пути, связанном с андрогенным рецептором, выбранном потому, что он хорошо аннотирован и биологически релевантен для нескольких видов рака. Каждая молекула из Tox21 переводится в числовой «отпечаток», фиксирующий её структурные признаки и сходства с другими химическими веществами. Эти отпечатки питают несколько предиктивных моделей, включая нейронные сети, решающие деревья, традиционный метод опорных векторов и квантово-вдохновлённый метод опорных векторов, использующий простую квантовую схему для сравнения соединений в иной математической области.
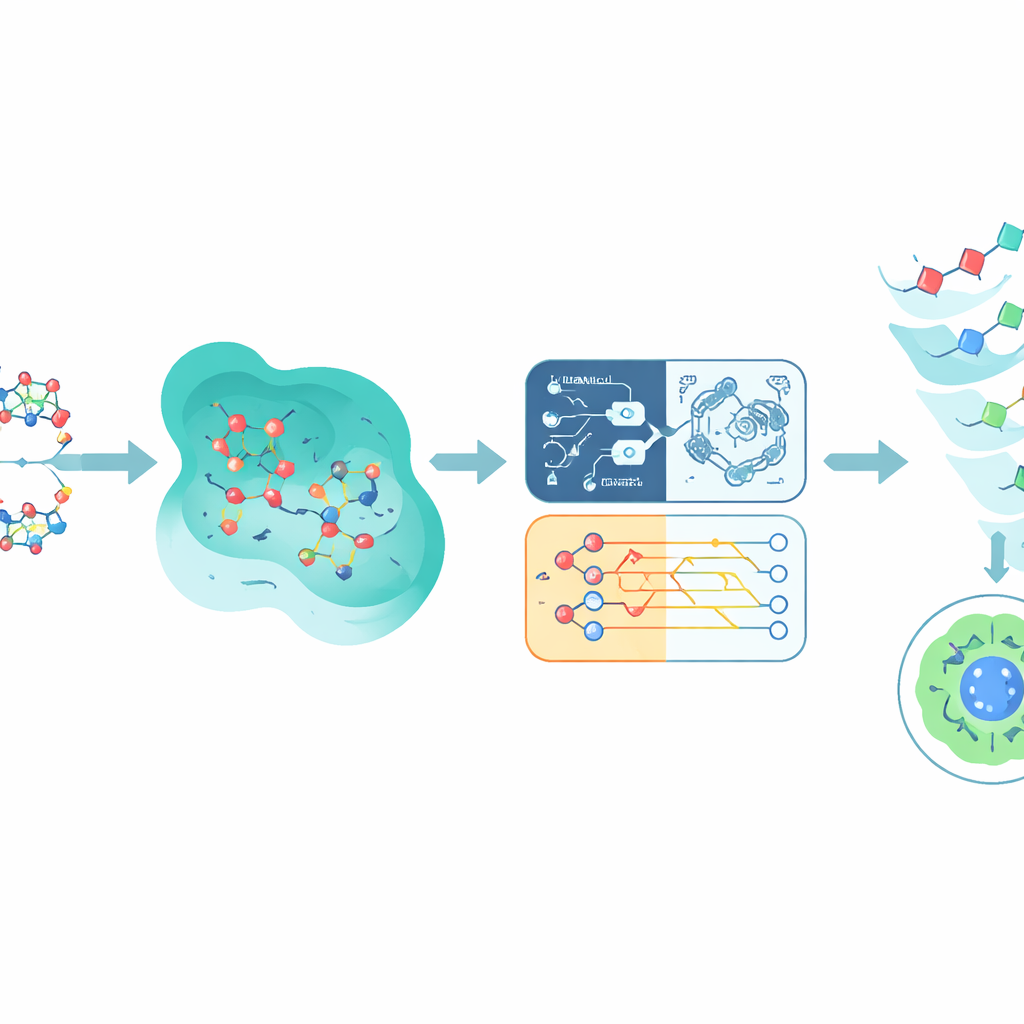
Смешение квантовых и классических предсказаний
Вместо того чтобы полагаться на одну модель, Q-CaDD объединяет выходы всех четырёх в ансамбль, отдавая наибольший вес нейронной сети, но при этом сохраняя слабый, но отличающийся сигнал от квантовой модели. При проверке на ранее не встречавшихся данных Tox21 такой смешанный подход превосходит любую отдельную модель в различении более и менее токсичных соединений, измеряемом стандартной метрикой — площадью под ROC-кривой. Хотя улучшение скромное, и квантовая часть всё ещё запускается на симуляторе, а не на реальном квантовом чипе, результаты указывают на то, что квантово-вдохновлённые методы уже могут добавлять полезные нюансы к существующим конвейерам машинного обучения даже на ранних этапах развития технологий.
От компьютерных оценок к будущим лабораторным испытаниям
После валидации моделей токсичности авторы применяют полный конвейер Q-CaDD к отфильтрованной библиотеке, ориентированной на EGFR. Они избегают жёсткого двоичного суждения о токсичности, сохраняя непрерывные оценки риска и комбинируя их с оценками докинга силы связывания. Это даёт приоритетный список кандидатов, некоторые из которых, по прогнозам, связываются с EGFR сильнее, чем референсный препарат, при сохранении низкой предсказанной токсичности. Эти молекулы не заявляются как новые лекарства; их отмечают как лиды, которые заслуживают лабораторного тестирования. Основной вывод исследования для неспециалистов не в том, что квантовые компьютеры уже полностью перевернули открытие лекарств, а в том, что тщательно спроектированные гибриды классических и квантово-вдохновлённых инструментов уже могут помочь сузить поиск, направляя исследователей к лучшим кандидатам быстрее, оставаясь реалистичными относительно текущих аппаратных ограничений.
Цитирование: Badarala, L. Q-CaDD: accelerating in silico methodologies with quantum computation and machine learning for Epidermal growth factor receptor. Sci Rep 16, 14436 (2026). https://doi.org/10.1038/s41598-026-44978-4
Ключевые слова: квантовое открытие лекарств, ингибиторы EGFR, токсичность машинное обучение, виртуальный скрининг, немелкоклеточный рак лёгкого