Clear Sky Science · ar
Q-CaDD: تسريع المنهجيات الحاسوبية عبر الحوسبة الكمّية وتعلّم الآلة لمستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبل مستقبلالمستقبل مستقبل مستقبل
لماذا الأدوات الحاسوبية الجديدة مهمة لأدوية السرطان المستقبلية
تصميم أدوية جديدة يشبه إلى حد كبير البحث عن إبرة في كومة من القش المليئة بالمركبات المحتملة. بالنسبة للسرطانات التي تحركها بروتين يُدعى مستقبل عامل نمو البشرة (EGFR)، يجب على الباحثين إيجاد مركبات ترتبط بهذا البروتين بقوة وتظل آمنة للمرضى. يقدم هذا البحث إطار عمل حاسوبي اسمه Q-CaDD، يمزج بين تقنيات تعلّم الآلة الحالية وأفكار الحوسبة الكمّية الناشئة لفرز مئات الآلاف من الجزيئات المرشحة بكفاءة أكبر ولتمييز تلك التي قد تصبح أدوية أكثر أماناً وفعالية.
من بروتين مرتبط بالسرطان إلى مسألة بحث رقمية
يوجد EGFR على سطح الخلايا ويساهم في التحكم في كيفية نموها وانقسامها. عند تعطّله—كما يحدث كثيراً في سرطان الرئة غير صغير الخلايا—يمكن أن تتكاثر الخلايا بلا ضابط. توجد أدوية تعيق EGFR بالفعل، لكن السرطانات قد تطوّر مقاومة، ولا يستجيب كل مريض بشكل جيد. بدلاً من اختبار مركبات جديدة واحداً تلو الآخر في المختبر، يستخدم Q-CaDD محاكيات حاسوبية لاستكشاف الفضاء الكيميائي بالجملة، بحثاً عن جزيئات ترتبط بـ EGFR وتظهر مؤشرات على سمّية منخفضة. تهدف هذه المقاربة إلى جعل الخطوات الأولى في اكتشاف الأدوية أسرع وأرخص وأكثر توجيهاً.
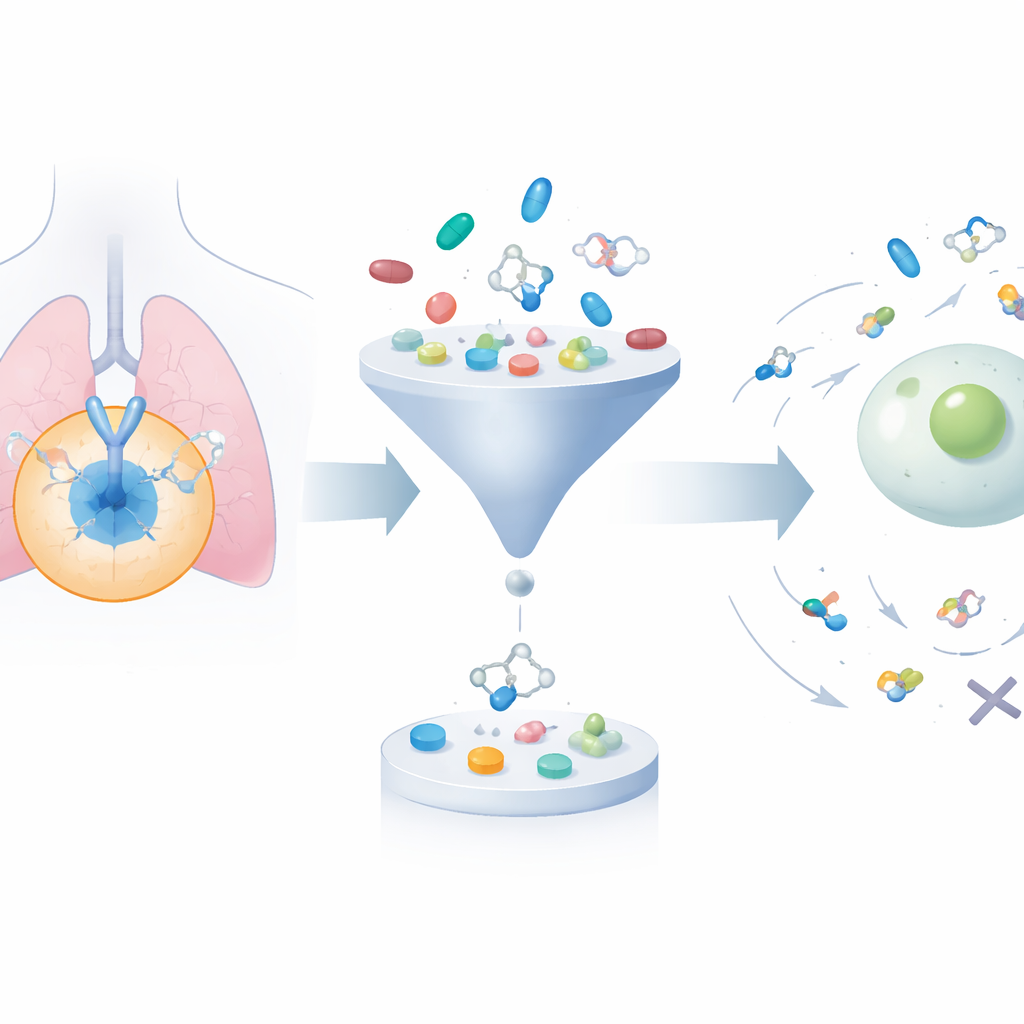
تكبير وتقليص مكتبة هائلة من الجزيئات
يبدأ الإطار بجمع نحو 24,000 جزيء معروف قادر على تثبيط EGFR من قواعد بيانات عامة. ثم يستخدم خوارزمية مولدة لتعديل هياكلها بشكل منهجي، منتِجاً نحو 200,000 مرشح ذي صلة. تُطبّق بعد ذلك مرشحات «شبه دوائية» معتمدة للتخلص من المركبات الكبيرة جداً أو الدهنية جداً أو غير المحتمل أن تتصرف جيداً داخل الجسم، ما يخفض المجموعة لأقل من 50,000. بعد ذلك، يقوم برنامج إرساء جزيئي بملاءمة كل جزيء افتراضياً في الجيب ثلاثي الأبعاد على EGFR حيث ستلتزم الأدوية الفعلية، مقدِّراً مدى قوة الارتباط المتوقعة لكل منها. هذا يضيق نطاق الاهتمام إلى المركبات المعقولة كيميائياً والتي يتوقع أن تتفاعل جيداً مع الهدف.
تعليم الحواسيب التعرف على علامات التحذير السمّية
الارتباط بـ EGFR هو نصف القصة؛ يجب أن يتجنّب المركب الواعد أيضاً إحداث ضرر للأنسجة السليمة. لتقدير السمّية، يلجأ البحث إلى مجموعة بيانات عامة كبيرة تسمى Tox21، التي تسجّل كيف تؤثر أكثر من 10,000 مادة كيميائية على مسارات خلوية مختلفة. يركز المؤلفون على مسار واحد مرتبط بمستقبل الأندروجين، اختير لأنه موثّق جيداً وذو صلة بيولوجية بعدة سرطانات. يُحوّل كل جزيء من Tox21 إلى بصمة رقمية تُعبّر عن خصائصه البنيوية وتشابهه مع مواد كيميائية أخرى. تُغذى هذه البصمات إلى عدة نماذج تنبؤية، بما في ذلك الشبكات العصبية، أشجار القرار، آلة الدعم الناقل التقليدية، وآلة دعم ناقل مستوحاة من الكمّ تستخدم دائرة كمّية بسيطة لمقارنة المركبات في فضاء رياضي مختلف.
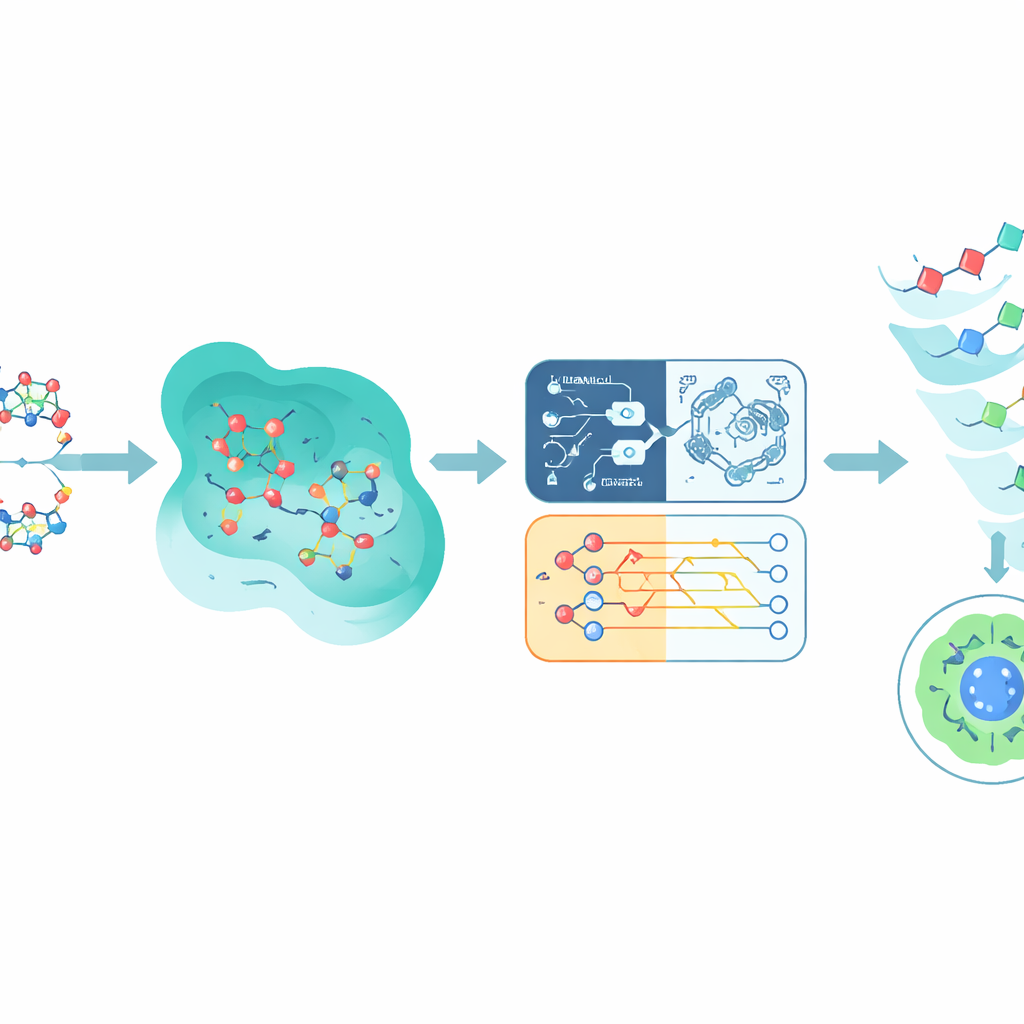
مزج التنبؤات الكمّية والكلاسيكية
بدلاً من الاعتماد على نموذج واحد، يجمع Q-CaDD مخرجات الأربعة في طقم متكامل (ensemble)، مع إعطاء الوزن الأكبر للشبكة العصبية مع الحفاظ على الإشارة الأضعف والمتميزة من النموذج الكمّي. عند اختباره على بيانات Tox21 غير المرئية سابقاً، يتفوق هذا المزج على أي نموذج فردي في التمييز بين المركبات الأكثر والأقل سمّية، كما يُقاس بواسطة معيار قياسي للتصنيف يعرف بمساحة تحت منحنى ROC. ومع أن التحسّن متواضع والجزء الكمّي لا يزال يعمل على محاكٍ بدل شريحة كمّية حقيقية، تشير النتائج إلى أن أساليب مستوحاة من الكمّ يمكن أن تضيف تميّزاً مفيداً إلى خطوط أنابيب تعلّم الآلة الحالية حتى في مراحلها الأولى.
من بطاقات درجات حاسوبية إلى اختبارات مخبرية مستقبلية
بعد التحقق من نماذج السمّية، يطبّق المؤلفون خط أنابيب Q-CaDD بالكامل على المكتبة المفلترة الموجهة إلى EGFR. يتجنّبون اتخاذ قرار صارم بنعم أو لا بشأن السمّية، ويحتفظون بدلاً من ذلك بدرجات مخاطرة مستمرة ويجمعونها مع تقديرات الإرساء لقوة الارتباط. ينتج عن ذلك قائمة أولويات من الجزيئات المرشحة، بعضها يبدو أنه يرتبط بـ EGFR بقوة أكبر من دواء مرجعي مع احتفاظه بمخاطر سمّية متوقعة منخفضة. هذه الجزيئات لا تُطرح كأدوية جديدة؛ بل تُوضع كمرشحات تستحق الفحص المخبري. الخلاصة الرئيسية للدراسة لغير المتخصصين ليست أن الحواسيب الكمّية قد أحدثت ثورة بالفعل في اكتشاف الأدوية، بل أن هجائناً مصممة بعناية من الأدوات الكلاسيكية والمستوحاة من الكمّ يمكنها حالياً تعزيز عملية البحث، موجهة الباحثين نحو مرشحين أفضل بسرعة أكبر مع المحافظة على الواقعية بخصوص حدود الأجهزة الحالية.
الاستشهاد: Badarala, L. Q-CaDD: accelerating in silico methodologies with quantum computation and machine learning for Epidermal growth factor receptor. Sci Rep 16, 14436 (2026). https://doi.org/10.1038/s41598-026-44978-4
الكلمات المفتاحية: اكتشاف الأدوية بالكمّيات, مثبطات EGFR, سمّية تعلّم الآلة, المسح الافتراضي, سرطان الرئة غير صغير الخلايا