Clear Sky Science · tr
Çocukluk çağı tümörleri genelinde makine öğrenimi ile tahmin edilen kromatin organizasyon manzarası
Genomun Katlanması Neden Hasta Çocuklar İçin Önemli
Çocukluk çağı beyin tümörleri, en ölümcül çocukluk çağı kanserleri arasında yer alır; yine de birçok genç hastada doktorlar DNA’da tam olarak neyin yanlış gittiğini hâlâ bilmiyor. Bu çalışma yeni bir açı sunuyor: yalnızca hangi genlerin mutasyona uğradığı değil, geniş DNA yeniden düzenlenmelerinin genomun her hücre içinde nasıl katlandığını nasıl değiştirdiği. Büyük kanser veri setlerini güçlü bir makine öğrenimi modeliyle birleştirerek yazarlar, bu 3B katlanma desenindeki gizli bozulmaların çocukluk çağı tümörlerini tetikliyor olabileceğini ve bilgisayarların artık daha fazla incelenmesi gereken en tehlikeli değişiklikleri işaretleyebileceğini gösteriyor.
Çocukluk Tümörlerindeki Büyük DNA Karışmaları
Genetik koddaki küçük yazım hatalarına odaklanmak yerine araştırmacılar yapısal varyantları inceledi—uzun DNA parçalarının büyük kesilme, kopyalanma, ters çevrilme ve yapıştırılma olayları. Bu ölçekli değişiklikler genleri birleştirebilir, koruyucu bölgeleri silebilir veya güçlü anahtarlar (enhancer’lar) yanlış genlerin yanına yerleşmesini sağlayabilir. Çalışma, Çocukların Beyin Tümörü Ağı’ndan (Children’s Brain Tumor Network) 61 tümör tipini kapsayan yaklaşık 1.900 çocuğun verilerini kullanarak neredeyse 300.000 böyle varyantı katalogladı. Lenfoma ve sarkom gibi bazı tümör gruplarında bu değişikliklerin diğerlerine göre çok daha fazla olduğunu, ayrıca başlangıç tedavisinden sonra nükseden veya ilerleyen tümörlerin genellikle orijinal tümörlerden daha fazla yapısal varyant taşıdığını buldular.
Genomu 3B Görmek İçin Yapay Zeka Kullanmak
Her bir yapısal varyantın hücre içindeki DNA katlanmasını nasıl değiştirdiğini doğrudan ölçmek, yüzbinlerce lokasyon için zahmetli deneyler gerektirir—bu ölçekte pratikte imkânsızdır. Bunun yerine yazarlar, SuPreMo-Akita boru hattı aracılığıyla erişilen Akita adlı konvolüsyonel sinir ağını kullanarak bir milyon baz çiftlik DNA parçasının 3B’de nasıl katlandığını tahmin etti. Her yapısal varyant için değişiklikli ve değişikliksiz yerel DNA dizisini simüle ettiler, modelden temas haritalarını—genomun hangi parçalarının birbirine dokunduğunu gösteren desenleri—tahmin etmesini istediler ve sonra bu haritaları karşılaştırdılar. Fark ne kadar büyükse, o varyantın genom organizasyonunu o kadar çok bozacağı öngörüldü. Bu, tümörler arasındaki varyantları normal katlanma desenlerini ne kadar kırıp bükmeleri beklendiğine göre sıralamalarına olanak verdi.
Katlanmanın Bozulduğu Sıcak Noktalar
Ekip, şiddetli bozucu varyantlarla tekrar tekrar hedef alınan genomic bölgeleri taradığında beş tekrar eden şekilde bozulmuş bölge ortaya çıkardı—çeşitli tümör tiplerinde birçok çocuğun tümöründe yerel katlanmada güçlü tahmini hasar görülen DNA dizileri. Bu bölgelerin birkaçında model, gen gruplarını ve onların anahtarlarını normalde ayıran alan sınırları ve döngüler gibi önemli yapısal özelliklerin kaybını işaret etti. Çarpıcı şekilde, bazı sıcak noktalar genel olarak özellikle yüksek mutasyon yoğunluğuna sahip değildi; onları ayıran nokta, o bölgelerde varyant oluştuğunda katlanmanın ne kadar şiddetle bozulduğuydu. Bu bölgeler beyin gelişimi ve bilinen kanserle ilişkili fonksiyonlarda rol alan genleri içeriyordu; bu da basit mutasyon sayısından ziyade ince 3B yanlış bağlanmanın daha önemli olabileceğini düşündürüyor.
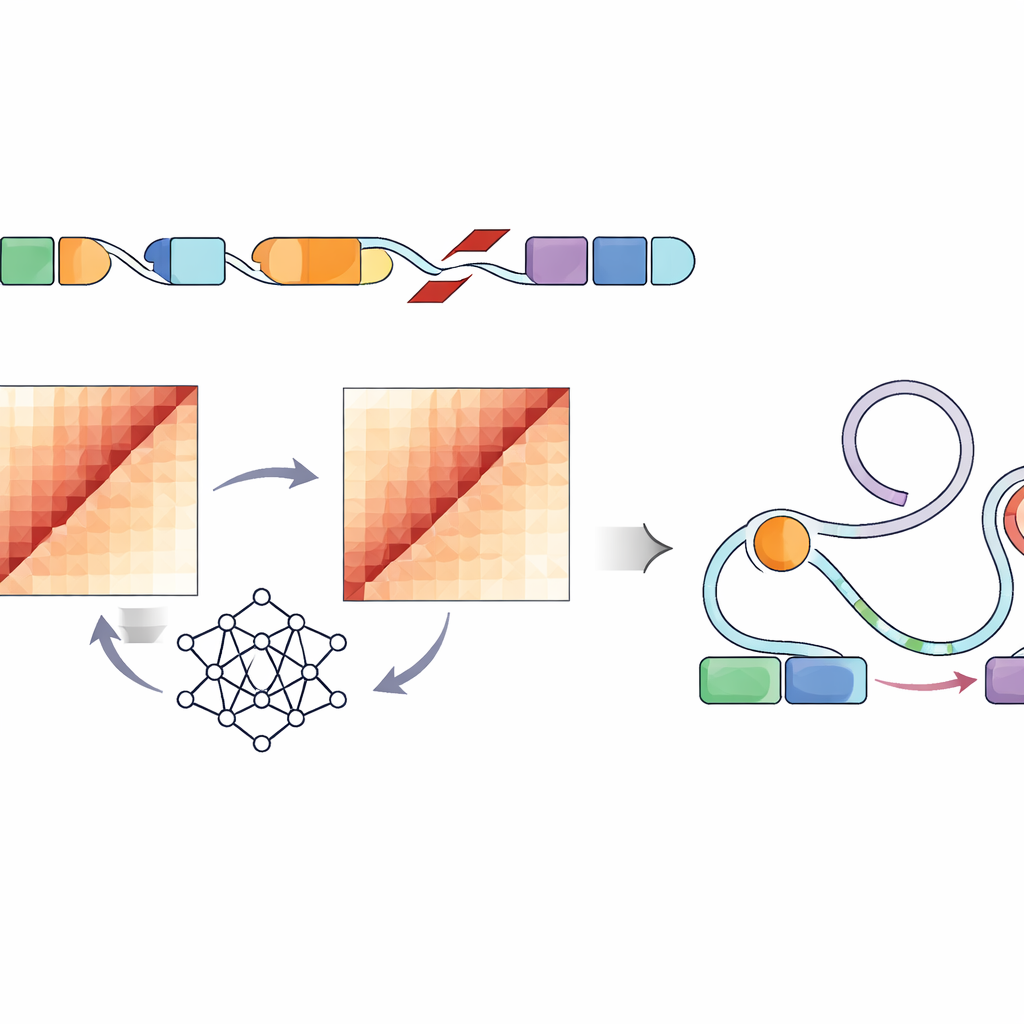
Katlanma Bozulmalarını Gen Kontrol Anahtarlarına Bağlamak
DNA biçimindeki her değişiklik hücre davranışını etkilemeyeceğinden araştırmacılar bir sonraki adımda düzenleyici elemanlara—tümör benzeri hücre hatlarında karakteristik kimyasal işaretlerle ve açık kromatinle işaretlenen enhancer’lara—özellikle baktılar. Birkaç çocuk tümör tipinde son derece bozucu varyantların bu aktif enhancer bölgelerinin içinde veya yakınında yer alma olasılığının daha yüksek olduğunu buldular. Activity-by-Contact (ABC) modeline dayanan mevcut bir çerçeveyi genişleterek, bu enhancer’ların bulunduğu yerlerde genom katlanmasını bozması öngörülen varyantlara ağırlık veren bir “ABC bozulma skoru” oluşturdular. Bu rafine edilmiş skor, enhancer’lar ile hücre büyümesi, hayatta kalma ve beyin fonksiyonlarında rol oynayan yakın genler arasındaki tahmini temasları güçlü biçimde değiştiren yapısal varyantları ön plana çıkardı; bunlar arasında PDGFRA, ID2, MYCN ve diğer tanınmış kanser genleri yer aldı.
Yeni Kanser Sürücüleri ve Gelecekteki Bakım İçin İpuçları
Atipik teratoid/rabdoid tümör adı verilen özellikle agresif bir tümör tipine odaklandıklarında bu yöntem; kromatin yeniden düzenlemesi, DNA onarımı ve sinir gelişiminde rol alan genlerin yakınındaki yeniden düzenlenmeleri öne çıkardı. Birkaç vakada bu varyantları taşıyan tümörler, yakın genlerde olağandışı yüksek veya düşük ifade düzeyleri gösterdi; bu da 3B temasların değişmesi yoluyla enhancer “kaçırma”yla tutarlı. Bu bulguların deneysel doğrulamaya ihtiyacı olsa da, devasa sayıda yapısal varyantı eleyip tümör davranışını etkileme olasılığı en yüksek olanları önceliklendirmek için güçlü yeni bir yol gösteriyorlar. Uzun vadede, genomun katlanma manzarasını makine öğrenimiyle haritalandırmak, genç kanser hastalarından elde edilen dizileme sonuçlarını yorumlamada doktorlara yardımcı olabilir, hastalığın gizli sürücülerini açığa çıkarabilir ve nihayetinde daha kesin, daha az toksik tedavilerin araştırılmasını yönlendirebilir.
Atıf: Gjoni, K., Zhang, S., Yan, R.E. et al. Machine learning-predicted chromatin organization landscape across pediatric tumors. Sci Rep 16, 10790 (2026). https://doi.org/10.1038/s41598-026-44925-3
Anahtar kelimeler: çocuk beyin tümörleri, yapısal varyantlar, 3B genom organizasyonu, makine öğrenimi genomik, enhancer kaçırma