Clear Sky Science · pt
Panorama da organização da cromatina previsto por aprendizado de máquina em tumores pediátricos
Por que o dobramento do genoma importa para crianças doentes
Os tumores cerebrais pediátricos estão entre os cânceres infantis mais letais, mas para muitos pacientes jovens os médicos ainda não sabem exatamente o que deu errado no DNA. Este estudo explora um ângulo novo: não apenas quais genes estão mutados, mas como grandes rearranjos de DNA alteram a maneira como o genoma se dobra dentro de cada célula. Ao combinar grandes conjuntos de dados sobre câncer com um poderoso modelo de aprendizado de máquina, os autores mostram que perturbações ocultas nesse padrão de dobramento 3D podem contribuir para impulsionar tumores infantis — e que computadores já podem sinalizar as mudanças mais perigosas para estudo posterior.
Grandes embaralhamentos de DNA em tumores infantis
Em vez de focar em pequenos erros de digitação no código genético, os pesquisadores examinaram variantes estruturais — grandes cortes, duplicações, inversões e colagens de longos trechos de DNA. Essas mudanças em grande escala podem fundir genes, deletar regiões protetoras ou colocar interruptores potentes (potenciadores) ao lado de genes errados. Usando dados de quase 1.900 crianças da Children’s Brain Tumor Network, abrangendo 61 tipos tumorais, a equipe catalogou quase 300.000 dessas variantes. Eles descobriram que alguns grupos de tumores, como linfomas e sarcomas, apresentavam muito mais dessas alterações do que outros, e que tumores recorrentes ou progressivos após o tratamento inicial normalmente continham mais variantes estruturais do que os tumores originais.
Usando IA para ver o genoma em 3D
Medir diretamente como cada variante estrutural altera o dobramento do DNA dentro de uma célula exigiria experimentos trabalhosos para centenas de milhares de sítios — essencialmente impossível nessa escala. Em vez disso, os autores usaram uma rede neural convolucional chamada Akita, acessada por meio de seu pipeline SuPreMo-Akita, para prever como um trecho de DNA de um milhão de pares de bases se dobra em 3D. Para cada variante estrutural, eles simularam a sequência local de DNA com e sem a alteração, pediram ao modelo que previsse mapas de contato — padrões que mostram quais partes do genoma se tocam — e então compararam esses mapas. Quanto maior a diferença, mais aquela variante foi prevista como perturbadora da organização genômica. Isso permitiu ranquear variantes em todos os tumores segundo o quanto se esperava que deformassem ou quebrassem os padrões normais de dobramento.
Pontos quentes onde o dobramento dá errado
Quando a equipe vasculhou o genoma em busca de locais repetidamente atingidos por variantes altamente disruptivas, descobriram cinco regiões recorrentemente perturbadas — trechos de DNA onde tumores de muitas crianças, de vários tipos, mostraram forte dano previsto ao dobramento local. Em várias dessas regiões, o modelo indicou perda de características estruturais-chave, como limites de domínios e laços que normalmente separam grupos de genes e seus interruptores. De forma marcante, alguns desses pontos quentes não eram particularmente mutados em termos de número total de alterações; o que os distinguia era a gravidade da perturbação do dobramento quando variantes ocorriam ali. Essas regiões continham genes envolvidos no desenvolvimento cerebral e funções relacionadas ao câncer, sugerindo que um mau cabeamento 3D sutil, em vez da simples contagem de mutações, pode ser o que mais importa.
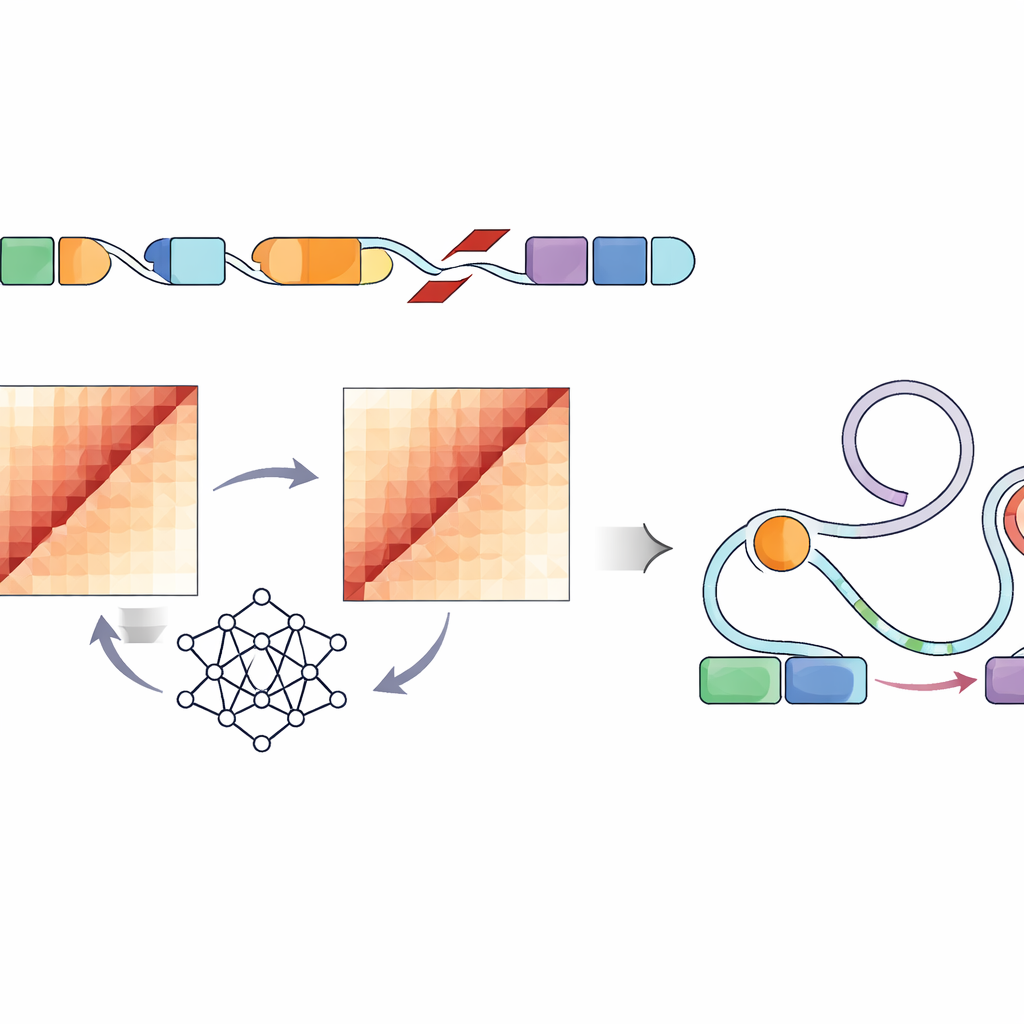
Ligando perturbações do dobramento a interruptores de controle gênico
Porque nem toda mudança na forma do DNA afetará o comportamento celular, os pesquisadores passaram a olhar especificamente para elementos regulatórios — potenciadores marcados por etiquetas químicas características e cromatina aberta em linhas celulares com características tumorais. Eles descobriram que variantes altamente disruptivas em vários tipos tumorais pediátricos tinham maior probabilidade de se localizar dentro ou perto dessas regiões de potenciadores ativas. Baseando-se em um quadro existente chamado modelo Activity-by-Contact, criaram uma “pontuação de ruptura ABC” que prioriza variantes previstas a perturbar o dobramento do genoma especificamente onde esses potenciadores residem. Essa pontuação refinada destacou variantes estruturais que alteravam fortemente os contatos previstos entre potenciadores e genes próximos com papéis em crescimento celular, sobrevivência e função cerebral, incluindo genes de câncer bem conhecidos como PDGFRA, ID2, MYCN e outros.
Pistas para novos motores do câncer e cuidados futuros
Focando em um tipo tumoral particularmente agressivo chamado tumor teratoide/rabdoide atípico, o método ressaltou rearranjos próximos a genes envolvidos em remodelamento da cromatina, reparo de DNA e desenvolvimento neural. Em vários casos, os tumores que carregavam essas variantes também exibiram expressão incomumente alta ou baixa dos genes próximos, consistente com “sequestro” de potenciadores por meio de contatos 3D alterados. Embora essas descobertas ainda precisem de confirmação experimental, elas apontam para uma nova e potente maneira de vasculhar vastos números de variantes estruturais e priorizar aquelas mais propensas a influenciar o comportamento tumoral. A longo prazo, mapas do panorama de dobramento do genoma guiados por aprendizado de máquina poderiam ajudar médicos a interpretar resultados de sequenciamento de pacientes jovens com câncer, descobrir motores ocultos da doença e, em última instância, orientar a busca por tratamentos mais precisos e menos tóxicos.
Citação: Gjoni, K., Zhang, S., Yan, R.E. et al. Machine learning-predicted chromatin organization landscape across pediatric tumors. Sci Rep 16, 10790 (2026). https://doi.org/10.1038/s41598-026-44925-3
Palavras-chave: tumores cerebrais pediátricos, variantes estruturais, organização 3D do genoma, genômica por aprendizado de máquina, sequestro de potenciadores