Clear Sky Science · ja
小児腫瘍における機械学習で予測したクロマチン構造のランドスケープ
ゲノムの折りたたみが病気の子どもにとって重要な理由
小児脳腫瘍は小児期のがんのなかでも致命率が高い一方で、多くの若い患者に対して医師はDNAで何が正確に誤ったのかをまだ解明できていません。本研究は新たな視点を提示します:どの遺伝子に変異があるかだけでなく、大規模なDNA再配列が細胞内でゲノムがどのように折りたたまれるかをどう変えるか、という点です。大規模ながんデータセットと強力な機械学習モデルを組み合わせることで、著者らはこの3次元の折りたたみパターンに隠れた攪乱が小児腫瘍を駆動する一因になり得ること、そしてコンピュータがさらなる検討が必要な最も危険な変化を特定できることを示しています。
小児腫瘍における大規模なDNA再配列
遺伝子コードの小さな誤字に注目する代わりに、研究者らは構造変異—長いDNA領域の大きな切断、複製、反転、貼り付け—を調べました。これらの大規模な変化は遺伝子を融合させたり、防御的な領域を欠失させたり、強力なスイッチ(エンハンサー)を誤った遺伝子の近くに配置したりします。Children’s Brain Tumor Network のほぼ1,900人、61の腫瘍タイプにわたるデータを用いて、チームは約30万件に及ぶこうした変異をカタログ化しました。一部の腫瘍群(例えばリンパ腫や肉腫)は他よりもこれらの変化をずっと多く抱えており、初回治療後に再発または進行した腫瘍は通常、元の腫瘍よりも多くの構造変異を有していることが分かりました。
AIを使ってゲノムを3次元で見る
各構造変異が細胞内でのDNAの折りたたみをどのように変えるかを直接測定するには、数十万箇所にわたる労力のかかる実験が必要で、規模的に事実上不可能です。そこで著者らは、SuPreMo-Akitaパイプラインを通じて利用した畳み込みニューラルネットワークAkitaを使い、100万塩基対の領域が3次元でどのように折りたたまれるかを予測しました。各構造変異について、変化のある場合とない場合の局所的なDNA配列をシミュレートし、モデルにコンタクトマップ—ゲノムのどの部分が接触するかを示すパターン—を予測させ、それらを比較しました。差が大きいほど、その変異がゲノム組織を撹乱すると予測されます。これにより全腫瘍の変異を、正常な折りたたみパターンをどれだけ曲げたり壊したりするかの強さでランク付けできました。
折りたたみが狂うホットスポット
チームが強く撹乱をもたらす変異が繰り返し集中する領域をゲノム上で走査したところ、5つの再発性に撹乱された領域が見つかりました—多様なタイプの多くの小児腫瘍で局所的な折りたたみに強い予測損傷が示されたDNAの伸びです。これらのいくつかの領域では、モデルは遺伝子群とそれらのスイッチを通常は分離しているドメイン境界やループなどの重要な構造的特徴の喪失を示しました。注目すべきは、これらのホットスポットの一部は全体として特に高い変異頻度を示していたわけではなく、変異が起こった際の折りたたみ撹乱の深刻さが際立っていた点です。これらの領域には脳発生や既知のがん関連機能に関与する遺伝子が含まれており、単純な変異数よりも微妙な3次元の配線ミスがより重要である可能性を示唆しています。
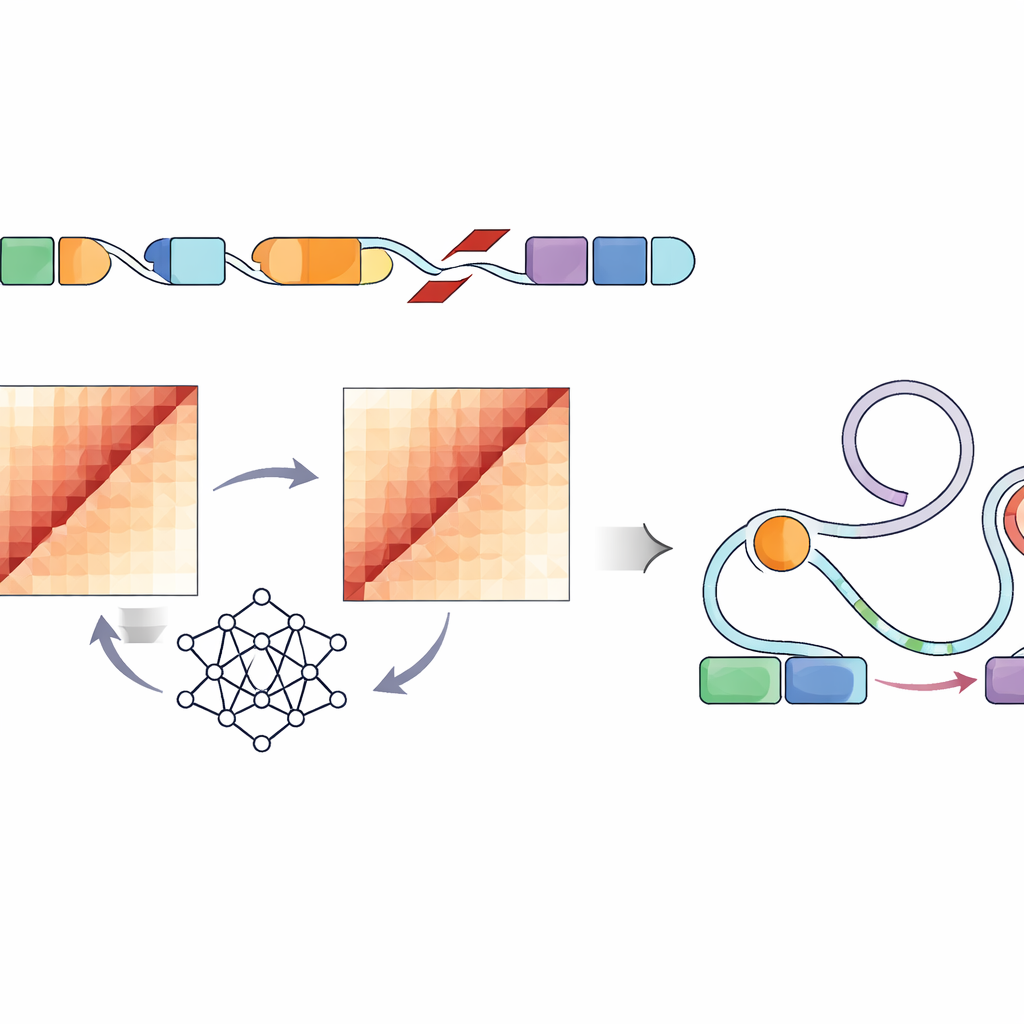
折りたたみ撹乱と遺伝子制御スイッチの結びつき
すべてのDNA形状の変化が細胞の挙動に影響するわけではないため、研究者らは次に制御エレメント—腫瘍様細胞株で特徴的な化学的標識や開いたクロマチンで示されるエンハンサー—に特に注目しました。彼らは、いくつかの小児腫瘍タイプにおいて高度に撹乱を引き起こす変異が、これらの活性化されたエンハンサー領域の内部や近傍にある傾向が強いことを見出しました。既存のActivity-by-Contactモデルに基づき、「ABC破壊スコア」を作成し、これらのエンハンサーが存在する場所でゲノム折りたたみを妨げると予測される変異のスコアを引き上げました。この精緻化されたスコアリングにより、エンハンサーと近傍遺伝子間の予測される接触を強く変える構造変異が浮き彫りになり、それらの遺伝子は細胞増殖、生存、脳機能に関与し、PDGFRA、ID2、MYCNなどの既知のがん遺伝子を含みます。
新たながんドライバーの手がかりと将来の診療
特に悪性度の高い腫瘍タイプである非典型的奇形腫様/横紋筋腫様腫瘍(atypical teratoid/rhabdoid tumor)に着目すると、この手法はクロマチン再構築、DNA修復、神経発生に関与する遺伝子近傍の再配列を強調しました。いくつかの例では、これらの変異を有する腫瘍で近傍遺伝子の発現が異常に高いまたは低いことが観察され、3次元接触の変化によるエンハンサーの「乗っ取り」と一致しました。これらの所見は実験的な検証を要しますが、膨大な数の構造変異をふるいにかけ、腫瘍挙動に影響を与える可能性が高いものを優先する強力な新しい方法を指し示しています。長期的には、機械学習に導かれたゲノムの折りたたみランドスケープマップが、若年がん患者のシーケンス結果の解釈、病気の隠れたドライバーの発見、そして最終的にはより精密で毒性の少ない治療法の探索に役立つ可能性があります。
引用: Gjoni, K., Zhang, S., Yan, R.E. et al. Machine learning-predicted chromatin organization landscape across pediatric tumors. Sci Rep 16, 10790 (2026). https://doi.org/10.1038/s41598-026-44925-3
キーワード: 小児脳腫瘍, 構造変異, 3次元ゲノム構造, 機械学習ゲノミクス, エンハンサー乗っ取り