Clear Sky Science · ru
Пейзаж организации хроматина в педиатрических опухолях, предсказанный методом машинного обучения
Почему сворачивание генома важно для больных детей
Педиатрические опухоли головного мозга входят в число самых смертоносных детских раков, но во многих случаях врачам по-прежнему неясно, что именно пошло не так в ДНК у молодых пациентов. В этом исследовании рассмотрен новый подход: не только какие гены мутировали, но и как крупные перестройки ДНК меняют то, как геном сворачивается внутри клетки. Комбинируя большие онкологические наборы данных с мощной моделью машинного обучения, авторы показывают, что скрытые нарушения в этой 3D-структуре могут способствовать развитию детских опухолей — и что компьютеры теперь могут выделять наиболее опасные изменения для дальнейшего изучения.
Крупные перестановки ДНК в детских опухолях
Вместо того чтобы сосредотачиваться на мелких опечатках в генетическом коде, исследователи изучали структурные варианты — крупные разрезы, копирования, инверсии и вставки длинных участков ДНК. Эти изменения в крупном масштабе могут сращивать гены, удалять защитные участки или помещать мощные переключатели (энхансеры) рядом с неправильными генами. Используя данные почти 1 900 детей из Сети по изучению детских опухолей головного мозга, охватывающие 61 тип опухолей, команда каталогизировала почти 300 000 таких вариантов. Они обнаружили, что в некоторых группах опухолей, таких как лимфомы и саркомы, таких изменений оказалось существенно больше, а рецидивные или прогрессирующие после первичного лечения опухоли, как правило, содержали больше структурных вариантов, чем исходные образцы.
Использование ИИ для визуализации генома в 3D
Прямое измерение того, как каждый структурный вариант меняет сворачивание ДНК в клетке, потребовало бы трудоёмких экспериментов для сотен тысяч участков — практически невозможно в таком масштабе. Вместо этого авторы использовали сверточную нейронную сеть Akita, доступную через их конвейер SuPreMo-Akita, чтобы предсказывать, как участок ДНК длиной в миллион пар оснований сворачивается в 3D. Для каждого структурного варианта они смоделировали локальную последовательность ДНК с изменением и без него, попросили модель предсказать карты контактов — схемы, показывающие, какие части генома соприкасаются — и затем сравнили эти карты. Чем больше различие, тем сильнее вариант, по прогнозу, нарушал организацию генома. Это позволило ранжировать варианты по всем опухолям по степени ожидаемого нарушения нормальных паттернов сворачивания.
Горячие точки, где сворачивание даёт сбой
При сканировании генома на предмет участков, многократно поражённых сильно нарушающими вариантами, команда обнаружила пять рекуррентно повреждённых регионов — участков ДНК, где у многих детей с разными типами опухолей предсказано серьёзное нарушение локального сворачивания. В нескольких из этих регионов модель указала на потерю ключевых структурных особенностей, таких как границы доменов и петли, которые обычно разделяют группы генов и их переключатели. Поразительно, что некоторые из этих горячих точек не отличались высокой общей частотой мутаций; их выделяла именно серьёзность нарушения сворачивания, когда варианты там возникали. В этих регионах находились гены, связанные с развитием мозга и известными онкологическими функциями, что указывает на то, что тонкая 3D-дезорганизация, а не просто число мутаций, может иметь решающее значение.
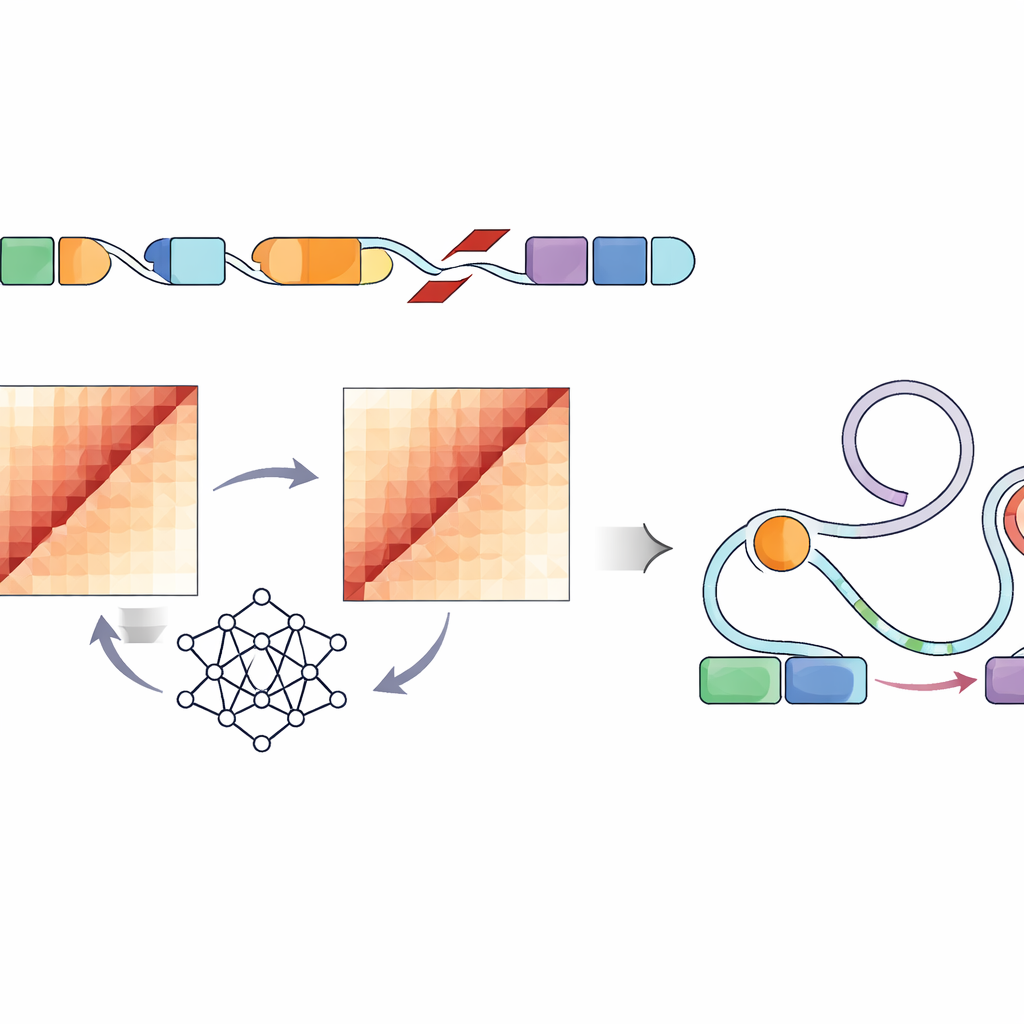
Связывание нарушений сворачивания с регуляторными переключателями генов
Поскольку не каждое изменение формы ДНК повлияет на поведение клетки, исследователи далее специально изучили регуляторные элементы — энхансеры, помеченные характерными химическими метками и участками открытой хроматина в клеточных линиях, напоминающих опухолевые. Они обнаружили, что сильно нарушающие варианты в нескольких типах педиатрических опухолей чаще локализуются в этих активных регионах энхансеров или рядом с ними. Развивая существующую модель Activity-by-Contact, авторы создали «ABC-оценку дисфункции», которая усиливает значимость вариантов, предсказано нарушающих сворачивание именно там, где находятся эти энхансеры. Это уточнённое ранжирование выявило структурные варианты, резко меняющие предсказанные контакты между энхансерами и ближайшими генами, вовлечёнными в рост клеток, выживание и функции мозга, включая хорошо известных онкогенов, таких как PDGFRA, ID2, MYCN и другие.
Подсказки к новым онкологическим драйверам и будущему лечению
Сфокусировавшись на особенно агрессивном типе опухоли — атипичном тератоидном/рабдоидном новообразовании, метод выделил перестройки рядом с генами, участвующими в ремоделировании хроматина, репарации ДНК и развитии нейронов. В нескольких случаях опухоли с такими вариантами также демонстрировали необычно повышенную или пониженную экспрессию соседних генов, что согласуется с «перехватом» энхансера через изменённые 3D-контакты. Несмотря на то, что эти выводы требуют экспериментального подтверждения, они указывают на мощный новый способ просеивать огромное число структурных вариантов и приоритизировать те, которые наиболее вероятно влияют на поведение опухоли. В перспективе такие карты ландшафта сворачивания генома, направляемые машинным обучением, могут помочь врачам интерпретировать результаты секвенирования у молодых пациентов с раком, выявлять скрытые драйверы болезни и в конечном счёте направлять поиск более точных и менее токсичных методов лечения.
Цитирование: Gjoni, K., Zhang, S., Yan, R.E. et al. Machine learning-predicted chromatin organization landscape across pediatric tumors. Sci Rep 16, 10790 (2026). https://doi.org/10.1038/s41598-026-44925-3
Ключевые слова: педиатрические опухоли головного мозга, структурные варианты, 3D-организация генома, геномика с машинным обучением, перехват энхансера