Clear Sky Science · sv
Maskininlärningspredikterat kromatinorganisationslandskap över pediatriska tumörer
Varför genomets veckning spelar roll för sjuka barn
Pediatriska hjärntumörer hör till de mest dödliga barncancerformerna, men för många unga patienter vet läkare fortfarande inte exakt vad som gick fel i deras DNA. Den här studien undersöker en ny vinkel: inte bara vilka gener som är muterade, utan hur stora DNA-omläggningar förändrar sättet genomet viks inuti varje cell. Genom att kombinera stora cancer-dataset med en kraftfull maskininlärningsmodell visar författarna att dolda störningar i detta 3D-veckmönster kan bidra till barndomstumörer — och att datorer nu kan flagga de mest farliga förändringarna för vidare studie.
Stora DNA-ombildningar i barndomstumörer
I stället för att fokusera på små fel i den genetiska koden undersökte forskarna strukturella varianter — stora snitt, kopior, vändningar och inklistringar av långa DNA-sträckor. Dessa storskaliga förändringar kan föra samman gener, ta bort skyddande regioner eller placera kraftfulla strömbrytare (enhancers) intill fel gen. Med data från nästan 1 900 barn i Children’s Brain Tumor Network, som spände över 61 tumörtyper, katalogiserade teamet nästan 300 000 sådana varianter. De fann att vissa tumörgrupper, som lymfom och sarkom, bar på betydligt fler av dessa förändringar än andra, och att tumörer som återkommit eller progredierat efter initial behandling vanligtvis hade fler strukturella varianter än de ursprungliga tumörerna.
Använda AI för att se genomet i 3D
Att direkt mäta hur varje strukturell variant förändrar DNA:s veckning i en cell skulle kräva arbetsintensiva experiment för hundratusentals platser — praktiskt taget omöjligt i denna skala. I stället använde författarna ett konvolutionellt neuralt nätverk kallat Akita, åtkomligt via deras SuPreMo-Akita-pipeline, för att förutsäga hur en miljon baspar lång DNA-sträcka viks i 3D. För varje strukturell variant simulerade de den lokala DNA-sekvensen med och utan förändringen, bad modellen att förutsäga kontaktkartor — mönster som visar vilka delar av genomet som rör vid varandra — och jämförde sedan dessa kartor. Ju större skillnad, desto mer förväntades varianten störa genomorganisationen. Detta gjorde att de kunde rangordna varianterna över alla tumörer efter hur starkt de förväntades böja eller bryta upp normala veckmönster.
Hotspots där veckningen går fel
När teamet sökte över genomet efter platser som upprepade gånger drabbades av mycket störande varianter upptäckte de fem återkommande störda regioner — DNA-sträckor där många barns tumörer, av olika typer, visade starkt förväntad skada på lokal veckning. I flera av dessa regioner indikerade modellen förlust av viktiga strukturella funktioner såsom domängränser och slingor som normalt separerar grupper av gener och deras regulatorer. Slående nog var vissa av dessa hotspots inte särskilt mycket muterade i stort; det som utmärkte dem var allvaret i veckningsstörningen när varianter väl förekom där. Dessa regioner innehöll gener involverade i hjärnans utveckling och kända cancerfunktioner, vilket tyder på att subtilt 3D-felkoppling snarare än enkla mutationsantal kan vara det som spelar störst roll.
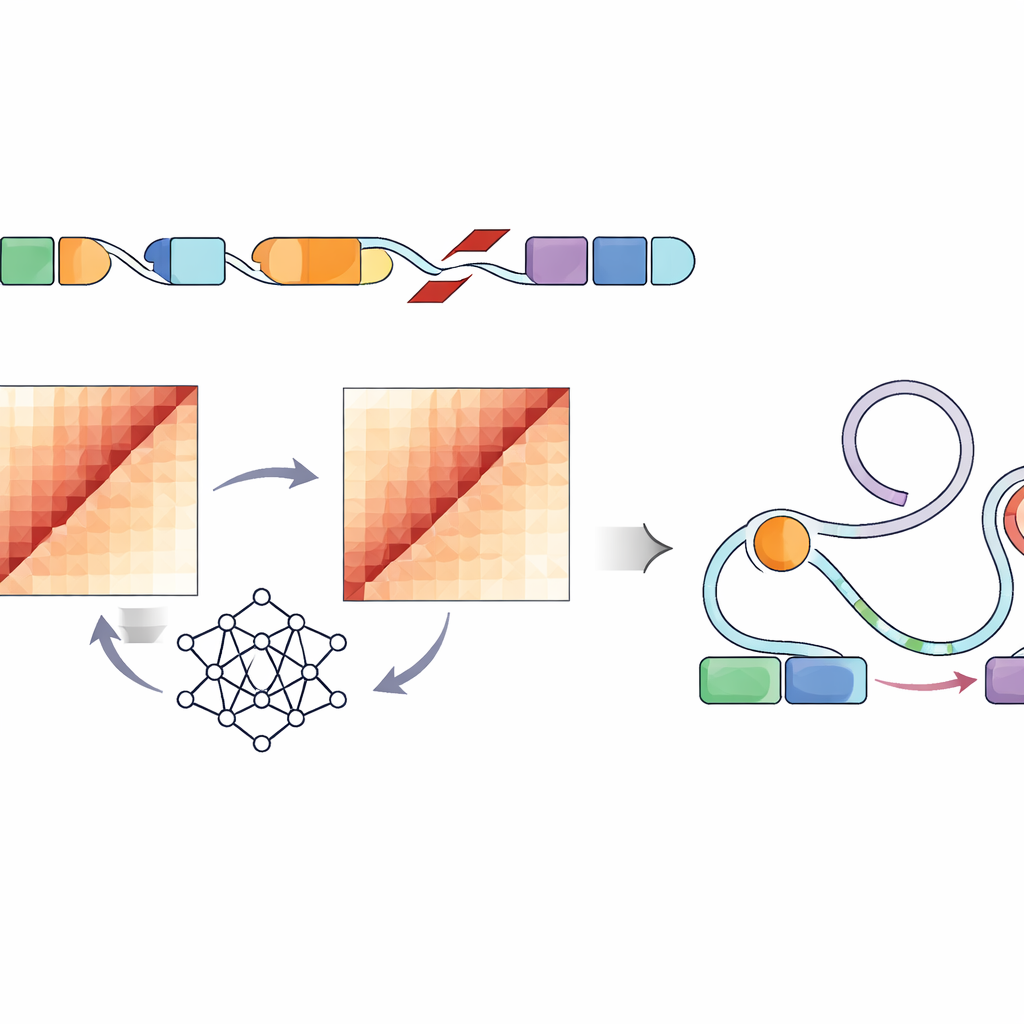
Koppla veckningsstörningar till genreglerande brytare
Eftersom inte varje förändring i DNA-form påverkar cellernas beteende undersökte forskarna därefter specifikt regulatoriska element — enhancers markerade av karakteristiska kemiska taggar och öppet kromatin i tumörlika cellinjer. De fann att mycket störande varianter i flera pediatriska tumörtyper oftare låg i eller nära dessa aktiva enhancer-regioner. Byggt på en befintlig ram kallad Activity-by-Contact-modellen skapade de en «ABC-disruptionspoäng» som gynnar varianter förväntade att störa genomveckningen just där dessa enhancers finns. Denna förfinade poängsättning lyfte fram strukturella varianter som starkt förändrade förväntade kontakter mellan enhancers och närliggande gener med roller i celltillväxt, överlevnad och hjärnfunktion, inklusive välkända cancerrelaterade gener såsom PDGFRA, ID2, MYCN och andra.
Ledtrådar till nya cancerrutiner och framtida vård
Med fokus på en särskilt aggressiv tumörtyp kallad atypiskt teratoid/rhabdoid-tumör belyste metoden omarrangemang nära gener involverade i kromatinremodellering, DNA-reparation och neural utveckling. I flera fall visade tumörer som bar dessa varianter också ovanligt hög eller låg uttrycksnivå av de närliggande generna, förenligt med enhancer-»kapning» genom förändrade 3D-kontakter. Även om dessa fynd fortfarande behöver experimentell bekräftelse, pekar de på ett kraftfullt nytt sätt att sålla bland stora mängder strukturella varianter och prioritera dem som mest sannolikt påverkar tumörbeteende. På lång sikt skulle sådana maskininlärningsstyrda kartor över genomet veckningslandskap kunna hjälpa läkare tolka sekvenseringsresultat från unga cancerpatienter, upptäcka dolda drivkrafter bakom sjukdom och i slutändan vägleda sökandet efter mer precisa, mindre toxiska behandlingar.
Citering: Gjoni, K., Zhang, S., Yan, R.E. et al. Machine learning-predicted chromatin organization landscape across pediatric tumors. Sci Rep 16, 10790 (2026). https://doi.org/10.1038/s41598-026-44925-3
Nyckelord: pediatriska hjärntumörer, strukturella varianter, 3D-genomorganisation, maskininlärning genomik, enhancerkapning