Clear Sky Science · tr
Aromatik ve N-heteroaromatik türevlenmemiş tiosemikarbazonların çok yönlü biyolojik ve hesaplamalı değerlendirmesi
Neden bu küçük moleküller önemli
Kanser ve paraziter enfeksiyonlar dünyadaki en inatçı sağlık sorunlarından ikisi olmaya devam ediyor; mevcut birçok ilaç ya yeterince etkili değil ya da güçlü yan etkilere yol açıyor. Bu çalışma, tiosemikarbazon adı verilen, nispeten basit ve kolay üretilen bir molekül ailesini inceleyerek bazı üyelerinin sağlıklı insan hücrelerini korurken kanser hücrelerine ve hastalık yapıcı parazitlere seçici zarar verip veremeyeceğini araştırıyor. Ayrıca bu moleküllerin vücutta nasıl davrandığını ve kan proteinleriyle nasıl etkileştiklerini hem laboratuvar deneyleri hem de bilgisayar simülasyonlarıyla inceliyor.
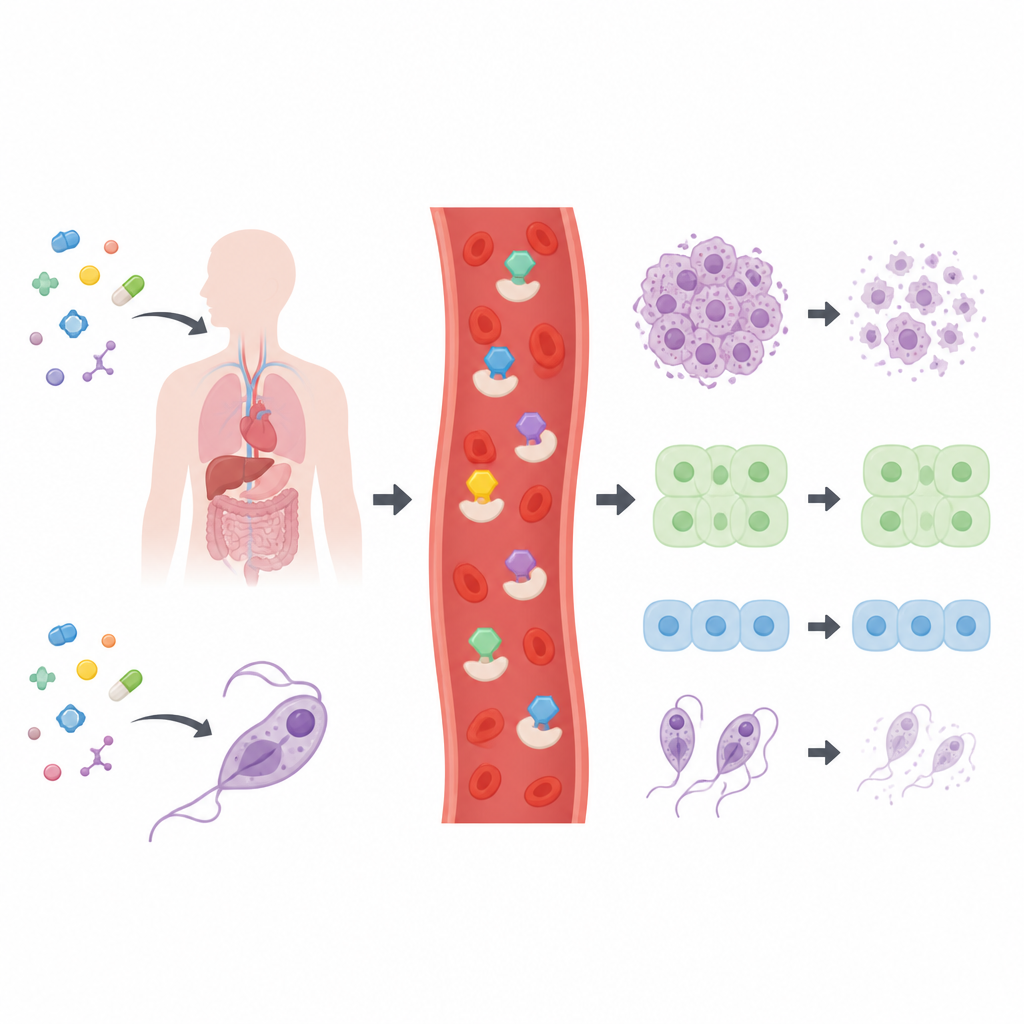
Teste sokulan bir aday kütüphanesi
Araştırmacılar, çoğu birçok ilaçta bilinen halka biçimli karbon çerçeveleri etrafında inşa edilmiş 28 ilişkili tiosemikarbazon bileşiği seti oluşturdu ve karakterize etti. Hücrelerde test etmeden önce, moleküllerin boyut, polarite ve esneklik gibi özellikleri dikkate alan yaygın “ilaç‑benzeri” kurallara uyup uymadıklarını kontrol ettiler. Bileşiklerin tamamı bu temel filtreleri geçti; bu da ilaç geliştirme için makul başlangıç noktaları olduğunu düşündürüyor. Ekip daha sonra hangi yapıların en aktif olduğunu haritalamak için çok sayıda insan kanser hücre hattını, iki tip normal insan hücresini ve dört hastalık yapıcı paraziti bileşiklere maruz bıraktı.
En umut verici moleküllerin belirlenmesi
Kütüphanenin çoğu yalnızca ılımlı etki gösterdi, ancak altı molekül öne çıktı. Üçü piridin halkası, biri kinolin halkası ve biri indol halkası temelindeydi. Bu önde gelen adaylar düşük konsantrasyonlarda kanser hücrelerini yavaşlattı veya öldürdü ve birkaç durumda Chagas hastalığı, Afrika uyku hastalığı ve leishmanyazise yol açan parazitlere karşı da güçlü etki gösterdi. Açık ara öne çıkan, 26 etiketli bileşik, akciğer, karaciğer, kemik ve rahim ağzı kanseri hücre hatlarına karşı özellikle etkiliyken normal akciğer ve kolon hücrelerine karşı neredeyse hiç toksisite göstermedi. Bu seçicilik kritik önemde; çünkü tümör dokusunun benzer ölçüde sağlıklı dokuya zarar vermeden hedeflenebileceği bir pencereye işaret ediyor.
Öncül bileşiğin kanser hücrelerine nasıl saldırdığı
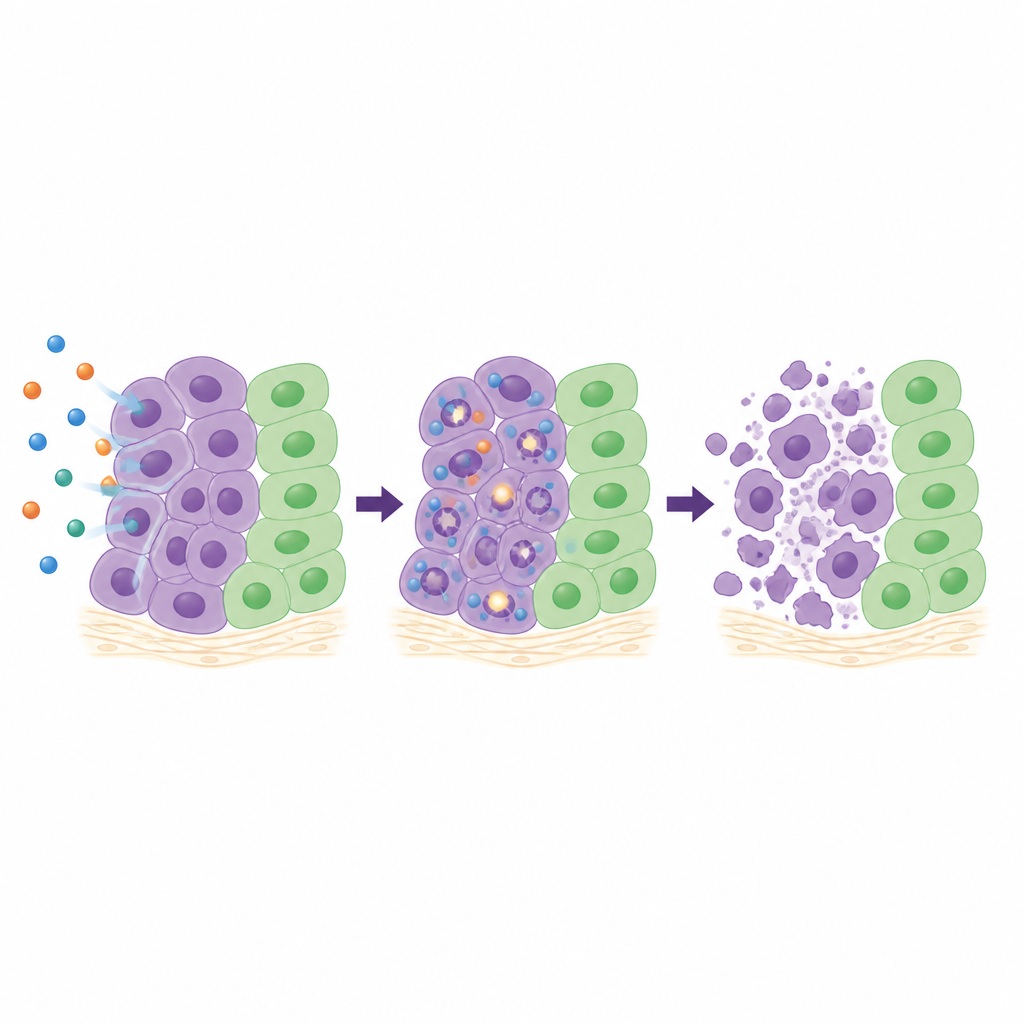
26’nın hücre içindeki etkisini anlamak için ekip, dört duyarlı kanser hattını ayrıntılı olarak inceledi. Hücre döngüsünde ilerlemeyi izlediler, DNA kırılmasının belirteçlerini ölçtüler ve içsel “kendini yok etme” enzimlerinin aktivasyonunu takip ettiler. Hücre tipine bağlı olarak 26, hücrelerin büyüme döngüsünde farklı aşamalarda duraksamasına neden oldu; ancak her durumda zamanla artan DNA hasarı oluşturdu ve programlı hücre ölümünde anahtar rol oynayan kaspaz‑3 ve kaspaz‑7’yi güçlü şekilde aktive etti. Düz hücre katmanlarına göre gerçek tümörleri daha iyi taklit eden üç boyutlu akciğer kanseri hücresi kümeleşmelerinde 26, sferoid büyümesini keskin şekilde azalttı ve daha yüksek dozlarda bunları küçülttü. İnsan tümör parçalarının kendi kan kaynağıyla büyüdüğü bir civciv yumurtası zar modeliyle yapılan çalışmada, 26 ile tedavi tümör alanını yaklaşık üçte iki oranında kesti ve çevre dokuya görünür bir zarar vermedi.
Metal bağlanması ve kan taşınımından ipuçları
Neden bazı tiosemikarbazonlar aktifken diğerleri değil? Kuantum‑kimyasal hesaplamalar kullanılarak yazarlar, en etkili bileşiklerin belirli atomlarda demir veya bakır gibi metal iyonlarını yakalamayı destekleyen elektronik yapılara sahip olduğunu gösterdi. Bu sıkı “şelat” kompleksleri oluşturma yeteneğinin biyolojik aktivitelerinin temelini oluşturduğu düşünülüyor. 27 etiketli bir bileşik öne çıkan bir istisna; yapısı bu tür metal bağlanmasını engellediği için alternatif bir etki mekanizmasını işaret ediyor. Ekip ayrıca altı ana bileşiğin bağırsak benzeri zarları ne kadar kolay geçebileceğini ve kanın başlıca taşıyıcı proteini olan insan serum albüminine ne kadar güçlü bağlandıklarını test etti. Hepsinin pasif bağırsak geçirgenliği oldukça zayıftı; bu da oral uygulama için formülasyon çalışması gerektiğini düşündürüyor. Bununla birlikte 26 bileşiği albüminle güçlü bağlandı ve bilgisayar simülasyonları bilinen bir ilaç bağlama cebinde onu sabitleyen stabil hidrojen bağları ve hidrofobik temaslar seti ortaya koydu.
Gelecekteki ilaçlar için anlamı
Deneyler ve simülasyonlar birlikte değerlendirildiğinde, bu moleküler ailenin bir üyesi olan 26’nın DNA kırılmalarına neden olarak ve kontrollü hücre ölümünü tetikleyerek kanser hücrelerine seçici zarar verebildiği, test edilen normal hücreleri ise büyük ölçüde sağlam bıraktığı görülüyor. Aynı zamanda, ilişkili moleküller birkaç önemli parazite karşı aktivite gösteriyor. Mevcut formları bağırsaktan emilim için ideal olmasa da basit yapıları, açık yapı‑aktivite ilişkileri ve kan proteinleriyle tanımlanmış etkileşimleri, bunları gelecekteki ilaç tasarımı için çekici yapı taşları yapıyor. Daha iyi taşıma sistemleri ve hayvan testleriyle bu tiosemikarbazonlar hem kanser hem de paraziter hastalıklar için yeni tedavilere katkıda bulunabilir.
Atıf: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Anahtar kelimeler: tiosemikarbazonlar, antikanser ajanlar, antiparazitik bileşikler, DNA hasarı, ilaç tasarımı