Clear Sky Science · ru
Многосторонняя биологическая и вычислительная оценка ароматических и N‑гетероароматических незамещённых тиосемикарбазонов
Почему эти малые молекулы важны
Рак и паразитарные инфекции остаются двумя из самых упорных мировых проблем здравоохранения, а многие существующие препараты либо недостаточно эффективны, либо вызывают серьёзные побочные эффекты. В этом исследовании рассматривается семейство относительно простых, легко синтезируемых молекул — тиосемикарбазонов — с целью выяснить, могут ли некоторые из них избирательно повреждать раковые клетки и патогенные паразиты, не затрагивая при этом здоровые клетки человека. Также изучается поведение этих молекул в организме и их взаимодействие с белками крови с помощью лабораторных тестов и компьютерного моделирования.
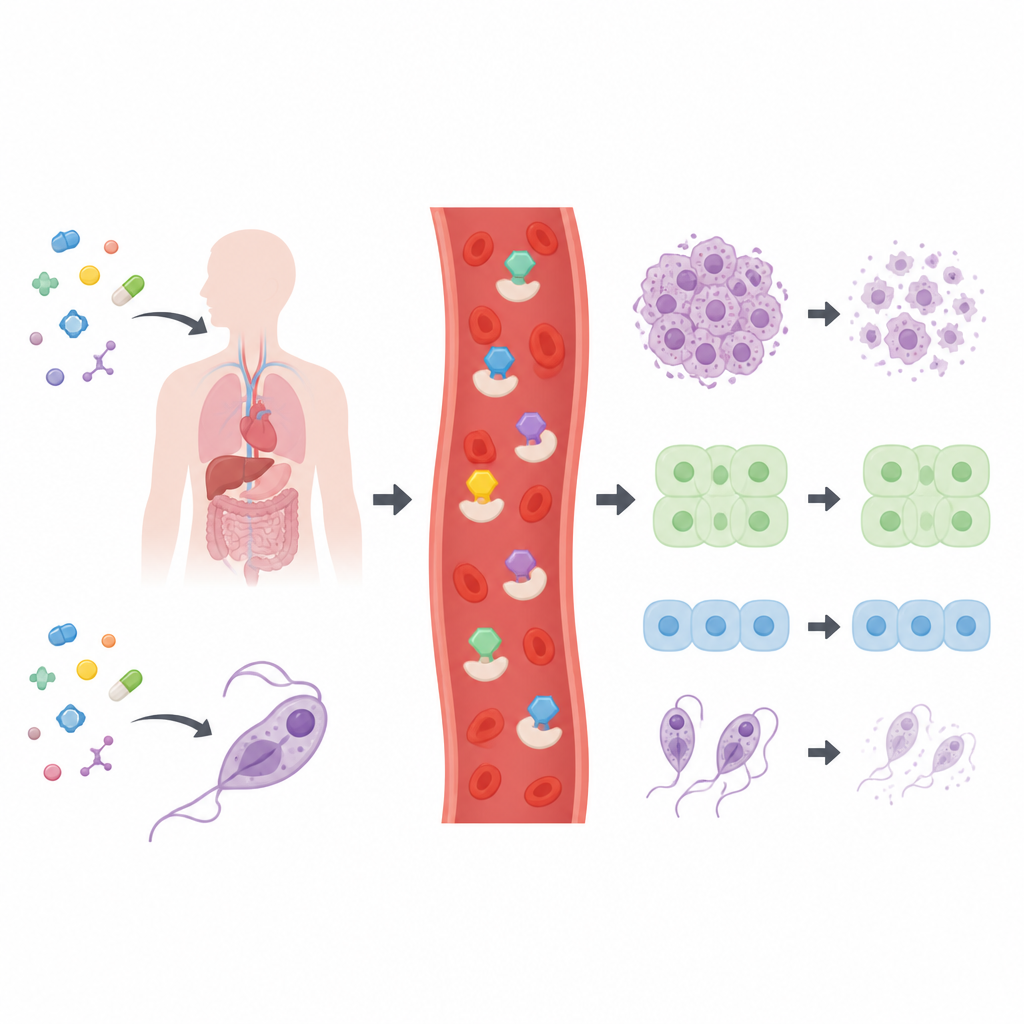
Библиотека кандидатов выходит на испытания
Авторы синтезировали и охарактеризовали набор из 28 родственных соединений тиосемикарбазонов, большинство из которых построено вокруг циклических углеродных скелетов, известных по многим лекарствам. Перед тестированием на клетках они проверили, соответствуют ли молекулы общепринятым правилам «лекарственности», используемым в фармацевтических исследованиях, которые учитывают размеры, полярность и подвижность. Все соединения прошли эти базовые фильтры, что указывает на их пригодность в качестве отправных точек для разработки лекарств. Команда затем подвергла широкий набор человеческих раковых клеточных линий, двум типам нормальных человеческих клеток и четырём патогенным паразитам действию этих соединений, чтобы определить, какие структуры наиболее активны.
Выявление наиболее перспективных молекул
Большинство соединений библиотеки показали лишь умеренную активность, но выделилось шесть молекул. Три основывались на пиридиновом кольце, одна — на хинолиновом, и одна — на индольном. Эти ведущие кандидаты либо замедляли рост, либо убивали раковые клетки при низких концентрациях и в нескольких случаях также проявляли сильную активность против паразитов, вызывающих болезнь Шагаса, африканскую трипаносомоз и лейшманиоз. Очевидный фаворит, помеченный как 26, оказался особенно эффективен против линий рака лёгкого, печени, кости и шейки матки, при этом практически не проявляя токсичности в отношении нормальных клеток лёгкого и толстой кишки. Такая селективность важна, поскольку указывает на окно, в котором опухоль можно атаковать без сопоставимого вреда для здоровой ткани.
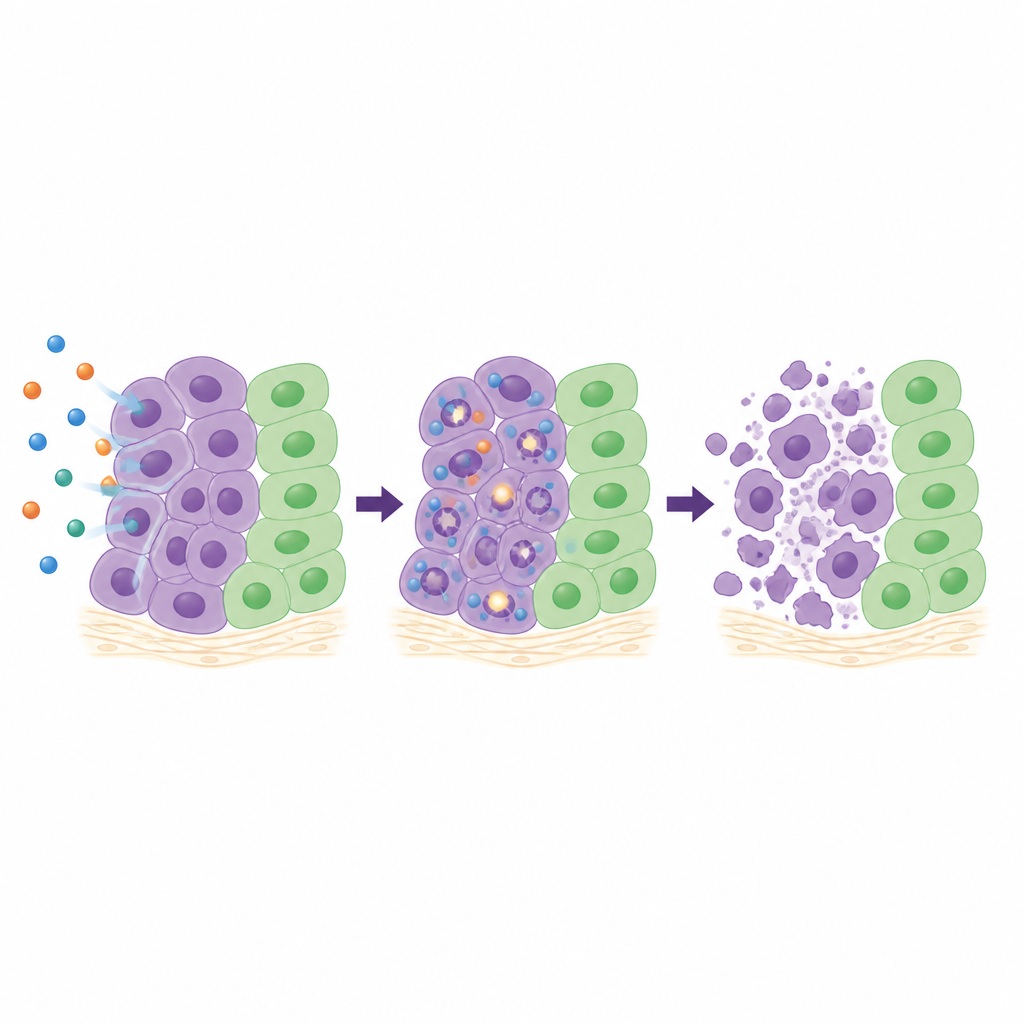
Как лидирующее соединение атакует раковые клетки
Чтобы понять, что делает 26 внутри клеток, команда подробно исследовала четыре чувствительные раковые линии. Они отслеживали прохождение клеток через клеточный цикл, измеряли маркеры разрывов ДНК и фиксировали активацию внутренних «ферментов самоуничтожения». В зависимости от типа клеток 26 тормозил клетки на разных стадиях их роста, но во всех случаях вызывал нарастающее повреждение ДНК с течением времени и сильно активировал каспазы‑3 и ‑7, ключевые участники программируемой гибели клеток. В трёхмерных скоплениях клеток лёгкого, которые лучше воспроизводят поведение настоящих опухолей, чем плоские клеточные монослои, 26 значительно подавлял рост сфероидов и при более высоких дозах сокращал их размер. В модели на перепонке куриного яйца, где человеческие фрагменты опухоли развиваются со своей собственной сосудистой сетью, лечение 26 сократило площадь опухоли примерно на две трети без видимого повреждения окружающих тканей.
Подсказки от связывания металлов и транспорта в крови
Почему одни тиосемикарбазоны активны, а другие нет? С помощью квантово‑химических расчётов авторы показали, что наиболее эффективные соединения имеют электронные структуры, благоприятствующие захвату ионов металлов, таких как железо или медь, в определённых атомных положениях. Способность образовывать прочные «хелатные» комплексы считается ключевым фактором их биологической активности. Один из заметных образцов, соединение 27, ведёт себя иначе, потому что его структура препятствует такому связыванию металлов, что указывает на альтернативный механизм действия. Команда также проверила, насколько легко шесть ключевых соединений могут проходить через мембраны, имитирующие кишечник, и насколько сильно они связываются с человеческим сывороточным альбумином, основным переносчиком в крови. Все они показали довольно низкую пассивную проницаемость через кишечник, что указывает на необходимость работы по формулировкам для перорального применения. Однако соединение 26 сильно связывалось с альбумином, и компьютерные симуляции выявили устойчивый набор водородных связей и гидрофобных контактов, которые помогают закрепить его в известном кармане для связывания лекарств.
Что это значит для будущих лекарств
В сумме эксперименты и моделирования показывают, что один представитель этого семейства молекул, соединение 26, может избирательно повреждать раковые клетки, вызывая разрывы ДНК и инициируя контролируемую гибель клеток, при этом испытываемые нормальные клетки остаются в значительной степени невредимыми. В то же время родственные молекулы демонстрируют активность против нескольких важных паразитов. Хотя их текущая форма не идеальна для всасывания через кишечник, их простая структура, ясные соотношения «структура‑активность» и определённые взаимодействия с белками крови делают их привлекательными строительными блоками для дальнейшей разработки лекарств. При улучшенных системах доставки и испытаниях на животных эти тиосемикарбазоны могли бы внести вклад в создание новых методов лечения как рака, так и паразитарных заболеваний.
Цитирование: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Ключевые слова: тиосемикарбазоны, противораковые агенты, антипаразитарные соединения, повреждение ДНК, дизайн лекарств