Clear Sky Science · de
Vielseitige biologische und rechnerische Bewertung aromatischer und N‑heteroaromatischer nicht‑substituierter Thiosemicarbazonen
Warum diese kleinen Moleküle wichtig sind
Krebs und parasitäre Infektionen zählen weiterhin zu den hartnäckigsten Gesundheitsproblemen weltweit, und viele verfügbare Medikamente wirken nicht ausreichend oder verursachen starke Nebenwirkungen. Diese Studie untersucht eine Familie relativ einfacher, leicht herstellbarer Moleküle, die als Thiosemicarbazone bezeichnet werden, um herauszufinden, ob einige davon Krebszellen und krankheitsverursachende Parasiten selektiv schädigen können, während sie gesunde menschliche Zellen verschonen. Außerdem wird untersucht, wie diese Moleküle sich im Körper verhalten und wie sie mit Blutproteinen interagieren — sowohl durch Labortests als auch durch Computersimulationen.
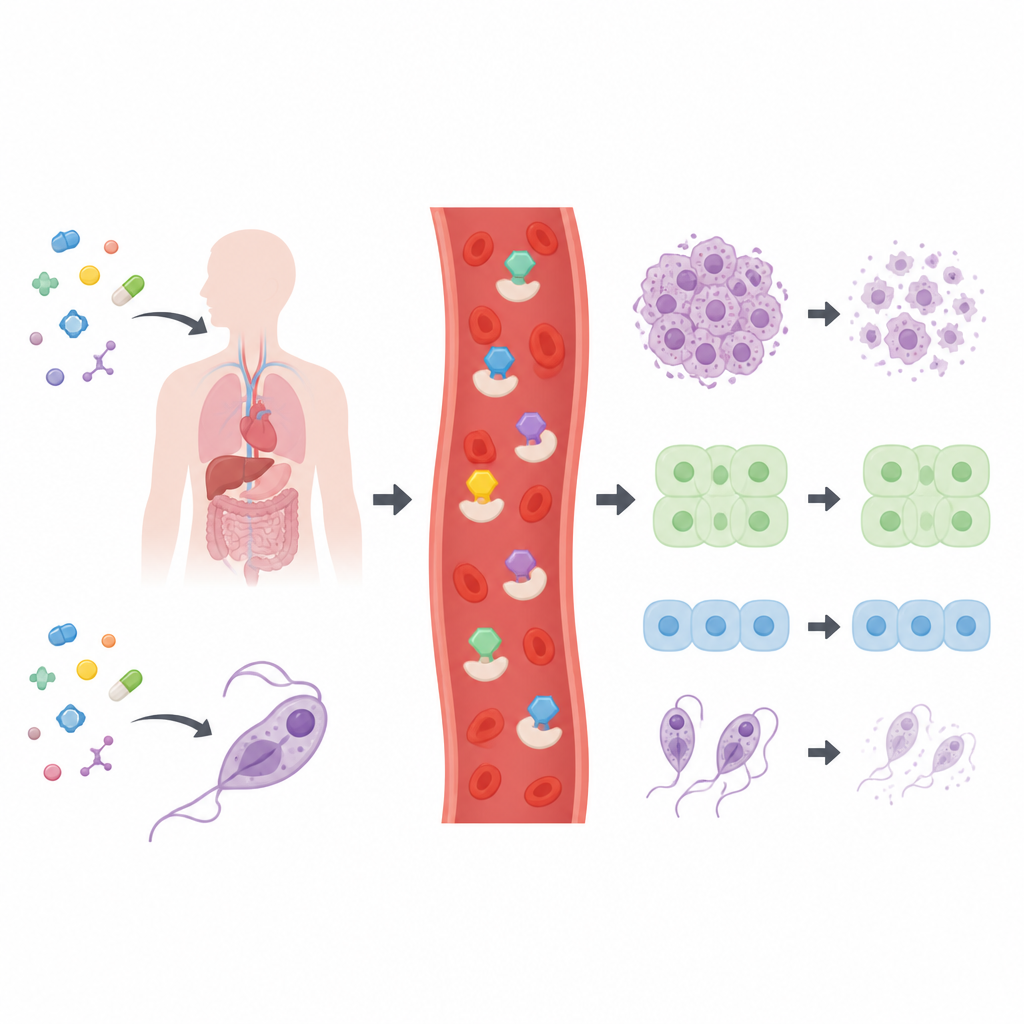
Eine Bibliothek von Kandidaten auf dem Prüfstand
Die Forscher stellten und charakterisierten eine Reihe von 28 verwandten Thiosemicarbazon‑Verbindungen her, die meist um ringförmige Kohlenstoffgerüste aufgebaut sind, wie sie aus vielen Arzneimitteln bekannt sind. Bevor sie an Zellen getestet wurden, prüfte man, ob die Moleküle gängige Regeln zur „Drug‑Likeness“ erfüllen, die in der pharmazeutischen Forschung Größe, Polarität und Flexibilität berücksichtigen. Alle Verbindungen bestanden diese grundlegenden Filter, was darauf hindeutet, dass sie vernünftige Ausgangspunkte für die Wirkstoffentwicklung sind. Anschließend setzte das Team eine breite Palette menschlicher Krebszelllinien, zwei Typen normaler menschlicher Zellen und vier krankheitsverursachende Parasiten den Verbindungen aus, um zu ermitteln, welche Strukturen am aktivsten sind.
Die vielversprechendsten Moleküle identifizieren
Die Mehrheit der Bibliothek zeigte nur mäßige Effekte, doch sechs Moleküle stachen heraus. Drei basierten auf einem Pyridinring, eines auf einem Chinolering und eines auf einem Indolring. Diese Spitzenkandidaten verlangsamten oder töteten Krebszellen bereits in niedrigen Konzentrationen und wirkten in mehreren Fällen auch stark gegen Parasiten, die Chagas‑Krankheit, die Schlafkrankheit und Leishmaniose verursachen. Der klare Spitzenreiter mit der Bezeichnung 26 war besonders wirksam gegen Lungen‑, Leber‑, Knochen‑ und Gebärmutterhals‑Krebszelllinien, zeigte dabei aber praktisch keine Toxizität gegenüber normalen Lungen‑ und Darmzellen. Diese Selektivität ist entscheidend, weil sie auf ein therapeutisches Fenster hindeutet, in dem Tumorgewebe angegriffen werden kann, ohne gesundes Gewebe in vergleichbarem Maß zu schädigen.
Wie die Leitverbindung Krebszellen angreift
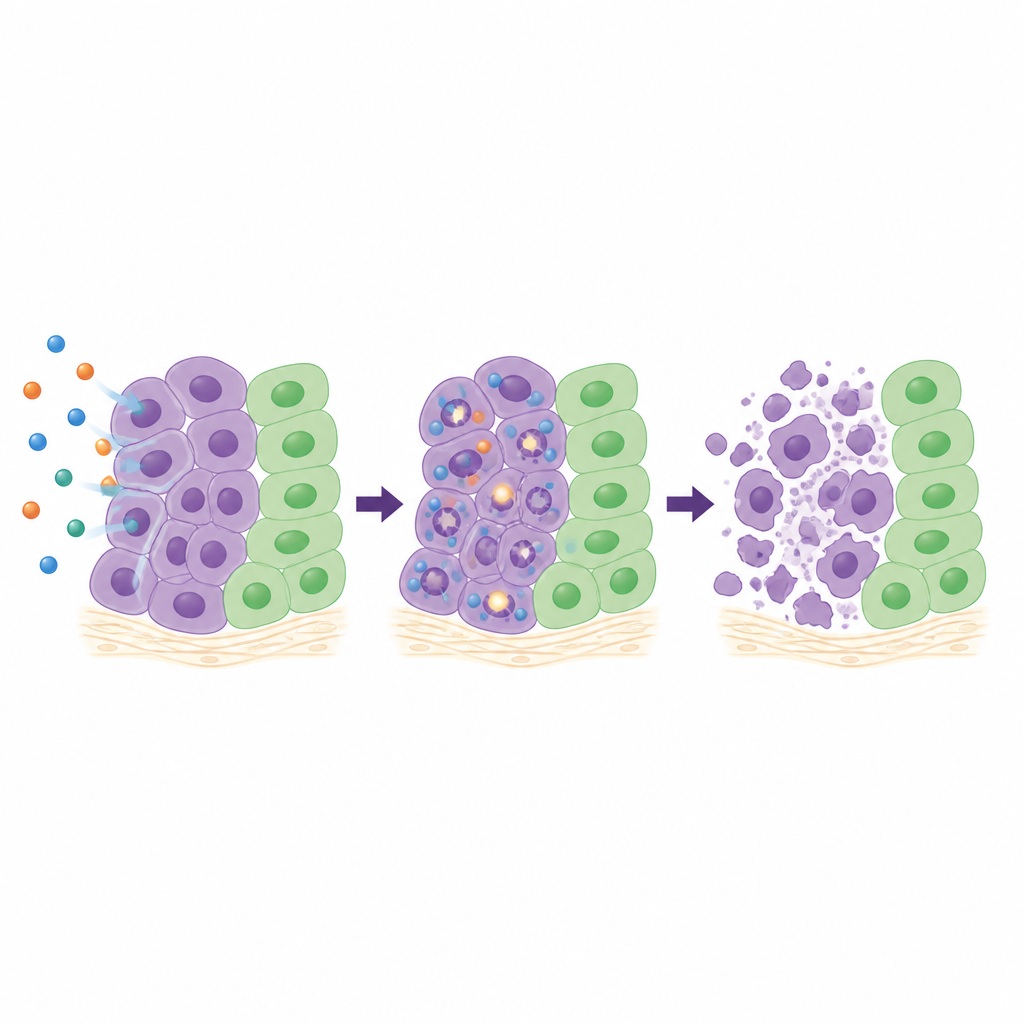
Um zu verstehen, was 26 in Zellen bewirkt, untersuchte das Team vier sensitive Krebszelllinien im Detail. Sie verfolgten den Zellzyklusverlauf, maßen Marker für DNA‑Brüche und beobachteten die Aktivierung innerzellulärer „Selbstzerstörungs“‑Enzyme. Abhängig vom Zelltyp bremste 26 die Zellen in unterschiedlichen Phasen ihres Wachstumszyklus, verursachte aber in allen Fällen über die Zeit zunehmende DNA‑Schäden und aktivierte stark Caspase‑3 und Caspase‑7, Schlüsselfaktoren des programmierten Zelltods. In dreidimensionalen Verbänden von Lungenkrebszellen, die reale Tumoren besser nachbilden als zweidimensionale Zellschichten, reduzierte 26 deutlich das Sphärodenwachstum und schrumpfte diese bei höheren Dosen sogar. In einem Modell mit der Geflügelmembran (Chorioallantoismembran), in dem menschliche Tumorfragmente mit ihrer eigenen Blutversorgung wachsen, verringerte die Behandlung mit 26 die Tumorfläche um etwa zwei Drittel, ohne sichtbare Schädigung des umliegenden Gewebes.
Hinweise aus Metallbindung und Bluttransport
Warum sind einige Thiosemicarbazone aktiv, andere nicht? Mithilfe quantenchemischer Berechnungen zeigten die Autoren, dass die effektivsten Verbindungen elektronische Strukturen besitzen, die das Ergreifen von Metallionen wie Eisen oder Kupfer an bestimmten Atomen begünstigen. Diese Fähigkeit, enge Chelat‑Komplexe zu bilden, wird als Grundlage vieler biologischer Aktivitäten angesehen. Ein Ausreißer, Verbindung 27, verhält sich anders, weil seine Struktur diese Art der Metallbindung verhindert, was auf einen alternativen Wirkmechanismus hindeutet. Das Team testete außerdem, wie leicht die sechs Schlüsselverbindungen ernähnungsähnliche Membranen passieren könnten und wie stark sie an das humanes Serumalbumin, das wichtigste Transportprotein im Blut, binden. Alle zeigten eine eher schlechte passive Darmpermeabilität, was darauf hinweist, dass Formulierungsarbeiten für orale Verabreichung nötig sein werden. Verbindung 26 hingegen band stark an Albumin, und Computersimulationen enthüllten ein stabiles Netzwerk aus Wasserstoffbrücken und hydrophoben Kontakten, das sie in einer bekannten Wirkstoffbindungs‑Tasche verankert.
Was das für künftige Medikamente bedeutet
Zusammen zeigen Experimente und Simulationen, dass ein Mitglied dieser Molekülfamilie, Verbindung 26, Krebszellen selektiv schädigen kann, indem es DNA‑Brüche verursacht und kontrollierten Zelltod auslöst, während die getesteten normalen Zellen weitgehend verschont bleiben. Gleichzeitig zeigen verwandte Moleküle Aktivität gegen mehrere wichtige Parasiten. Obwohl ihre derzeitige Form nicht ideal für die Absorption im Darm ist, machen ihre einfachen Strukturen, klaren Struktur‑Aktivitäts‑Beziehungen und definierten Wechselwirkungen mit Blutproteinen sie zu attraktiven Bausteinen für zukünftiges Wirkstoffdesign. Mit verbesserten Abgabesystemen und Tierversuchen könnten diese Thiosemicarbazone zu neuen Behandlungen sowohl für Krebs als auch für parasitäre Erkrankungen beitragen.
Zitation: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Schlüsselwörter: Thiosemicarbazone, Antikrebsmittel, antiparasitäre Verbindungen, DNA‑Schädigung, Wirkstoffdesign