Clear Sky Science · es
Evaluación biológica y computacional multifacética de tiossemicarbazonas aromáticas y N-heteroaromáticas no sustituidas
Por qué importan estas pequeñas moléculas
El cáncer y las infecciones parasitarias siguen siendo dos de los problemas de salud más persistentes del mundo, y muchos de los fármacos existentes o no funcionan lo suficiente o provocan efectos secundarios importantes. Este estudio explora una familia de moléculas relativamente simples y fáciles de sintetizar, las tiossemicarbazonas, para evaluar si algunas de ellas pueden dañar selectivamente células cancerosas y parásitos patógenos al mismo tiempo que respetan las células humanas sanas. También examina cómo se comportan estas moléculas en el organismo y cómo interaccionan con proteínas sanguíneas, mediante ensayos de laboratorio y simulaciones por ordenador.
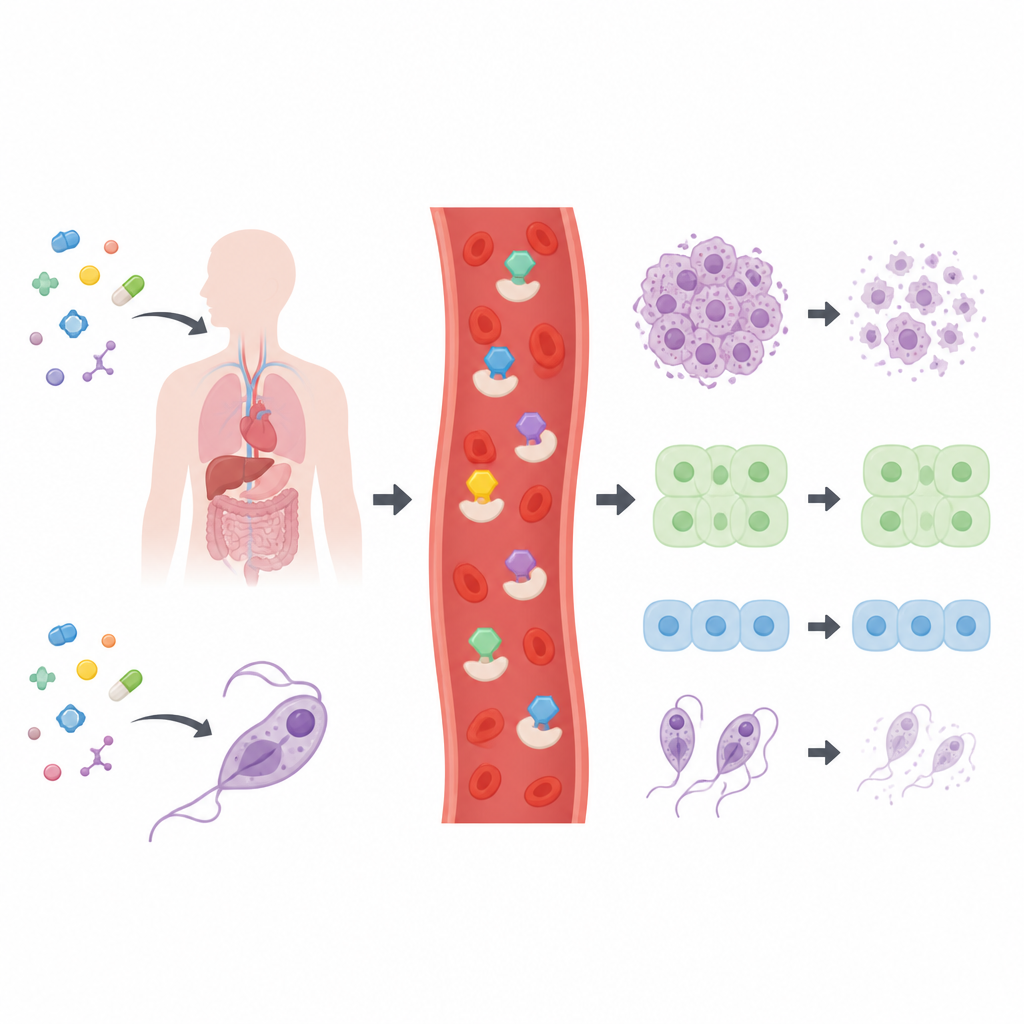
Una biblioteca de candidatos puesta a prueba
Los investigadores sintetizaron y caracterizaron un conjunto de 28 tiossemicarbazonas relacionadas, la mayoría construidas sobre marcos carbonados en forma de anillo conocidos en muchos fármacos. Antes de probarlas en células, comprobaron si las moléculas cumplían las reglas comunes de “similaridad a fármaco” utilizadas en investigación farmacéutica, que consideran tamaño, polaridad y flexibilidad. Todos los compuestos superaron estos filtros básicos, lo que sugiere que son puntos de partida razonables para el desarrollo de fármacos. A continuación, el equipo expuso un amplio panel de líneas celulares humanas cancerosas, dos tipos de células humanas normales y cuatro parásitos patógenos a los compuestos para mapear qué estructuras eran más activas.
Identificando las moléculas más prometedoras
La mayor parte de la biblioteca mostró efectos modestos, pero seis moléculas destacaron. Tres estaban basadas en un anillo de piridina, una en un anillo de quinolina y una en un anillo de indol. Estos candidatos principales ralentizaron o mataron células cancerosas a bajas concentraciones y, en varios casos, también actuaron con fuerza contra parásitos causantes de la enfermedad de Chagas, el sueño africano y la leishmaniasis. La clara favorita, etiquetada como 26, fue especialmente eficaz frente a líneas celulares de cáncer de pulmón, hígado, hueso y cuello uterino, mostrando prácticamente ninguna toxicidad hacia células normales de pulmón y colon. Esa selectividad es crucial, pues sugiere una ventana terapéutica en la que el tejido tumoral puede ser atacado sin causar un daño comparable al tejido sano.
Cómo el compuesto líder ataca las células cancerosas
Para comprender qué hace el 26 dentro de las células, el equipo examinó en detalle cuatro líneas cancerosas sensibles. Siguieron el progreso de las células a través del ciclo celular, midieron marcadores de rotura del ADN y rastrearon la activación de enzimas internas de “autodestrucción”. Dependiendo del tipo celular, el 26 ralentizó las células en distintas fases de su ciclo de crecimiento, pero en todos los casos causó una cantidad creciente de daño en el ADN con el tiempo y activó de forma potente la caspasa‑3 y la caspasa‑7, actores clave en la muerte celular programada. En cúmulos tridimensionales de células de pulmón, que imitan mejor los tumores reales que las capas celulares planas, el 26 redujo de forma marcada el crecimiento de los esferoides e incluso los encogió a dosis más altas. En un modelo de membrana de huevo de gallina donde fragmentos tumorales humanos crecen con su propia vasculatura, el tratamiento con 26 redujo el área tumoral en aproximadamente dos terceras partes sin daño visible en el tejido circundante.
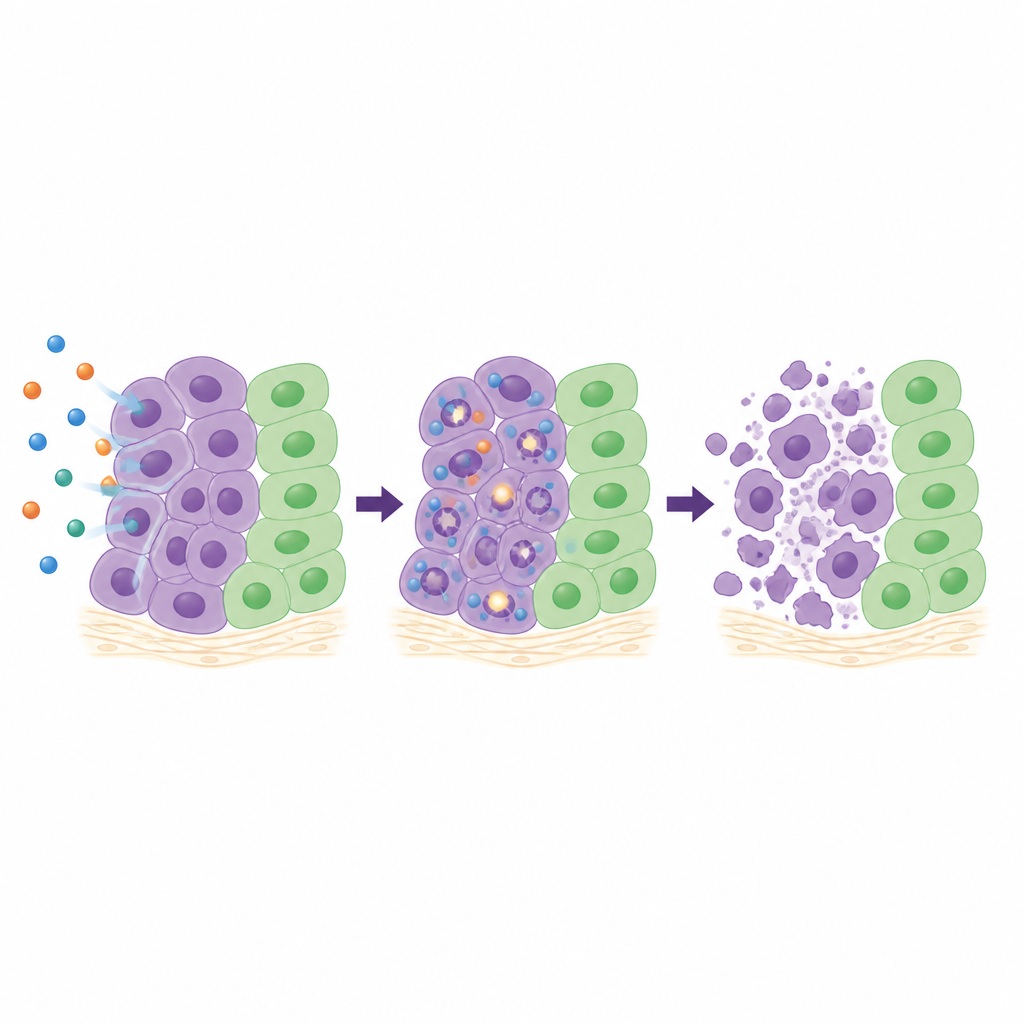
Pistas sobre unión a metales y transporte en sangre
¿Por qué algunas tiossemicarbazonas son activas y otras no? Mediante cálculos cuántico‑químicos, los autores mostraron que los compuestos más efectivos tienen estructuras electrónicas que favorecen la captura de iones metálicos como hierro o cobre en átomos específicos. Esta capacidad de formar complejos “quelato” firmes se considera la base de gran parte de su actividad biológica. Un compuesto destacado, el 27, se comporta de forma diferente porque su estructura impide este tipo de unión a metales, lo que sugiere un modo de acción alternativo. El equipo también evaluó la facilidad con la que los seis compuestos clave podrían cruzar membranas similares a las intestinales y con qué fuerza se unen a la albúmina sérica humana, la principal proteína transportadora en sangre. Todos mostraron una permeabilidad pasiva intestinal bastante baja, lo que indica que será necesario trabajar en formulaciones para la administración oral. El compuesto 26, sin embargo, se unió fuertemente a la albúmina, y las simulaciones por ordenador revelaron un conjunto estable de enlaces de hidrógeno y contactos hidrofóbicos que ayudan a anclarlo en un bolsillo conocido de unión a fármacos.
Qué significa esto para futuros fármacos
En conjunto, los experimentos y las simulaciones muestran que un miembro de esta familia molecular, el compuesto 26, puede dañar selectivamente células cancerosas provocando roturas en el ADN y desencadenando la muerte celular controlada, al tiempo que deja en gran medida indemnes a las células normales probadas. Paralelamente, moléculas relacionadas muestran actividad contra varios parásitos importantes. Aunque su forma actual no es ideal para la absorción intestinal, sus estructuras simples, relaciones estructura‑actividad claras e interacciones definidas con proteínas sanguíneas las convierten en bloques de construcción atractivos para el diseño de fármacos futuros. Con mejores sistemas de administración y ensayos en animales, estas tiossemicarbazonas podrían contribuir a nuevos tratamientos tanto para el cáncer como para enfermedades parasitarias.
Cita: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Palabras clave: tiossemicarbazonas, agentes anticancerígenos, compuestos antiparasitarios, daño en el ADN, diseño de fármacos