Clear Sky Science · pl
Wielopłaszczyznowa ocena biologiczna i obliczeniowa aromatycznych i N‑heteroaromatycznych nienacechowanych tiomaszczwiozazonów
Dlaczego te małe cząsteczki mają znaczenie
Nowotwory i infekcje pasożytnicze pozostają jednymi z najbardziej uporczywych problemów zdrowotnych na świecie, a wiele dostępnych leków albo działa niewystarczająco skutecznie, albo wywołuje silne skutki uboczne. W tym badaniu analizowano rodzinę relatywnie prostych, łatwych do syntezy związków zwanych tiomaszczwiozazonami, aby sprawdzić, czy niektóre z nich mogą selektywnie uszkadzać komórki nowotworowe i chorobotwórcze pasożyty, oszczędzając przy tym zdrowe komórki ludzkie. Badano też, jak te związki zachowują się w organizmie i jak oddziałują z białkami krwi, stosując zarówno testy laboratoryjne, jak i symulacje komputerowe.
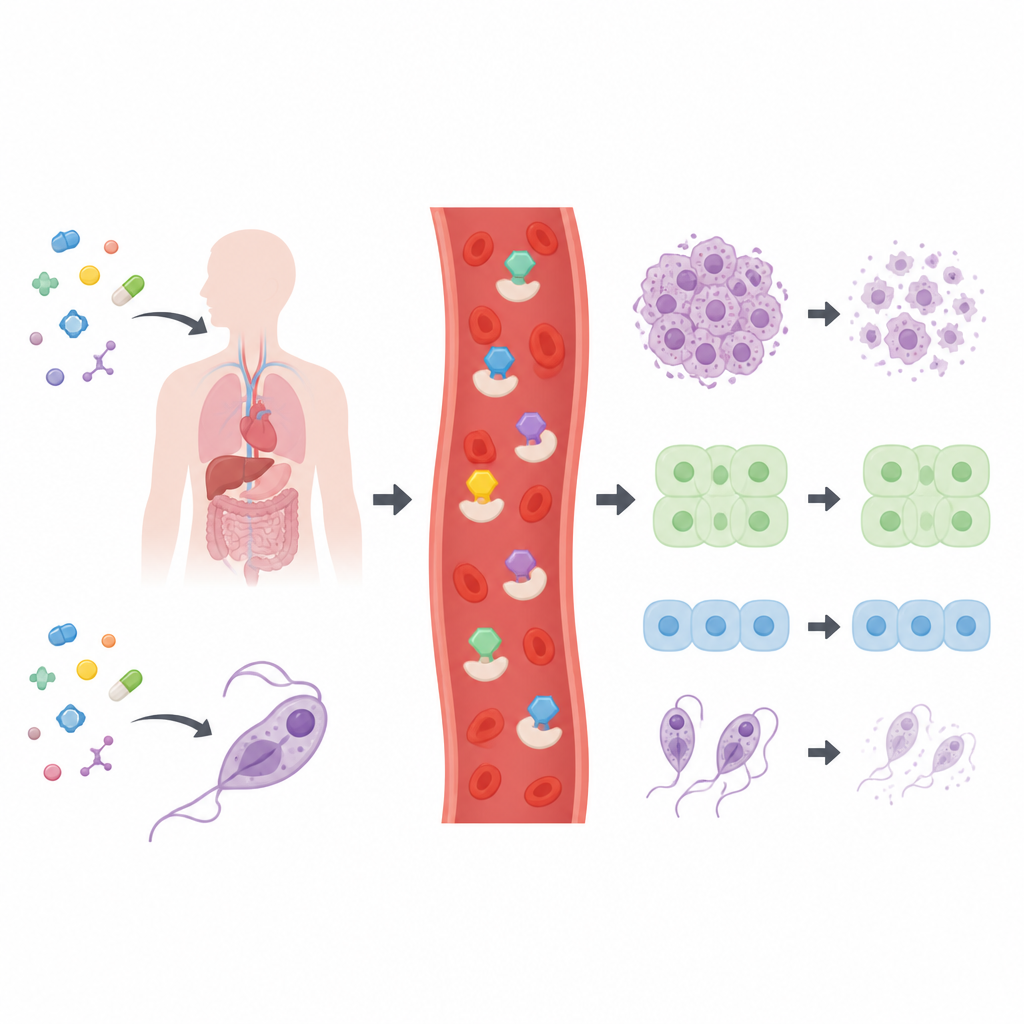
Biblioteka kandydatów poddana próbom
Naukowcy stworzyli i scharakteryzowali zestaw 28 spokrewnionych związków tiomaszczwiozazonowych, większość oparta na pierścieniowych ramach węglowych znanych z wielu leków. Zanim przetestowali je na komórkach, sprawdzili, czy cząsteczki spełniają powszechne zasady „drug‑likeness” stosowane w badaniach farmaceutycznych, które uwzględniają rozmiar, polarność i elastyczność. Wszystkie związki przeszły te podstawowe filtry, co sugeruje, że są rozsądnymi punktami wyjścia do rozwoju leków. Zespół następnie wystawił szeroki panel ludzkich linii komórek nowotworowych, dwa typy normalnych komórek ludzkich oraz cztery chorobotwórcze pasożyty na działanie tych związków, aby określić, które struktury wykazują największą aktywność.
Wybór najbardziej obiecujących molekuł
Większość bibliotek wykazała tylko umiarkowane efekty, ale sześć cząsteczek wyróżniło się. Trzy opierały się na pierścieniu pirydynowym, jedna na chinolinowym, a jedna na indolowym. Te najlepsze kandydaty albo spowalniały, albo zabijały komórki nowotworowe przy niskich stężeniach i w kilku przypadkach silnie działały przeciw pasożytom wywołującym chorobę Chagasa, śpiączkę afrykańską i leiszmaniozę. Wyraźnym faworytem był związek oznaczony jako 26, który wykazywał szczególne działanie przeciw liniom nowotworowym płuca, wątroby, kości i szyjki macicy, przy niemal braku toksyczności wobec normalnych komórek płuc i okrężnicy. Ta selektywność jest kluczowa, ponieważ wskazuje na okno terapeutyczne, w którym można zaatakować tkankę nowotworową bez porównywalnej szkody dla tkanek zdrowych.
Jak wiodący związek atakuje komórki nowotworowe
Aby zrozumieć, co związek 26 robi wewnątrz komórek, zespół dokładnie przebadał cztery wrażliwe linie nowotworowe. Śledzili przebieg cyklu komórkowego, mierzyli markery pęknięć DNA i monitorowali aktywację wewnętrznych enzymów „autodestrukcji”. W zależności od typu komórek, 26 zatrzymywał je na różnych etapach cyklu wzrostu, ale we wszystkich przypadkach powodował narastające uszkodzenia DNA w czasie oraz silnie aktywował kaspazę‑3 i kaspazę‑7, kluczowe elementy programowanej śmierci komórki. W trójwymiarowych skupiskach komórek płucnych, które lepiej naśladują prawdziwe guzy niż płaskie monowarstwy, 26 wyraźnie zmniejszał wzrost sferoidów, a przy wyższych dawkach nawet je kurczył. W modelu błony jaja kurzego, gdzie fragmenty ludzkich guzów rosną z własnym unaczynieniem, leczenie 26 zmniejszyło powierzchnię guza o około dwie trzecie bez widocznych uszkodzeń otaczających tkanek.
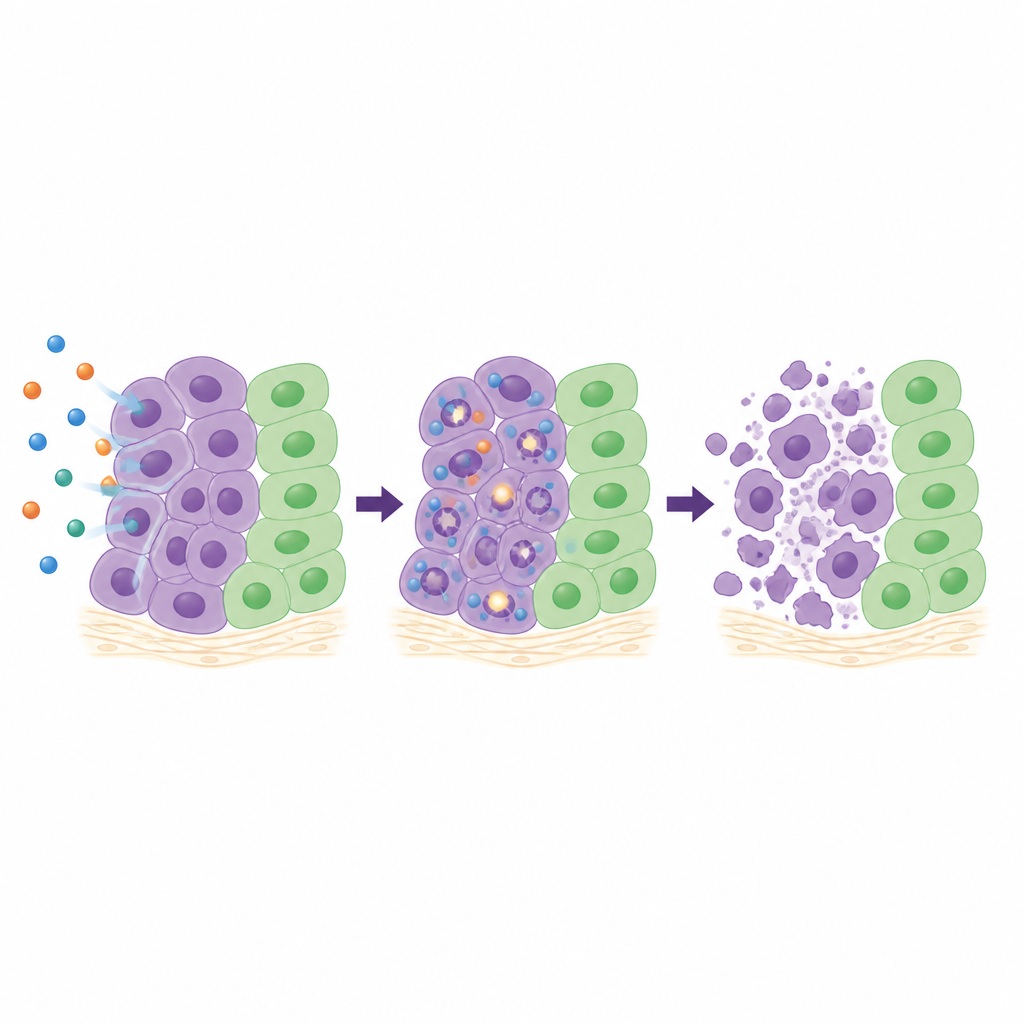
Wskazówki z wiązania metali i transportu we krwi
Dlaczego niektóre tiomaszczwiozazony są aktywne, a inne nie? Wykorzystując obliczenia kwantowo‑chemiczne, autorzy pokazali, że najbardziej skuteczne związki mają strukturę elektronową sprzyjającą chwytaniu jonów metali, takich jak żelazo czy miedź, w określonych atomach. Zdolność do tworzenia silnych kompleksów „chelatujących” uważa się za podstawę wielu ich aktywności biologicznych. Jeden z wyróżniających się związków, numer 27, zachowuje się inaczej, ponieważ jego struktura uniemożliwia tego rodzaju wiązanie metalu, co sugeruje alternatywny mechanizm działania. Zespół sprawdził też, jak łatwo sześć kluczowych związków może przekraczać membrany przypominające jelito oraz jak silnie wiążą się z albuminą surowicy ludzkiej, głównym białkiem transportującym krew. Wszystkie miały dość słabą pasywną przepuszczalność przez jelito, co sugeruje, że konieczne będzie opracowanie formulacji dla podawania doustnego. Związek 26 jednak silnie wiązał się z albuminą, a symulacje komputerowe ujawniły stabilny zestaw wiązań wodorowych i kontaktów hydrofobowych, które pomagają zakotwiczyć go w znanym kieszeniowym miejscu wiążącym leki.
Co to oznacza dla przyszłych leków
Podsumowując, eksperymenty i symulacje pokazują, że jeden członek tej rodziny molekularnej, związek 26, może selektywnie uszkadzać komórki nowotworowe poprzez powodowanie pęknięć DNA i wywoływanie kontrolowanej śmierci komórki, pozostawiając testowane komórki normalne w dużej mierze nienaruszone. Jednocześnie spokrewnione molekuły wykazują aktywność przeciw kilku istotnym pasożytom. Chociaż ich obecna forma nie jest idealna pod względem wchłaniania przez jelito, proste struktury, przejrzyste zależności struktura‑aktywność i określone interakcje z białkami krwi czynią je atrakcyjnymi cegiełkami do przyszłego projektowania leków. Przy lepszych systemach dostarczania i badaniach na zwierzętach te tiomaszczwiozazony mogłyby przyczynić się do nowych terapii zarówno w onkologii, jak i w leczeniu chorób pasożytniczych.
Cytowanie: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Słowa kluczowe: tiomaszczwiozazony, środki przeciwnowotworowe, związki przeciwpasożytnicze, uszkodzenia DNA, projektowanie leków