Clear Sky Science · it
Valutazione biologica e computazionale multifaccettata di tiosemicarbazoni aromatici e N-eteroaromatici non sostituiti
Perché queste piccole molecole sono importanti
I tumori e le infezioni parassitarie restano tra i problemi di salute più ostinati a livello globale, e molti farmaci esistenti non sono sufficientemente efficaci o provocano effetti collaterali rilevanti. Questo studio esplora una famiglia di molecole relativamente semplici e facilmente sintetizzabili, i tiosemicarbazoni, per verificare se alcune di esse possano danneggiare selettivamente le cellule tumorali e i parassiti patogeni preservando le cellule umane sane. Esamina inoltre il comportamento di queste molecole nell’organismo e il loro interagire con le proteine plasmatiche, impiegando sia test di laboratorio sia simulazioni al computer.
Una libreria di candidati messa alla prova
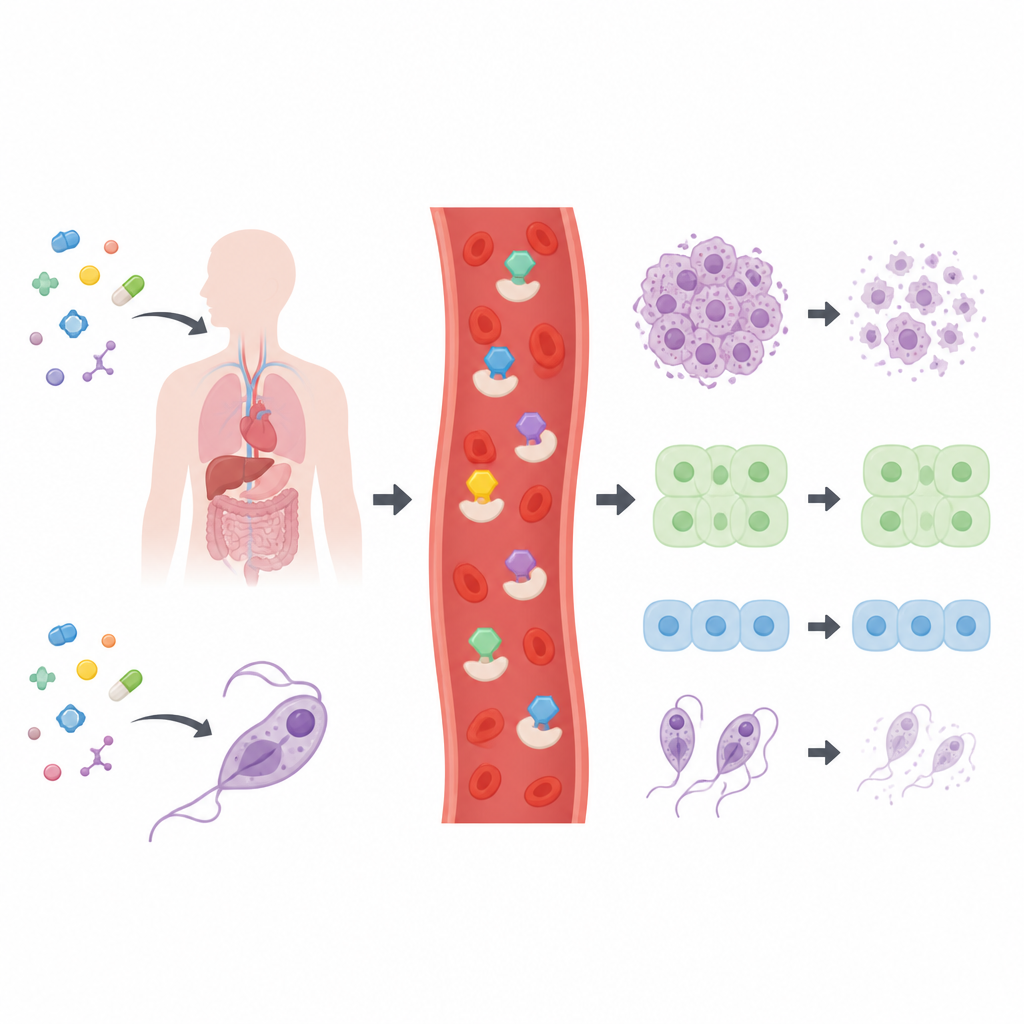
I ricercatori hanno sintetizzato e caratterizzato un insieme di 28 tiosemicarbazoni correlati, per lo più costruiti attorno a schemi anulari di carbonio noti in molti farmaci. Prima di testarli sulle cellule, hanno verificato se le molecole rispettassero comuni regole di “drug‑likeness” usate nella ricerca farmaceutica, che valutano dimensione, polarità e flessibilità. Tutti i composti hanno superato questi filtri di base, suggerendo che siano punti di partenza ragionevoli per lo sviluppo farmacologico. Il gruppo ha quindi esposto un ampio pannello di linee cellulari tumorali umane, due tipi di cellule umane normali e quattro parassiti patogeni ai composti per mappare quali strutture risultassero più attive.
Individuazione delle molecole più promettenti
La maggior parte della libreria ha mostrato effetti modesti, ma sei molecole si sono distinte. Tre erano basate su un anello di piridina, una su un anello di chinolina e una su un anello di indolo. Questi candidati principali rallentavano o uccidevano le cellule tumorali a basse concentrazioni e, in diversi casi, agivano efficacemente anche contro parassiti responsabili della malattia di Chagas, della tripanosomiasi africana e della leishmaniosi. Il chiaro capofila, indicato come composto 26, è risultato particolarmente efficace contro linee cellulari di tumore del polmone, fegato, osso e cervice, mostrando al contempo praticamente nessuna tossicità verso cellule polmonari e del colon normali. Tale selettività è cruciale, perché suggerisce una finestra terapeutica in cui il tessuto tumorale può essere colpito senza danni comparabili al tessuto sano.
Come il composto di punta attacca le cellule tumorali
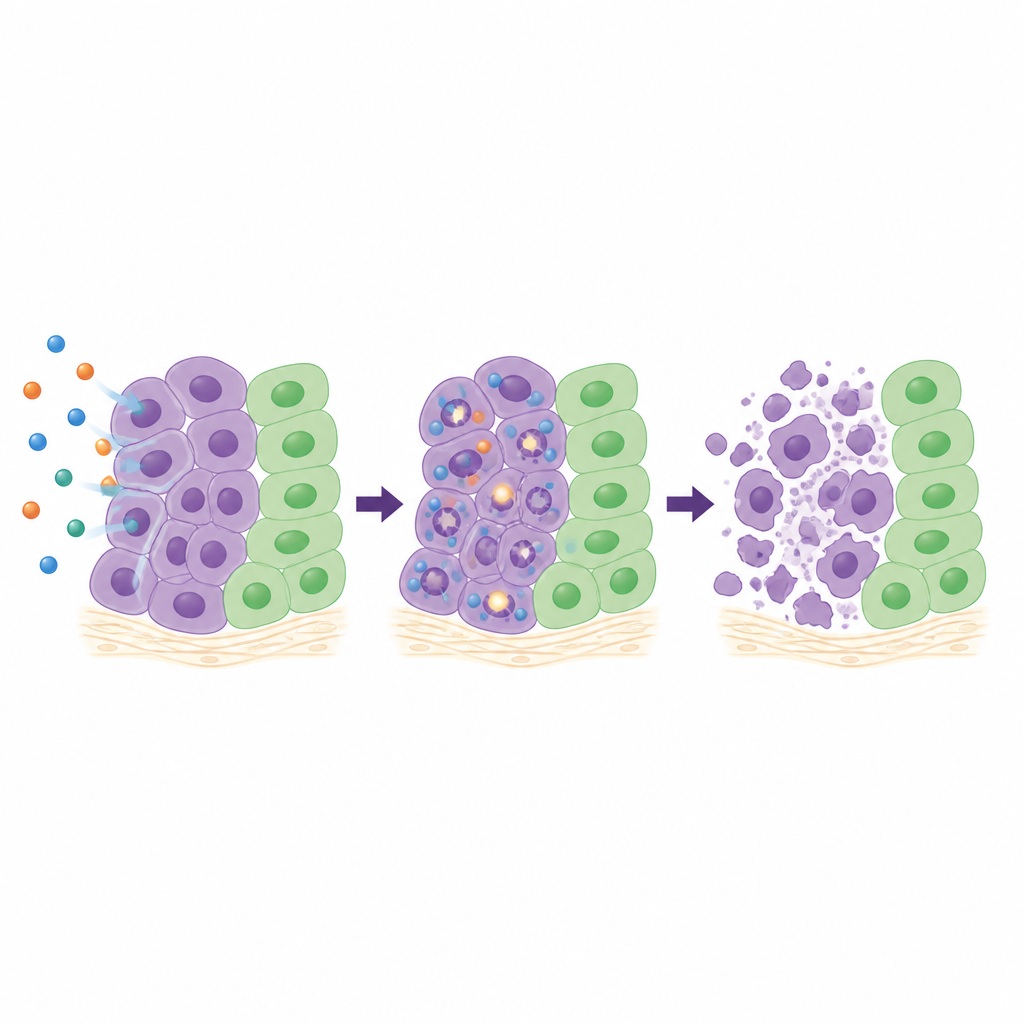
Per capire cosa faccia il composto 26 all’interno delle cellule, il team ha analizzato in dettaglio quattro linee tumorali sensibili. Ha seguito la progressione del ciclo cellulare, misurato marcatori di rottura del DNA e monitorato l’attivazione di enzimi interni di “auto‑distruzione”. A seconda del tipo cellulare, il 26 ha rallentato le cellule in differenti fasi del ciclo di crescita, ma in tutti i casi ha provocato un aumento del danno al DNA nel tempo e ha fortemente attivato caspasi‑3 e caspasi‑7, attori chiave nell’apoptosi programmata. In aggregati tridimensionali di cellule tumorali polmonari, che meglio imitano i tumori reali rispetto a monostrati, il 26 ha ridotto nettamente la crescita degli sfere e le ha addirittura ridotte a dosi maggiori. In un modello su membrana di uovo di gallina, dove frammenti tumorali umani crescono con il loro apporto vascolare, il trattamento con 26 ha ridotto l’area tumorale di circa due terzi senza danni visibili ai tessuti circostanti.
Indizi dal legame con i metalli e dal trasporto nel sangue
Perché alcuni tiosemicarbazoni sono attivi mentre altri no? Mediante calcoli quantistico‑chimici, gli autori hanno mostrato che i composti più efficaci possiedono strutture elettroniche che favoriscono il legame di ioni metallici come ferro o rame in atomi specifici. Questa capacità di formare complessi chelati stabili è ritenuta alla base di gran parte della loro attività biologica. Un composto particolare, il 27, si comporta diversamente perché la sua struttura impedisce questo tipo di legame con i metalli, suggerendo un meccanismo d’azione alternativo. Il team ha anche testato quanto facilmente i sei composti chiave possano attraversare membrane di tipo intestinale e quanto fortemente si leghino all’albumina sierica umana, la principale proteina trasportatrice nel sangue. Tutti hanno mostrato una permeabilità intestinale passiva piuttosto scarsa, indicando che sarà necessario lavorare sulla formulazione per la somministrazione orale. Il composto 26, tuttavia, si è legato saldamente all’albumina, e le simulazioni al computer hanno rivelato un insieme stabile di legami idrogeno e contatti idrofobici che ne favoriscono l’ancoraggio in una tasca nota per il binding dei farmaci.
Cosa significa per i farmaci futuri
Presi nel loro insieme, esperimenti e simulazioni mostrano che un membro di questa famiglia molecolare, il composto 26, può danneggiare selettivamente le cellule tumorali causando rotture nel DNA e innescando la morte cellulare programmata, lasciando perlopiù indenni le cellule normali testate. Allo stesso tempo, molecole correlate mostrano attività contro diversi parassiti di rilevanza clinica. Sebbene la loro forma attuale non sia ideale per l’assorbimento intestinale, le strutture semplici, le chiare relazioni struttura‑attività e le interazioni definite con le proteine plasmatiche ne fanno mattoni attraenti per la progettazione di futuri farmaci. Con sistemi di somministrazione migliorati e test su animali, questi tiosemicarbazoni potrebbero contribuire a nuovi trattamenti sia per il cancro sia per le malattie parassitarie.
Citazione: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Parole chiave: tiosemicarbazoni, agenti antitumorali, composti antiparassitari, danno al DNA, progettazione di farmaci