Clear Sky Science · pt
Avaliação biológica e computacional multifacetada de tiosemicarbazonas aromáticas e N‑heteroaromáticas não substituídas
Por que essas pequenas moléculas são importantes
Câncer e infecções parasitárias continuam entre os problemas de saúde mais persistentes do mundo, e muitos medicamentos existentes ou não funcionam bem o suficiente ou provocam efeitos colaterais intensos. Este estudo explora uma família de moléculas relativamente simples e fáceis de sintetizar, chamadas tiosemicarbazonas, para avaliar se algumas delas podem danificar seletivamente células cancerígenas e parasitas causadores de doenças, poupando células humanas saudáveis. Também examina como essas moléculas se comportam no organismo e como interagem com proteínas plasmáticas, empregando tanto testes laboratoriais quanto simulações computacionais.
Uma biblioteca de candidatos posta à prova
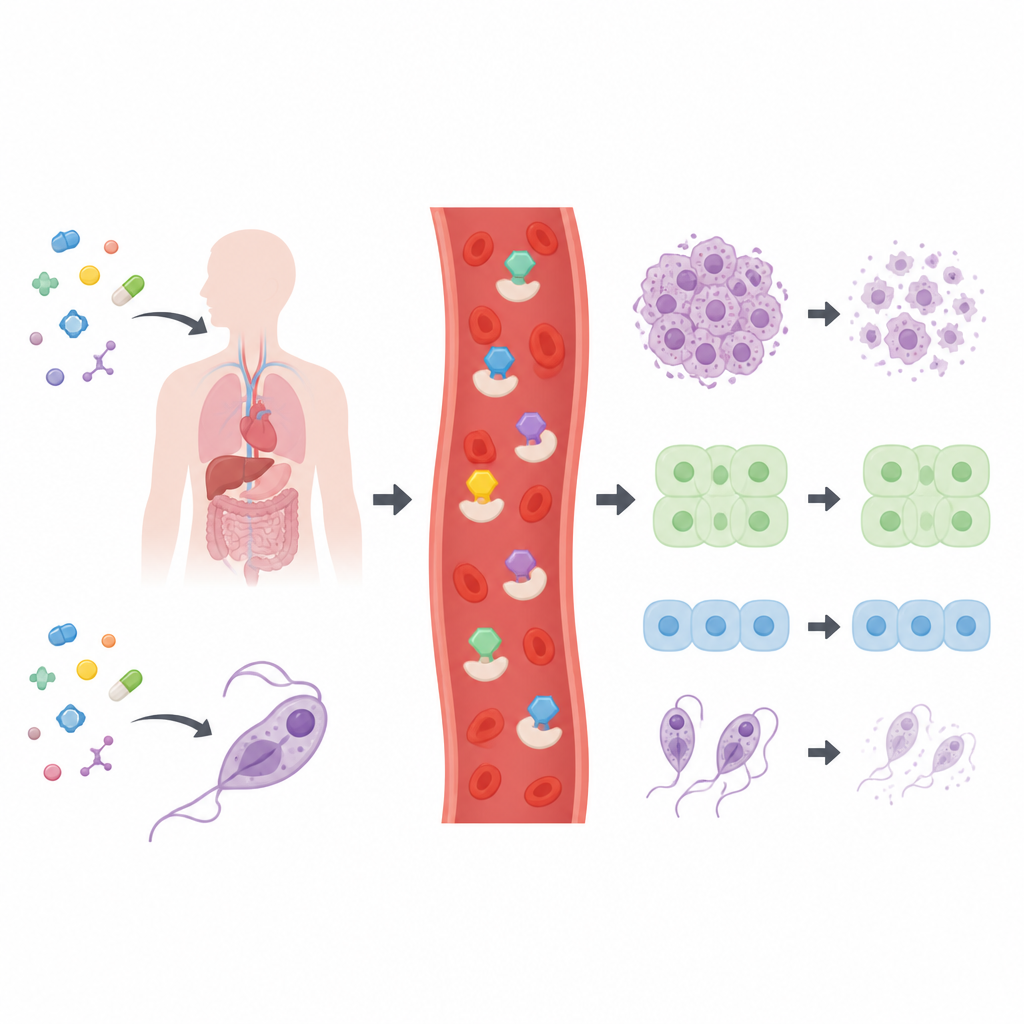
Os pesquisadores criaram e caracterizaram um conjunto de 28 compostos tiosemicarbazona relacionados, em sua maioria construídos sobre esqueletos carbônicos cíclicos conhecidos em muitos fármacos. Antes de testá‑los em células, verificaram se as moléculas atendiam às regras comuns de “drug‑likeness” usadas na pesquisa farmacêutica, que consideram tamanho, polaridade e flexibilidade. Todos os compostos passaram nesses filtros básicos, sugerindo que são pontos de partida razoáveis para desenvolvimento de fármacos. A equipe então expôs um amplo painel de linhagens celulares humanas de câncer, dois tipos de células humanas normais e quatro parasitas causadores de doenças aos compostos para mapear quais estruturas eram mais ativas.
Identificando as moléculas mais promissoras
A maior parte da biblioteca apresentou apenas efeitos modestos, mas seis moléculas se destacaram. Três eram baseadas em um anel de piridina, uma em um anel de quinolina e uma em um anel de indol. Esses candidatos principais retardaram ou mataram células cancerígenas em baixas concentrações e, em vários casos, também agiram fortemente contra parasitas que causam doença de Chagas, sono africano e leishmaniose. O claro favorito, rotulado 26, foi especialmente eficaz contra linhagens de câncer de pulmão, fígado, osso e colo do útero, mostrando praticamente nenhuma toxicidade frente a células normais de pulmão e cólon. Essa seletividade é crucial, pois indica uma janela em que o tecido tumoral pode ser atacado sem causar dano comparável ao tecido saudável.
Como o composto líder ataca células cancerígenas
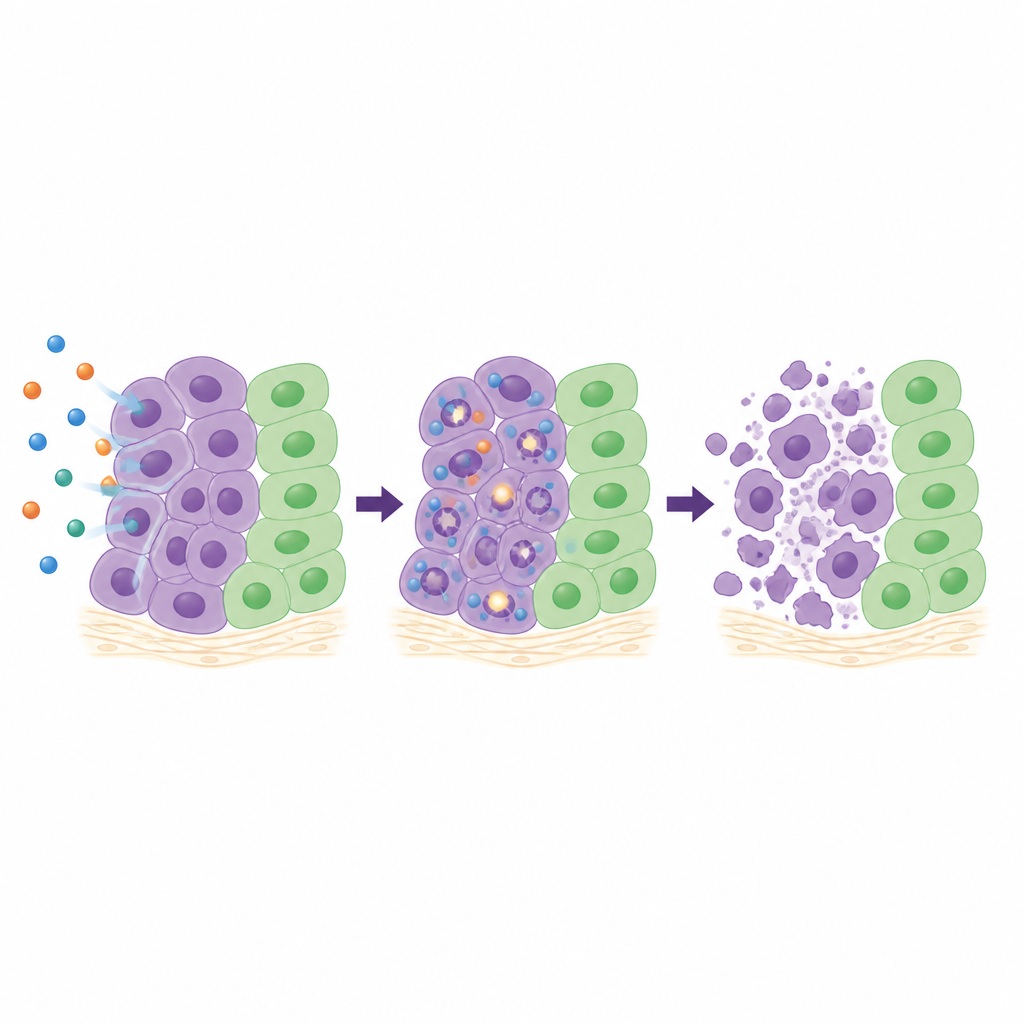
Para entender o que o 26 faz dentro das células, a equipe examinou em detalhe quatro linhagens cancerígenas sensíveis. Acompanharam a progressão das células pelo ciclo celular, mediram marcadores de quebra do DNA e rastrearam a ativação de enzimas internas de “autodestruição”. Dependendo do tipo celular, o 26 retardou as células em diferentes estágios do ciclo de crescimento, mas em todos os casos causou aumento gradual de danos ao DNA e ativou fortemente caspase‑3 e caspase‑7, protagonistas da morte celular programada. Em aglomerados tridimensionais de células de câncer de pulmão, que imitam mais fielmente tumores reais do que camadas celulares planas, o 26 reduziu acentuadamente o crescimento de esferoides e até os encolheu em doses mais altas. Em um modelo de membrana de ovo de galinha onde fragmentos tumorais humanos crescem com seu próprio suprimento sanguíneo, o tratamento com 26 reduziu a área tumoral em cerca de dois terços sem dano visível ao tecido circundante.
Pistas a partir da ligação a metais e do transporte sanguíneo
Por que algumas tiosemicarbazonas são ativas enquanto outras não? Usando cálculos quântico‑químicos, os autores mostraram que os compostos mais eficazes têm estruturas eletrônicas que favorecem a captura de íons metálicos como ferro ou cobre em átomos específicos. Essa capacidade de formar complexos “quelatos” estáveis é considerada a base de grande parte de sua atividade biológica. Um composto distinto, o 27, comportou‑se de forma diferente porque sua estrutura impede esse tipo de ligação a metais, sugerindo um modo alternativo de ação. A equipe também testou com que facilidade os seis compostos principais poderiam atravessar membranas tipo intestinal e quão fortemente se ligavam à albumina sérica humana, a principal proteína transportadora no sangue. Todos apresentaram permeabilidade passiva intestinal relativamente baixa, o que indica que será necessário trabalho de formulação para administração oral. O composto 26, contudo, ligou‑se fortemente à albumina, e simulações computacionais revelaram um conjunto estável de ligações de hidrogênio e contatos hidrofóbicos que ajudam a ancorá‑lo em um bolso conhecido de ligação a fármacos.
O que isso significa para futuros medicamentos
Em conjunto, experimentos e simulações mostram que um membro dessa família molecular, o composto 26, pode danificar seletivamente células cancerígenas ao causar quebras no DNA e desencadear morte celular programada, enquanto deixa as células normais testadas em grande parte ilesas. Ao mesmo tempo, moléculas relacionadas apresentam atividade contra vários parasitas importantes. Embora sua forma atual não seja ideal para absorção pelo trato gastrointestinal, suas estruturas simples, relações claras entre estrutura e atividade e interações definidas com proteínas plasmáticas os tornam blocos de construção atraentes para o desenho de futuros fármacos. Com sistemas de entrega melhores e testes animais, essas tiosemicarbazonas podem contribuir para novos tratamentos tanto para o câncer quanto para doenças parasitárias.
Citação: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Palavras-chave: tiosemicarbazonas, agentes anticâncer, compostos antiparasitários, danos ao DNA, design de fármacos