Clear Sky Science · nl
Veelzijdige biologische en computationele beoordeling van aromatische en N-heteroaromatische niet-gesubstitueerde thiosemicarbazonen
Waarom deze kleine moleculen ertoe doen
Kanker en parasitaire infecties blijven twee van de hardnekkigste gezondheidsproblemen wereldwijd, en veel bestaande medicijnen werken niet goed genoeg of veroorzaken sterke bijwerkingen. Deze studie onderzoekt een familie van relatief eenvoudige, gemakkelijk te maken moleculen, thiosemicarbazonen genoemd, om te zien of sommige daarvan selectief kankercellen en ziekteveroorzakende parasieten kunnen beschadigen terwijl gezonde menselijke cellen gespaard blijven. Er wordt ook gekeken naar hoe deze moleculen zich in het lichaam gedragen en hoe ze interageren met bloedproteïnen, met behulp van laboratoriumtests en computersimulaties.
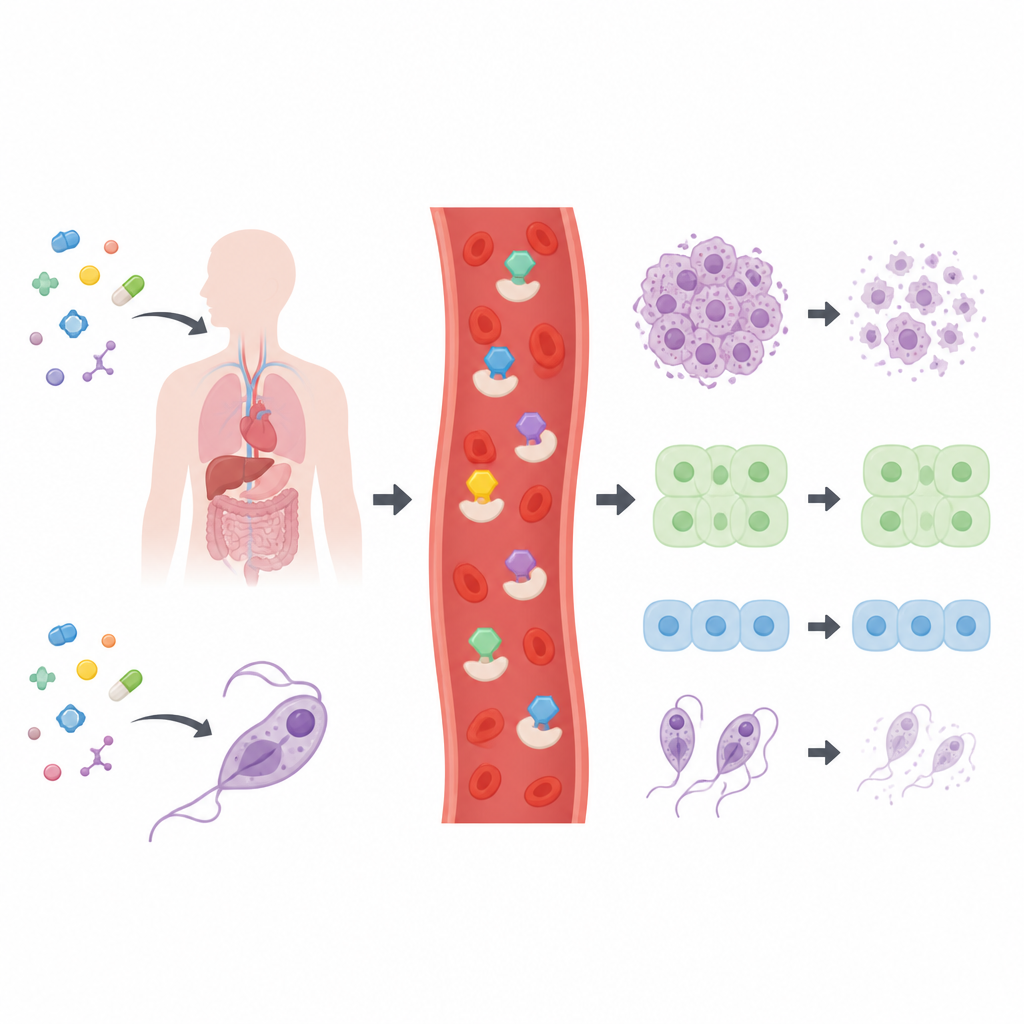
Een bibliotheek aan kandidaten op de proef gesteld
De onderzoekers maakten en karakteriseerden een reeks van 28 verwante thiosemicarbazoneverbindingen, waarvan de meeste zijn opgebouwd rond ringvormige koolstofskeletjes die in veel geneesmiddelen voorkomen. Voordat ze op cellen werden getest, controleerden ze of de moleculen voldeden aan gangbare regels voor “drug‑likeness” die in de farmaceutische research worden gebruikt en die kijken naar grootte, polariteit en flexibiliteit. Alle verbindingen slaagden voor deze basale filters, wat suggereert dat ze redelijke uitgangspunten zijn voor geneesmiddelenontwikkeling. Het team stelde daarna een breed panel van menselijke kankercellijnen, twee soorten normale menselijke cellen en vier ziekteveroorzakende parasieten bloot aan de verbindingen om in kaart te brengen welke structuren het meest actief waren.
Het aanwijzen van de meest veelbelovende moleculen
Het merendeel van de bibliotheek liet slechts bescheiden effecten zien, maar zes moleculen staken eruit. Drie waren gebaseerd op een pyridine‑ring, één op een kinoline‑ring en één op een indool‑ring. Deze topkandidaten vertraagden of doodden kankercellen bij lage concentraties en werkten in meerdere gevallen ook sterk tegen parasieten die Chagas‑ziekte, Afrikaanse slaapziekte en leishmaniasis veroorzaken. De duidelijke koploper, aangeduid als 26, was bijzonder effectief tegen long-, lever-, bot- en baarmoederhalskankercellijnen en toonde vrijwel geen toxiciteit tegenover normale long- en darmcellen. Die selectiviteit is cruciaal, omdat ze wijst op een venster waarin tumorgebied kan worden aangevallen zonder vergelijkbare schade aan gezond weefsel.
Hoe de leidende verbinding kankercellen aanvalt
Om te begrijpen wat 26 binnenin cellen doet, bestudeerde het team vier gevoelige kankercellijnen in detail. Ze volgden hoe cellen door de celcyclus gaan, maten markeringen van DNA‑breuken en volgden de activatie van interne “zelfvernietigings”enzymen. Afhankelijk van het celtype vertraagde 26 cellen in verschillende stadia van hun groeicyclus, maar in alle gevallen veroorzaakte het in de loop van de tijd toenemende DNA‑schade en zette het sterk aan tot activatie van caspase‑3 en caspase‑7, sleutelspelers in geprogrammeerde celdood. In driedimensionale clusters van longkankercellen, die echte tumoren beter nabootsen dan platte cellagen, verminderde 26 scherp de sferoïde groei en krimpten deze bij hogere doses zelfs. In een kippenei-membraanmodel waarin menselijke tumorfragmenten groeien met hun eigen bloedvoorziening, verminderde behandeling met 26 de tumoroppervlakte met ongeveer twee derde zonder zichtbare schade aan het omringende weefsel.
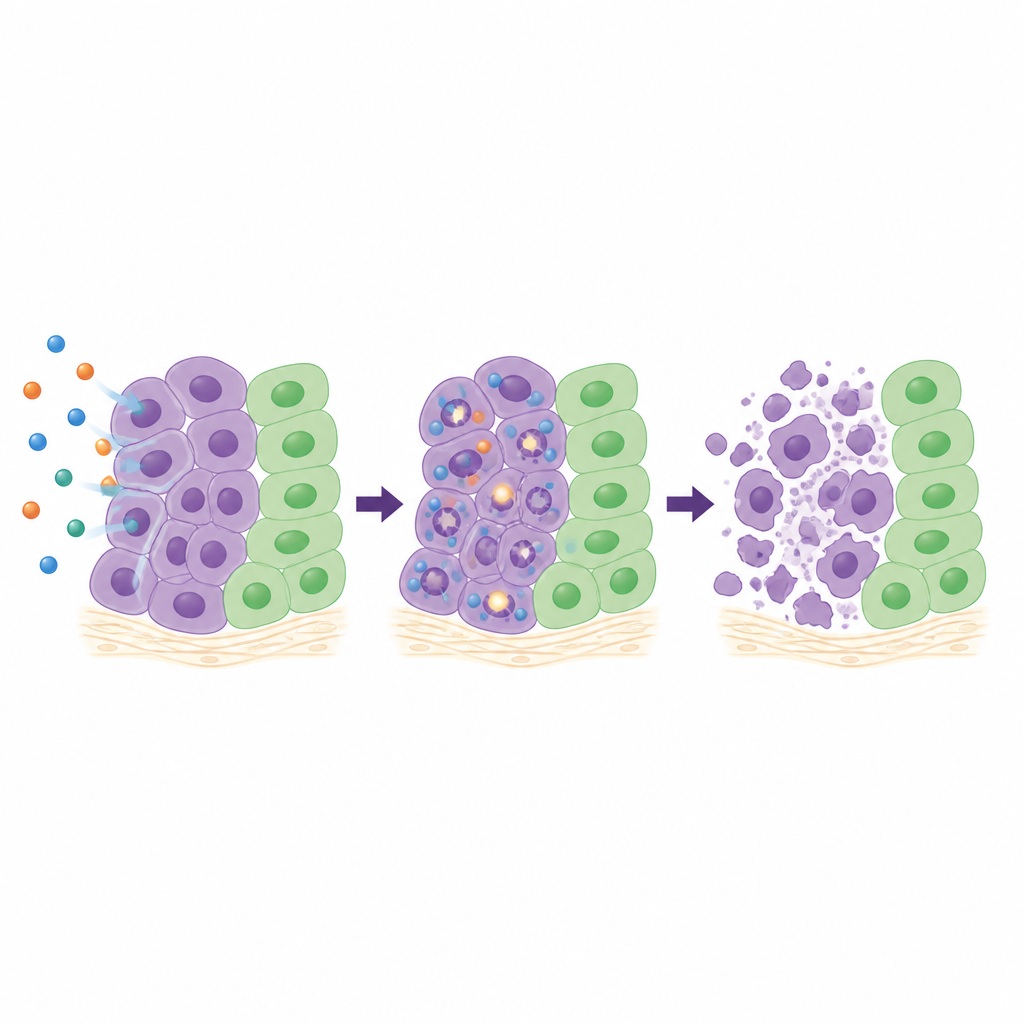
Wegwijzers uit metaalbinding en bloedtransport
Waarom zijn sommige thiosemicarbazonen actief terwijl andere dat niet zijn? Met behulp van kwantum‑chemische berekeningen toonden de auteurs aan dat de meest effectieve verbindingen elektronische structuren hebben die het vangen van metaalionen zoals ijzer of koper op specifieke atomen bevorderen. Dit vermogen om stevige “chelaat”complexen te vormen wordt verondersteld ten grondslag te liggen aan veel van hun biologische activiteit. Eén uitschieter, verbinding 27, gedraagt zich anders omdat zijn structuur dit soort metaalbinding belemmert, wat wijst op een alternatieve werkingswijze. Het team testte ook hoe gemakkelijk de zes sleutelverbindingen door darm‑achtige membranen zouden kunnen kruisen en hoe sterk ze binden aan humaan serumalbumine, het belangrijkste draagproteïne in het bloed. Alle hadden tamelijk slechte passieve darmpermeabiliteit, wat aangeeft dat formulering nodig zal zijn voor orale toediening. Verbinding 26 daarentegen bond sterk aan albumine, en computersimulaties lieten een stabiel netwerk van waterstofbruggen en hydrofobe contacten zien die helpen het te verankeren in een bekend geneesmiddelenbindingsplekje.
Wat dit betekent voor toekomstige geneesmiddelen
Samen genomen tonen de experimenten en simulaties aan dat één lid van deze moleculaire familie, verbinding 26, selectief kankercellen kan beschadigen door DNA‑breuken te veroorzaken en geprogrammeerde celdood te activeren, terwijl geteste normale cellen grotendeels onaangetast blijven. Tegelijkertijd tonen verwante moleculen activiteit tegen meerdere belangrijke parasieten. Hoewel hun huidige vorm niet ideaal is voor opname via de darm, maken hun eenvoudige structuren, duidelijke structuur‑activiteitrelaties en gedefinieerde interacties met bloedproteïnen ze aantrekkelijke bouwstenen voor toekomstig geneesmiddelenontwerp. Met betere afleveringssystemen en dierproeven zouden deze thiosemicarbazonen kunnen bijdragen aan nieuwe behandelopties voor zowel kanker als parasitaire ziekten.
Bronvermelding: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Trefwoorden: thiosemicarbazonen, antikankermiddelen, antiparasitaire verbindingen, DNA-schade, geneesmiddelenontwerp