Clear Sky Science · sv
Mångfacetterad biologisk och beräkningsbaserad bedömning av aromatiska och N‑heteroaromatiska icke‑substituerade thiosemikarbazoner
Varför dessa småmolekyler är viktiga
Cancer och parasitinfektioner förblir två av världens mest envisa hälsoproblem, och många befintliga läkemedel fungerar antingen inte tillräckligt bra eller ger starka biverkningar. Denna studie undersöker en familj relativt enkla, lättframställda molekyler kallade thiosemikarbazoner för att se om några av dem kan selektivt skada cancerceller och sjukdomsframkallande parasiter samtidigt som friska mänskliga celler skonas. Den undersöker också hur dessa molekyler beter sig i kroppen och hur de interagerar med blodproteiner, med både laboratorietester och datorbaserade simuleringar.
En kandidatbibliotek testas
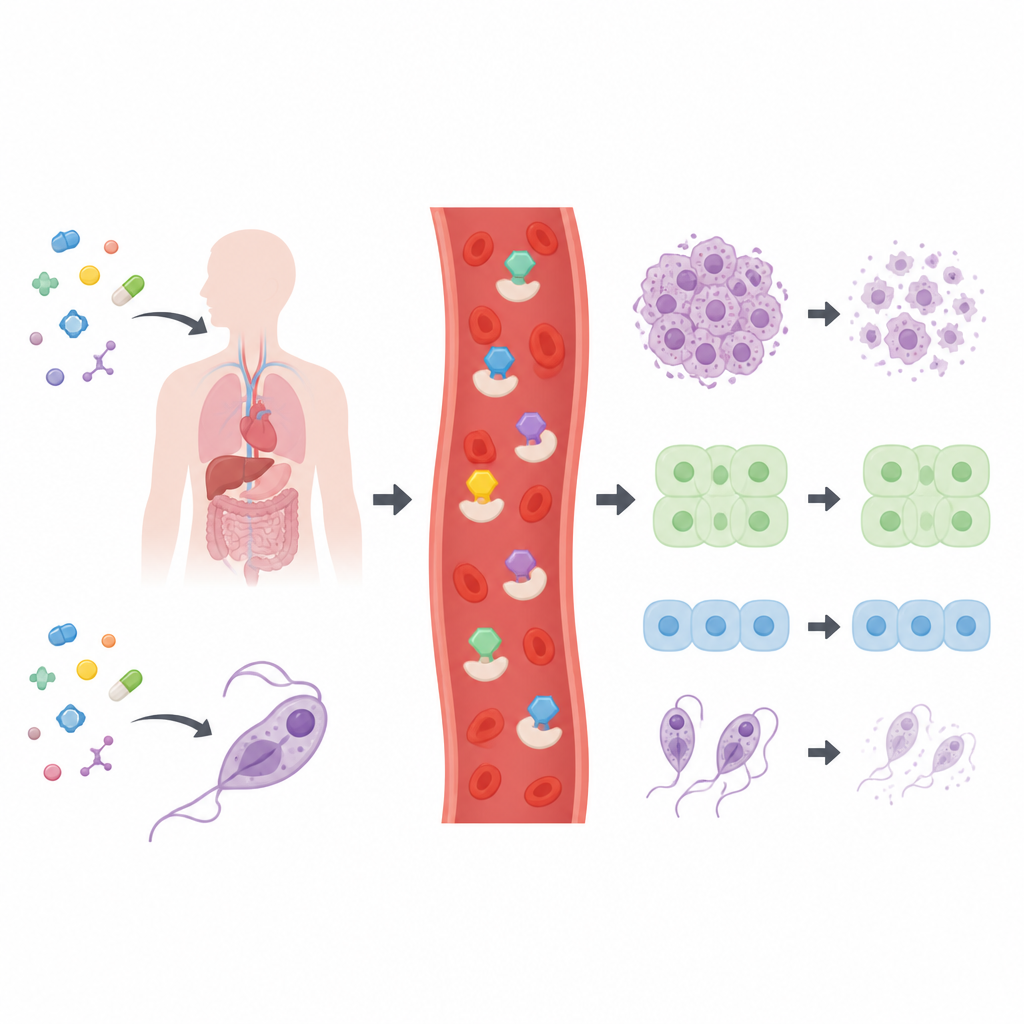
Forskarna skapade och karaktäriserade en uppsättning om 28 närbesläktade thiosemikarbazonföreningar, de flesta byggda kring ringsystem av kol som är välbekanta från många läkemedel. Innan de testade dem på celler kontrollerade de om molekylerna uppfyllde vanliga ”drug‑likeness”‑regler som används i läkemedelsforskning, vilka tar hänsyn till storlek, polaritet och flexibilitet. Alla föreningarna passerade dessa grundläggande filter, vilket tyder på att de är rimliga startpunkter för läkemedelsutveckling. Teamet exponerade därefter en bred panel av mänskliga cancercellinjer, två typer av normala mänskliga celler och fyra sjukdomsframkallande parasiter för föreningarna för att kartlägga vilka strukturer som var mest aktiva.
Identifiering av de mest lovande molekylerna
Majoriteten av biblioteket visade endast måttliga effekter, men sex molekyler utmärkte sig. Tre baserades på en pyridinkrans, en på en kinolinkrans och en på en indolkrans. Dessa toppkandidater saktade antingen ner eller dödade cancerceller vid låga koncentrationer och i flera fall verkade de också kraftfullt mot parasiter som orsakar Chagas‑sjukdom, afrikansk sömnsjuka och leishmanios. Den tydliga etta, märkt 26, var särskilt effektiv mot lung-, lever-, ben‑ och livmoderhalscancercellinjer samtidigt som den i praktiken inte visade någon toxicitet mot normala lung‑ och kolon‑celler. Den selektiviteten är avgörande eftersom den antyder ett fönster där tumörvävnad kan angripas utan motsvarande skada på frisk vävnad.
Hur ledande föreningen angriper cancerceller
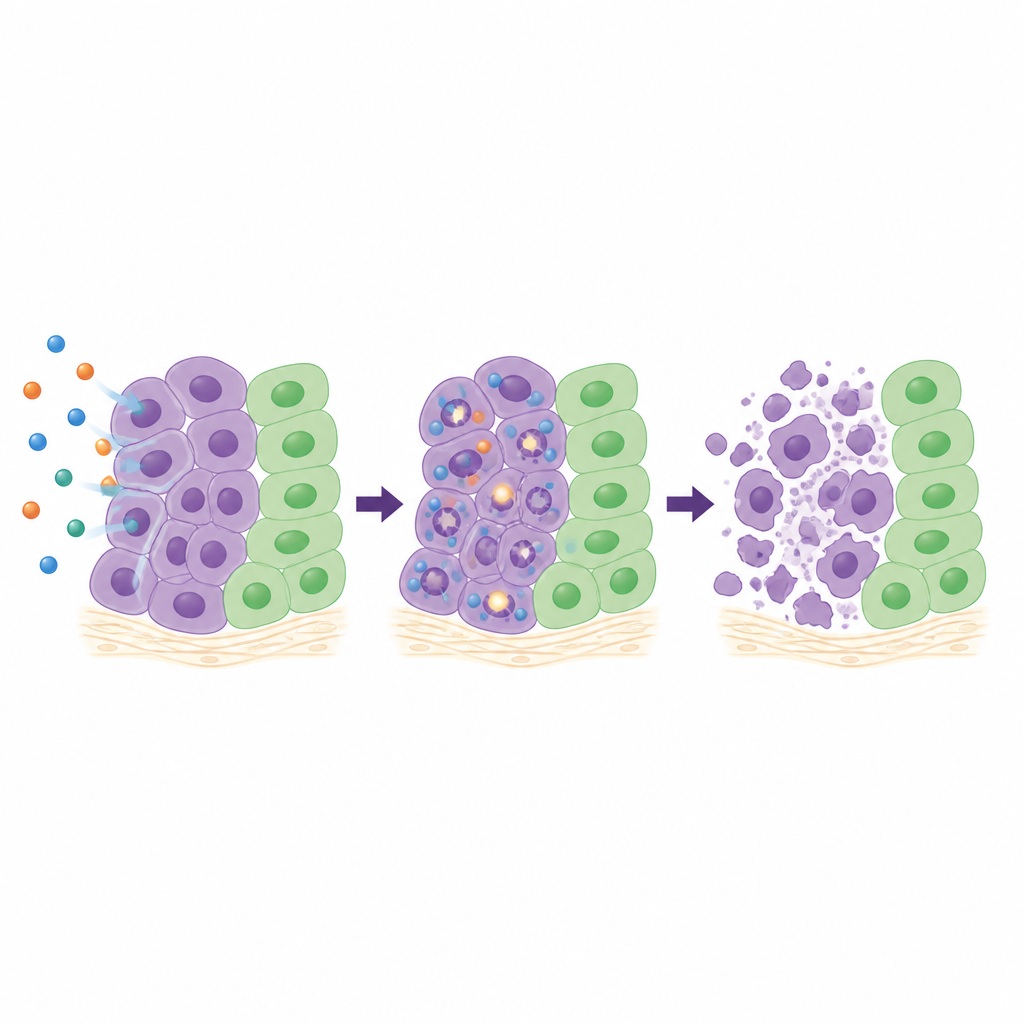
För att förstå vad 26 gör inne i cellerna undersökte teamet detaljerat fyra känsliga cancercellinjer. De följde hur cellerna fortskrider genom cellcykeln, mätte markörer för DNA‑brott och spårade aktivering av interna ”självdestrukts”‑enzymer. Beroende på celltyp bromsade 26 cellerna i olika skeden av deras tillväxtcykel, men i samtliga fall orsakade den ökande mängder DNA‑skador över tid och aktiverade kraftigt caspas‑3 och caspas‑7, nyckelkomponenter i programmerad celldöd. I tredimensionella kluster av lungceller, som bättre speglar verkliga tumörer än platta cellager, minskade 26 spheroidtillväxten kraftigt och krympte dem till och med vid högre doser. I en modell med kycklingäggs membran där humana tumörfragment växer med egen blodförsörjning minskade behandling med 26 tumörområdet med ungefär två tredjedelar utan synbar skada på omgivande vävnad.
Ledtrådar från metallbindning och blodtransport
Varför är vissa thiosemikarbazoner aktiva medan andra inte är det? Genom kvantkemiska beräkningar visade författarna att de mest effektiva föreningarna har elektroniska strukturer som gynnar att fånga metalljoner som järn eller koppar vid specifika atomer. Denna förmåga att bilda täta ”kelat”‑komplex tros ligga bakom mycket av deras biologiska aktivitet. En avvikare, förening 27, beter sig annorlunda eftersom dess struktur hindrar denna typ av metallbindning, vilket antyder en alternativ verkningsmekanism. Teamet testade också hur lätt de sex nyckelföreningarna kan korsa tarmliknande membran och hur starkt de binder till human serumalbumin, det viktigaste transportproteinet i blodet. Alla uppvisade ganska dålig passiv tarmpermeabilitet, vilket antyder att formuleringsarbete kommer att behövas för oral dosering. Förening 26, däremot, band starkt till albumin, och datorsimuleringar visade ett stabilt nätverk av vätebindningar och hydrofoba kontakter som hjälper till att förankra den i en känd läkemedelsbindande ficka.
Vad detta betyder för framtida läkemedel
Tillsammans visar experimenten och simuleringarna att en medlem av denna molekylfamilj, förening 26, kan selektivt skada cancerceller genom att orsaka DNA‑brott och utlösa kontrollerad celldöd, samtidigt som testade normala celler i huvudsak lämnas orörda. Samtidigt visar närbesläktade molekyler aktivitet mot flera viktiga parasiter. Även om deras nuvarande form inte är idealisk för upptag genom tarmen, gör deras enkla strukturer, tydliga struktur‑aktivitet‑relationer och väldefinierade interaktioner med blodproteiner dem till attraktiva byggstenar för framtida läkemedelsdesign. Med bättre leveranssystem och djurtester skulle dessa thiosemikarbazoner kunna bidra till nya behandlingar för både cancer och parasitära sjukdomar.
Citering: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Nyckelord: thiosemicarbazoner, anticancer‑medel, antiparasitiska föreningar, DNA‑skada, läkemedelsdesign