Clear Sky Science · ar
تقييم بيولوجي وحوسبي متعدد الجوانب للثيوسيميكاربازونات العطرية والن-هتيرو عطرية غير المستبدلة
لماذا تهم هذه الجزيئات الصغيرة
لا يزال السرطان والعدوى الطفيلية من أكثر مشاكل الصحة العامة إصراراً في العالم، والعديد من الأدوية الحالية إما لا تعمل بشكل كافٍ أو تسبب آثاراً جانبية قوية. تستعرض هذه الدراسة عائلة من الجزيئات البسيطة نسبياً وسهلة التصنيع تُدعى ثيوسيميكاربازونات للتحقق مما إذا كان بعضها يمكن أن يضرُّ خلايا السرطان والطفيليات الممرضة بشكل انتقائي مع حفاظه على الخلايا البشرية السليمة. كما تفحص كيف تتصرف هذه الجزيئات في الجسم وكيف تتفاعل مع بروتينات الدم، مستعينةً بالاختبارات المخبرية والمحاكاة الحاسوبية.
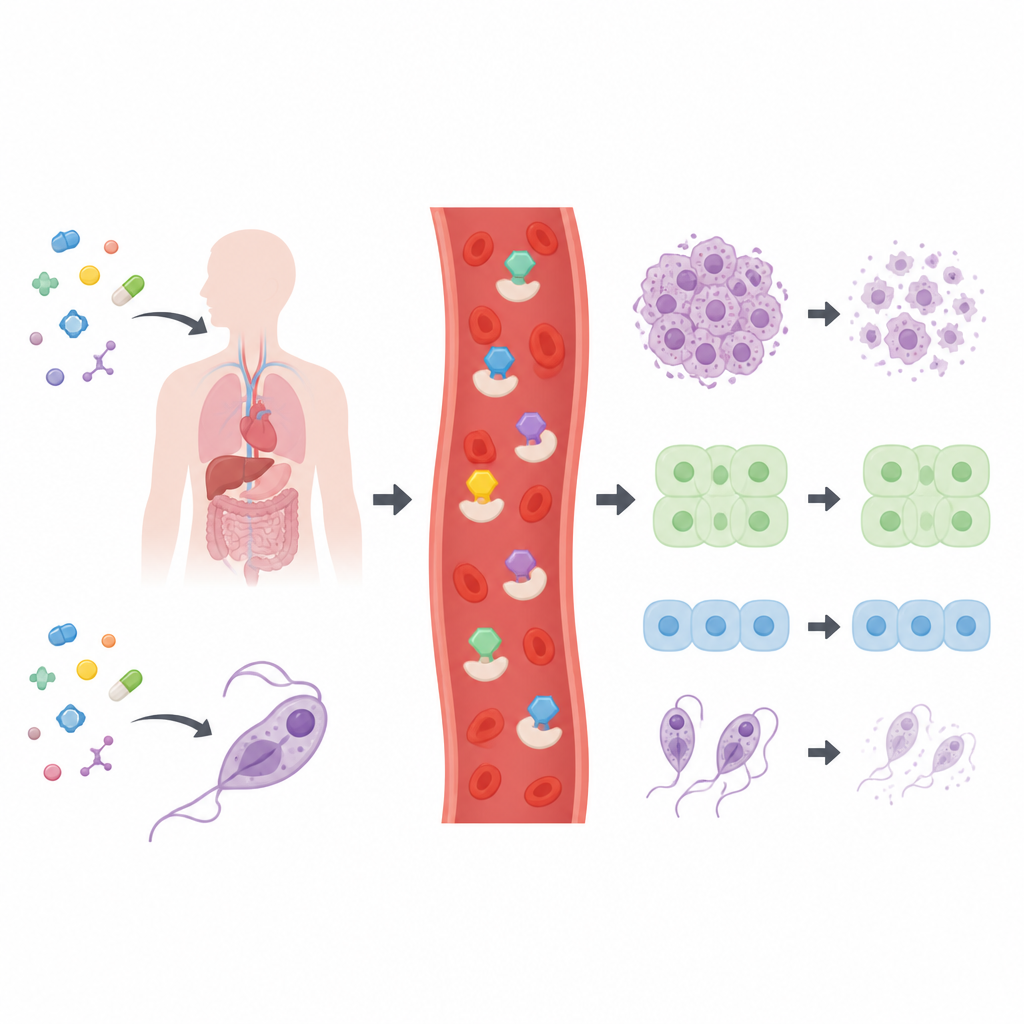
مكتبة من المرشحين قيد الاختبار
صنع الباحثون ووصفوا طيفاً مكوَّناً من 28 مركباً متعلقاً بالثيوسيميكاربازون، معظمها مبني على هياكل كربونية حلقية معروفة في كثير من الأدوية. قبل اختبارها على الخلايا، تحققوا مما إذا كانت الجزيئات تفي بقواعد “ملاءمة الدواء” الشائعة في بحوث الأدوية، التي تأخذ بعين الاعتبار الحجم والقطبية والمرونة. اجتازت جميع المركبات هذه المرشحات الأساسية، ما يشير إلى أنها نقاط انطلاق معقولة لتطوير الأدوية. ثم عرض الفريق مجموعة واسعة من خطوط خلايا السرطان البشرية، ونوعين من الخلايا البشرية الطبيعية، وأربع طفيليات ممرضة على المركبات لوضع خريطة للهياكل الأكثر نشاطاً.
تحديد الجزيئات الأكثر واعدة
أظهر معظم أفراد المكتبة تأثيرات معتدلة فقط، لكن ستة جزيئات برزت. ثلاثة منها كانت مبنية على حلقة البيريدين، واحد على حلقة الكينولين، وواحد على حلقة الإندول. كانت هذه المرشحات الرائدة تبطئ أو تقتل خلايا السرطان عند تراكيز منخفضة وفي عدة حالات أبدت نشاطاً قوياً ضد طفيليات تسبب داء شاغاس، ومرض النوم الأفريقي، والليشمينيات. المتقدم الواضح، المسمى 26، كان فعالاً بشكل خاص ضد خطوط خلايا سرطان الرئة والكبد والعظام وعنق الرحم بينما أظهر عملاً شبه معدومٍ ساماً تجاه خلايا الرئة والقولون الطبيعية. هذه الانتقائية حاسمة، لأنها تشير إلى نافذة يمكن فيها مهاجمة النسيج الورمي دون إلحاق ضرر مماثل بالأنسجة السليمة.
كيف يهاجم المركب الرائد خلايا السرطان
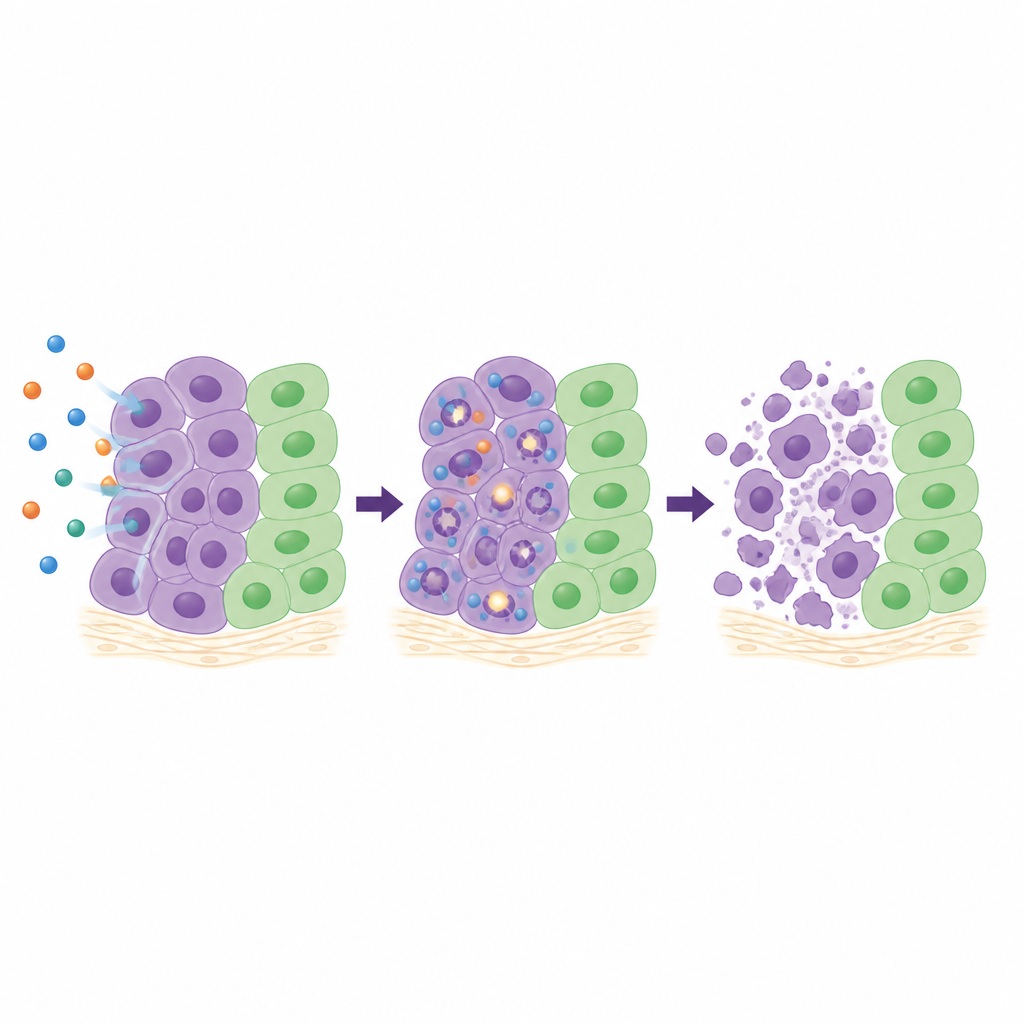
لفهم ما يفعله المركب 26 داخل الخلايا، نظر الفريق بتفصيل إلى أربعة خطوط سرطانية حساسة. تتبعوا تقدم الخلايا خلال دورة الخلية، وقيَّموا علامات انكسار الحمض النووي، ورصدوا تفعيل إنزيمات “الانتحار الخلوي” الداخلية. اعتماداً على نوع الخلية، أبطأ 26 الخلايا في مراحل مختلفة من دورة النمو، لكن في جميع الحالات تسبب بزيادة تدريجية في تلف الحمض النووي مع الزمن وفعل بقوة الكاسبيز-3 والكاسبيز-7، الفاعلان الرئيسيان في موت الخلايا المبرمج. في تجمعات ثلاثية الأبعاد لخلايا سرطان الرئة، التي تحاكي الأورام الحقيقية أفضل من طبقات الخلايا المسطحة، قلَّص 26 نمو الكريات الحبيبية بحدة وحتى تسبب في انكماشها عند جرعات أعلى. في نموذج غشاء بيضة دجاج حيث تنمو شظايا الأورام البشرية مع إمدادها الدموي الخاص، خفض العلاج بالمركب 26 مساحة الورم بنحو ثلثيها دون ضرر مرئي للأنسجة المحيطة.
دلائل من ربط المعادن ونقل الدم
لماذا تكون بعض الثيوسيميكاربازونات فعالة بينما لا يكون بعضها كذلك؟ باستخدام حسابات كميّة-كيميائية، أظهر المؤلفون أن المركبات الأكثر فعالية تملك هياكل إلكترونية تُفضّل احتجاز أيونات المعادن مثل الحديد أو النحاس عند ذرات معينة. يُعتقد أن هذه القدرة على تشكيل مركبات شيلات محكمة تفسّر الكثير من نشاطها البيولوجي. أحد المركبات المميزة، المركب 27، يتصرف بطريقة مختلفة لأن بنيته تمنع هذا النوع من ربط المعادن، مما يشير إلى نمط عمل بديل. اختبر الفريق أيضاً مدى سهولة عبور المركبات الستة الرئيسية لأغشية شبيهة بالأمعاء ومدى ارتباطها بألبومين المصل البشري، البروتين الحامل الرئيسي في الدم. كلها أظهرت نفاذية معوية سلبية نسبياً، مما يوحي بأن هناك حاجة للعمل على الصياغة للجرعات الفموية. مع ذلك ارتبط المركب 26 بقوة بالألبومين، وكشفت المحاكاة الحاسوبية عن مجموعة مستقرة من روابط الهيدروجين والتلامسات الكارهة للماء التي تساعد في تثبيته في جيب ربط دوائي معروف.
ما الذي يعنيه هذا للأدوية المستقبلية
تظهر التجارب والمحاكاة مجتمعة أن عضواً واحداً من هذه العائلة الجزيئية، المركب 26، يمكن أن يضر خلايا السرطان انتقائياً عبر التسبب في كسورٍ بالحمض النووي وتحفيز موت الخلايا المبرمج، بينما يترك الخلايا الطبيعية المختبرة إلى حد كبير دون ضرر. وفي الوقت نفسه، تُظهر جزيئات ذات صلة فعالية ضد عدة طفيليات مهمة. رغم أن شكلها الحالي ليس مثالياً للامتصاص المعوي، فإن هياكلها البسيطة، وعلاقات البنية-النشاط الواضحة، وتفاعلاتها المعرفة مع بروتينات الدم تجعلها لبنات بناء جذابة لتصميم أدوية مستقبلية. مع أنظمة توصيل أفضل واختبارات على الحيوانات، قد تسهم هذه الثيوسيميكاربازونات في علاج جديد لكل من السرطان والأمراض الطفيلية.
الاستشهاد: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
الكلمات المفتاحية: الثيوسيميكاربازونات, عوامل مضادة للسرطان, مركبات مضادة للطفيليات, تلف الحمض النووي, تصميم الأدوية