Clear Sky Science · fr
Évaluation biologique et computationnelle multifacette de thiosemicarbazones aromatiques et N‑hétéroaromatiques non substitués
Pourquoi ces petites molécules sont importantes
Le cancer et les infections parasitaires restent deux des problèmes de santé les plus tenaces au monde, et de nombreux médicaments existants sont soit insuffisamment efficaces, soit responsables d’effets secondaires importants. Cette étude examine une famille de molécules relativement simples et faciles à synthétiser, appelées thiosemicarbazones, pour déterminer si certaines d’entre elles peuvent endommager sélectivement les cellules cancéreuses et les parasites pathogènes tout en épargnant les cellules humaines saines. Elle analyse également leur comportement dans l’organisme et leurs interactions avec les protéines sanguines, en combinant tests de laboratoire et simulations informatiques.
Une bibliothèque de candidats mise à l’épreuve
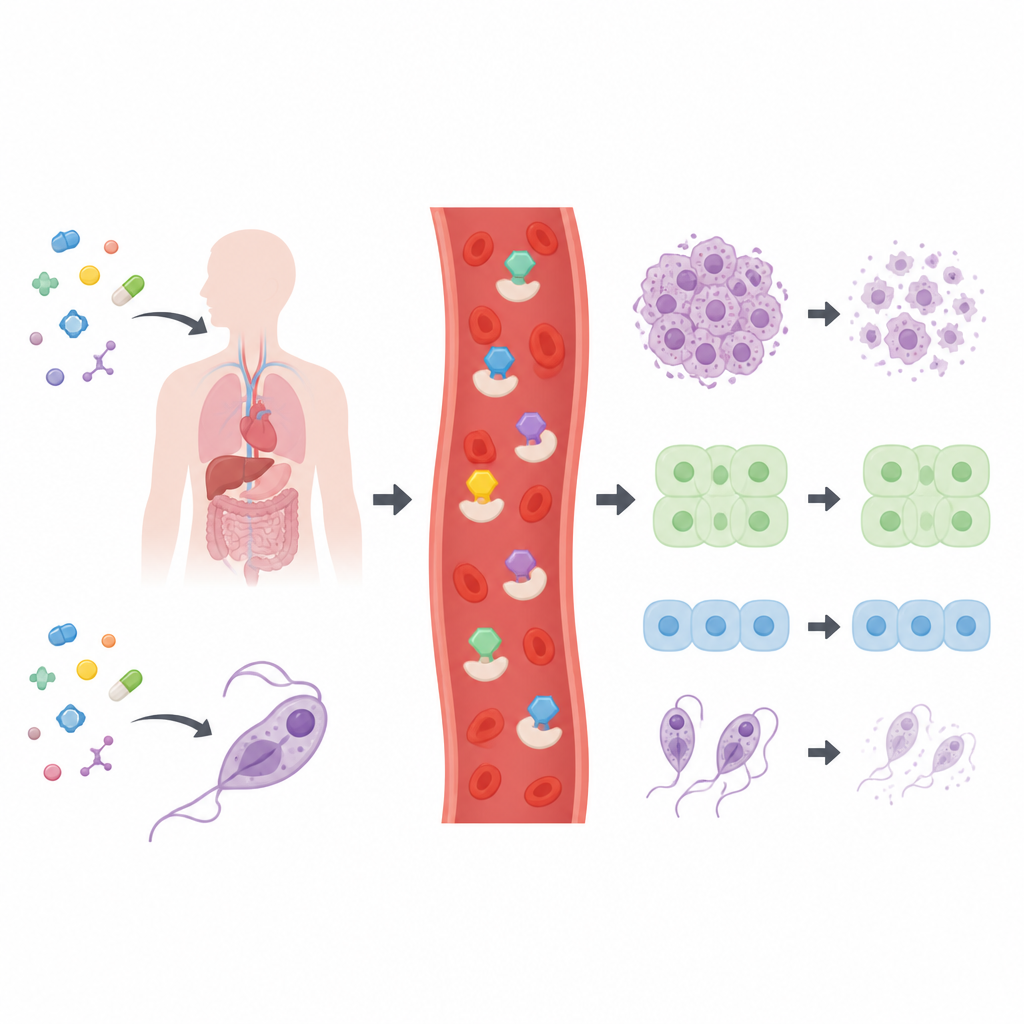
Les chercheurs ont synthétisé et caractérisé un ensemble de 28 thiosemicarbazones apparentés, pour la plupart centrés sur des systèmes carbonés cycliques couramment retrouvés en pharmacologie. Avant de les tester sur des cellules, ils ont vérifié si ces molécules respectaient les règles usuelles de « drug‑likeness » utilisées en recherche pharmaceutique, qui tiennent compte de la taille, de la polarité et de la flexibilité. Tous les composés ont franchi ces filtres de base, ce qui suggère qu’ils constituent des points de départ raisonnables pour le développement de médicaments. L’équipe a ensuite exposé un large panel de lignées cellulaires cancéreuses humaines, deux types de cellules humaines normales et quatre parasites pathogènes aux composés afin de cartographier quelles structures étaient les plus actives.
Identifier les molécules les plus prometteuses
La plupart de la bibliothèque n’a montré que des effets modestes, mais six molécules se sont distinguées. Trois étaient basées sur un noyau pyridine, une sur un noyau quinoline et une sur un noyau indole. Ces candidats principaux ralentissaient ou tuaient les cellules cancéreuses à faibles concentrations et, dans plusieurs cas, étaient également très actifs contre des parasites responsables de la maladie de Chagas, du sommeil africain et de la leishmaniose. Le grand favori, désigné 26, était particulièrement efficace contre des lignées de cancer du poumon, du foie, des os et du col de l’utérus tout en ne montrant pratiquement aucune toxicité envers des cellules normales de poumon et de côlon. Cette sélectivité est cruciale car elle suggère une fenêtre therapeutique permettant d’attaquer le tissu tumoral sans causer de dommages comparables aux tissus sains.
Comment le composé principal attaque les cellules cancéreuses
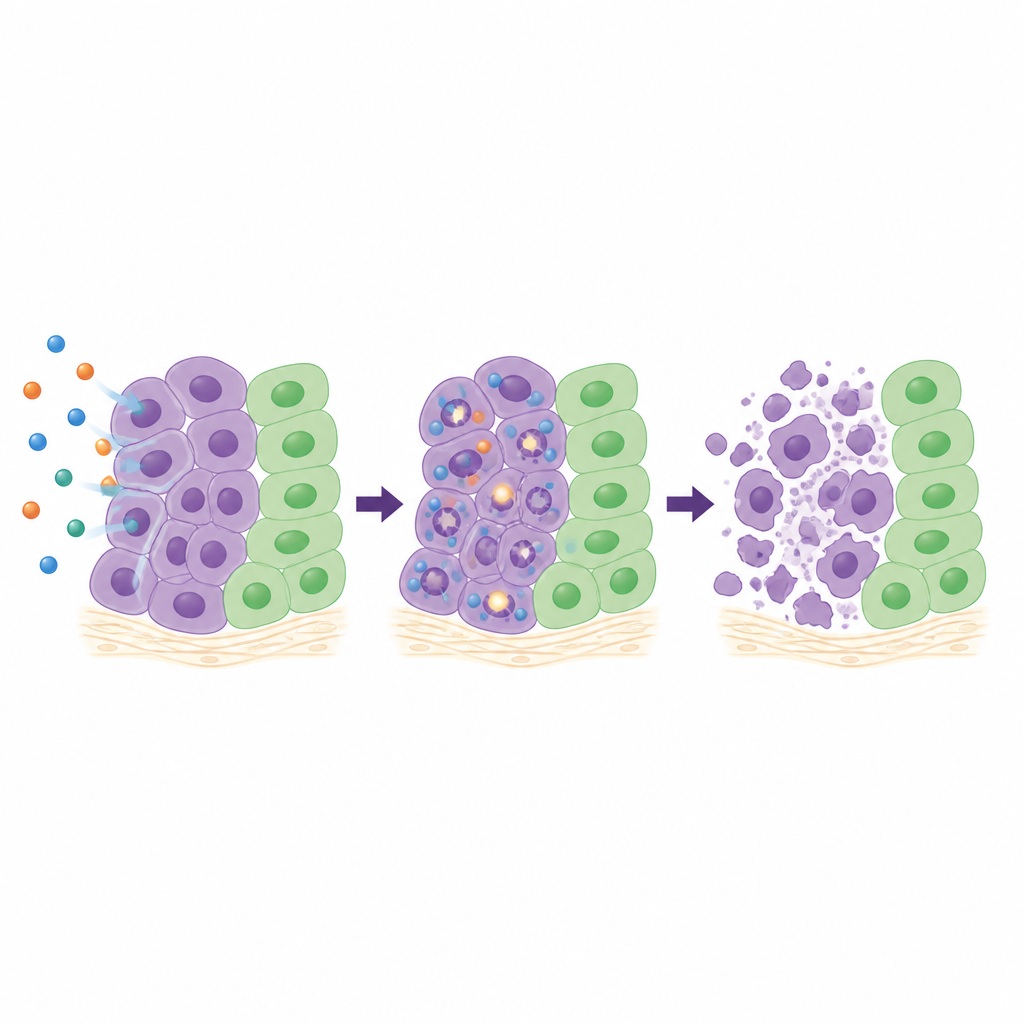
Pour comprendre l’action du composé 26 à l’intérieur des cellules, l’équipe a étudié en détail quatre lignées cancéreuses sensibles. Ils ont suivi la progression du cycle cellulaire, mesuré des marqueurs de cassures de l’ADN et observé l’activation d’enzymes internes de « autodestruction ». Selon le type cellulaire, le composé 26 a ralenti les cellules à différentes étapes du cycle de croissance, mais dans tous les cas il a provoqué une augmentation progressive des dommages à l’ADN et a fortement activé la caspase‑3 et la caspase‑7, acteurs clés de la mort cellulaire programmée. Dans des amas tridimensionnels de cellules pulmonaires, qui reproduisent mieux les tumeurs réelles que des couches cellulaires plates, le composé 26 a nettement réduit la croissance des sphéroïdes et les a même réduits à des doses plus élevées. Dans un modèle de membrane d’œuf de poule où des fragments tumoraux humains se développent avec leur propre vascularisation, le traitement par le composé 26 a réduit la surface tumorale d’environ deux tiers sans dommages visibles aux tissus environnants.
Indices fournis par la liaison aux métaux et le transport sanguin
Pourquoi certains thiosemicarbazones sont‑ils actifs tandis que d’autres ne le sont pas ? Grâce à des calculs quantico‑chimiques, les auteurs montrent que les composés les plus efficaces possèdent des structures électroniques favorisant la complexation d’ions métalliques tels que le fer ou le cuivre sur des atomes spécifiques. Cette capacité à former des complexes chélatés serrés est considérée comme à l’origine d’une grande partie de leur activité biologique. Un composé particulier, le 27, se comporte différemment car sa structure empêche ce type de liaison aux métaux, ce qui suggère un mode d’action alternatif. L’équipe a également testé la perméabilité passive au travers de membranes de type intestinal et l’affinité des six composés clés pour l’albumine sérique humaine, la principale protéine porteuse dans le sang. Tous présentaient une perméabilité intestinale passive plutôt faible, ce qui laisse entendre qu’un travail de formulation sera nécessaire pour l’administration orale. Le composé 26, en revanche, se lie fortement à l’albumine, et les simulations informatiques ont révélé un ensemble stable de liaisons hydrogène et d’interactions hydrophobes qui aident à l’ancrer dans une poche de fixation aux médicaments connue.
Ce que cela signifie pour les médicaments futurs
Pris ensemble, les expériences et les simulations montrent qu’un membre de cette famille moléculaire, le composé 26, peut endommager sélectivement les cellules cancéreuses en provoquant des cassures de l’ADN et en déclenchant la mort cellulaire programmée, tout en laissant les cellules normales testées largement indemnes. Parallèlement, des molécules apparentées présentent une activité contre plusieurs parasites importants. Bien que leur forme actuelle ne soit pas idéale pour l’absorption intestinale, leurs structures simples, les relations claires structure‑activité et leurs interactions définies avec les protéines sanguines en font des briques attrayantes pour la conception de futurs médicaments. Avec de meilleurs systèmes d’administration et des essais sur des modèles animaux, ces thiosemicarbazones pourraient contribuer à de nouveaux traitements contre le cancer et les maladies parasitaires.
Citation: Macijewska, N., Ristić, P., Kallingal, A. et al. Multifaceted biological and computational assessment of aromatic and N-heteroaromatic non-substituted thiosemicarbazones. Sci Rep 16, 14911 (2026). https://doi.org/10.1038/s41598-026-44568-4
Mots-clés: thiosemicarbazones, agents anticancéreux, composés antiparasitaires, lésions de l’ADN, conception de médicaments