Clear Sky Science · tr
ASCC3 kolorektal kanser hücrelerinde kemoterapötik duyarlılığı artırır
Bu araştırma neden önemli
Kemoterapi ileri düzey kolorektal kanser için temel bir tedavi olmakla birlikte, birçok tümör zamanla bu sert ilaçlara karşı hayatta kalmayı öğrenir. Bu çalışma ASCC3 adlı daha az bilinen bir proteini inceliyor ve beklenmedik biçimde ASCC3’ün kolorektal kanser hücrelerini yaygın kemoterapi ilaçlarına karşı daha hassas hâle getirdiğini ortaya koyuyor. ASCC3’ün DNA hasarını, hücre metabolizmasını ve hücre içi stres sinyallerini nasıl bağladığını açığa çıkararak, hangi hastaların tedaviye yanıt vereceğini öngörmeye ve dirençli tümörlerin nasıl etkisiz hâle getirilebileceğine dair olası yeni yolları işaret ediyor.
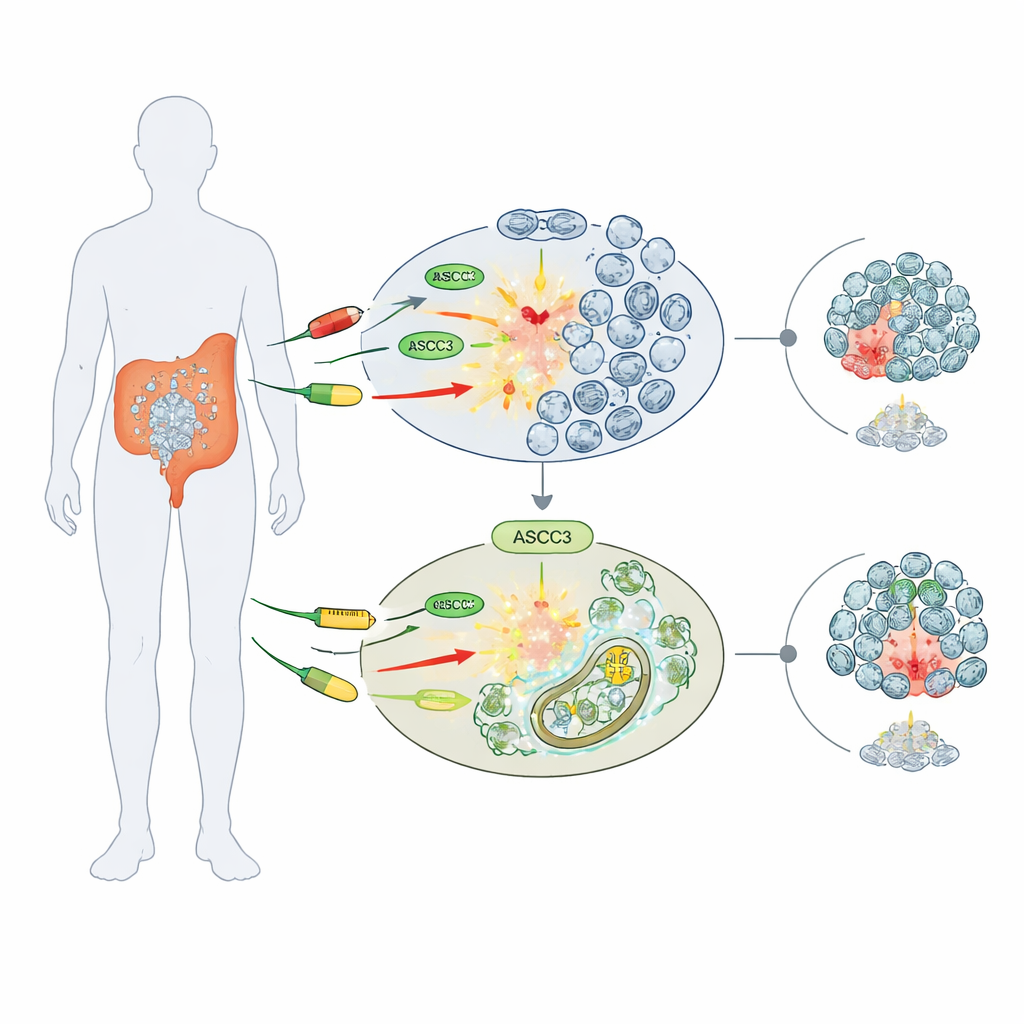
İlaç hassasiyeti için bir kapı bekçisi
Araştırmacılar DNA’yı zarar veren veya üretimini engelleyen üç yaygın kemoterapi ilacına odaklandı: 5-florourasil (5-FU), sisplatin ve hidroksiüre. Birkaç insan kolorektal kanser hücre hattı ile çalışarak, normal hücreleri ASCC3 geninden yoksun olarak genetik olarak düzenlenmiş hücrelerle karşılaştırdılar. İlginç bir şekilde, ASCC3 olmayan hücreler bu ilaçlarda daha iyi hayatta kaldı; daha fazla koloni oluşturdular ve normal hücrelere göre daha yüksek viabilite korudular. Bu "kemorezistans" etkisi özgündü: kemik kanseri (osteosarkom) hücrelerinde ASCC3’ün kaldırılması ilaç duyarlılığını değiştirmedi, bu da rolünün kanser türüne bağlı olduğunu düşündürdü.
Daha fazla DNA hasarı, fakat daha fazla hayatta kalma
İlk bakışta, ASCC3 eksik hücrelerin artmış hayatta kalması paradoksal görünüyor. Önceki çalışmalar ASCC3’ün hücrelerin tıkanmış DNA replikasyonuyla başa çıkmasına, kırık kromozomları önlemeye yardımcı olduğunu göstermişti. Bu çalışmada, kolorektal kanser hücreleri kemoterapi ile muamele edildiğinde, ASCC3 kaybı daha fazla DNA hasarı belirtisine yol açtı—hasarlı DNA’nın parlak nükleer odakları ve mikronükleus adı verilen ekstra kromozom parçaları. Başka bir deyişle, hücreler genetik olarak daha az kararlıydı, ancak öldürülmesi daha zordu. Bu uyumsuzluk, basit DNA tamirinin ötesinde diğer koruyucu yolların hasarlı hücrelerin varlığını sürdürmesine izin verdiğini düşündürdü.
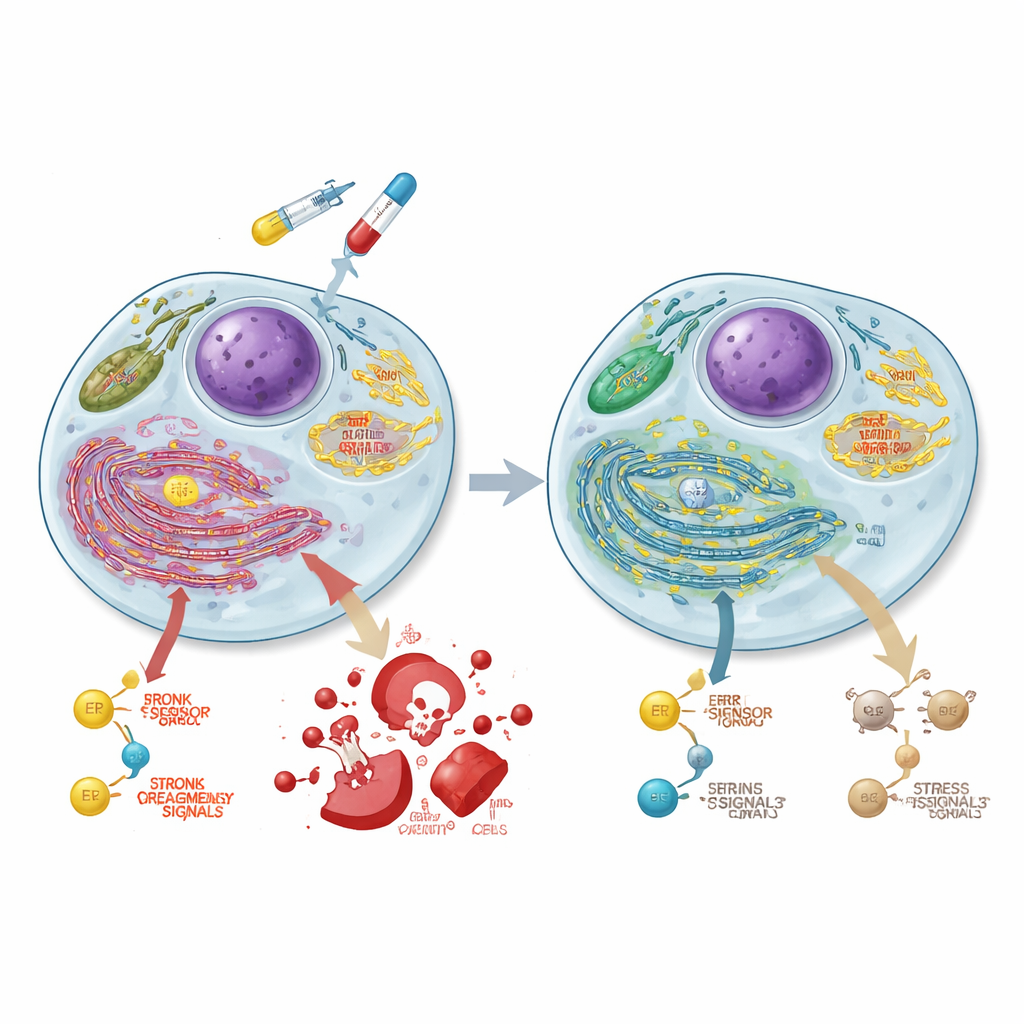
Kanser hücrelerinin enerji üretim biçimini yeniden kablajlama
ASCC3 kaybolduğunda başka nelerin değiştiğini anlamak için ekip tüm genom boyunca gen aktivitesini ölçtü. ASCC3’ün normalde glikoz parçalanmasıyla (glikoliz) ilgili gen kümelerini, büyüme ile ilişkili bir sinyal merkezi olan mTORC1’i ve hücre içindeki endoplazmik retikulumda protein katlanma yollarını desteklediğini buldular. Uzman metabolik testler kullanarak, ASCC3 eksik hücrelerin glikolizden uzaklaşıp bunun yerine hücrenin enerji santralleri olan mitokondrilere ağırlık verdiğini, oksijen bazlı enerji üretimini artırdığını gösterdiler. İşaretlenmiş glikozla yapılan izleyici deneyleri, bu hücrelerin şekeri trikarboksilik asit (TCA) döngüsüne ve ilişkili aminoasitlere daha fazla kanalize ettiğini, oysa alanin ve serin gibi bazı yapı taşları için kullanımını azalttığını doğruladı. ASCC3 ayrıca hücrenin serini sıfırdan sentezleme yeteneğini ve bu aminoasit kıt olduğunda büyümeyi destekledi; bununla birlikte kesin mekanizmalar hücre hatları arasında değişiklik gösteriyordu.
Kendini yok etmeye yönelik bir stres sinyalini kırpma
Endoplazmik retikulum (ER) proteinlerin doğru katlanıp katlanmadığını izler; aşırı yüklendiğinde, hücrelerin uyum sağlamasına yardımcı olabilecek veya onları ölüme zorlayabilecek stres yanıtlarını tetikler. Önemli bir ER sensörü olan PERK nihayetinde CHOP ve kaspaz 3 gibi proteinleri içeren pro-ölüm programını etkinleştirebilir. Araştırmacılar ASCC3’ün kolorektal kanser hücrelerinde ER stresi sırasında PERK proteinini biriktirmek için gerekli olduğunu buldular; oysa bu durum PERK’in gen transkriptini veya yıkım hızını değiştirmiyordu. Hücreler 5-FU ile muamele edildiğinde, normal hücrelerde zaman içinde PERK, CHOP ve aktif kaspaz 3’te güçlü artışlar görüldü; bu, kemoterapi kaynaklı hücre ölümüne uygundu. Buna karşın, ASCC3 eksik hücreler bu proteinleri tam olarak indükleyemedi ve ölüm yanıtları belirgin şekilde azaldı; bu da daha ağır DNA hasarına rağmen neden kemorezistans gösterdiklerini açıklamaya yardımcı oluyor.
Hastalar için anlamı
Bir araya getirildiğinde, çalışma ASCC3’ü kolorektal kanser hücrelerinde kemoterapinin içsel bir müttefiki olarak resmediyor. ASCC3 bulunduğunda, hücre daha çok glikoliz odaklı bir metabolizmayı, sağlam serin üretimini ve hasarlı hücreleri öz-öldürmeye itebilecek PERK aracılı güçlü bir ER stres sinyalini destekliyor. ASCC3 kaybolduğunda ise hücreler daha fazla genetik hasar biriktiriyor ama enerji üretimini mitokondrilere kaydırıp PERK–CHOP ölüm yolunu köreltmek suretiyle hayatta kalıyor. Bu bulgular ASCC3 düzeylerinin hangi kolorektal tümörlerin 5-FU ve oksaliplatin gibi ilaçlara iyi yanıt vereceğini öngörmede yardımcı olabileceğini ve ASCC3 düşük tümörlerin değişmiş metabolizmasını veya stres yanıtlarını hedeflemenin kemorezistansı aşmak için yeni stratejiler sunabileceğini düşündürüyor.
Atıf: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Anahtar kelimeler: kolorektal kanser, kemorezistans, hücre metabolizması, ER stresi, PERK sinyal iletimi