Clear Sky Science · ar
ASCC3 يعزز التحسس الكيميائي في خلايا سرطان القولون والمستقيم
لماذا يهم هذا البحث
تعد المعالجة الكيميائية علاجاً أساسياً لسرطان القولون والمستقيم المتقدم، لكن العديد من الأورام يتعلم في نهاية المطاف كيفية النجاة من هذه الأدوية القاسية. يستكشف هذا العمل بروتينًا أقل شهرة يسمى ASCC3 ويكشف أنه بشكل غير متوقع يجعل خلايا سرطان القولون والمستقيم أكثر عرضة للأدوية الكيميائية الشائعة. من خلال الكشف عن كيفية ربط ASCC3 بين تلف الحمض النووي، واستقلاب الخلية، وإشارات الإجهاد داخل الخلية، يشير العمل إلى طرق محتملة جديدة للتنبؤ بمن سيستجيب للعلاج—وكيف يمكن تحييد الأورام المقاومة.
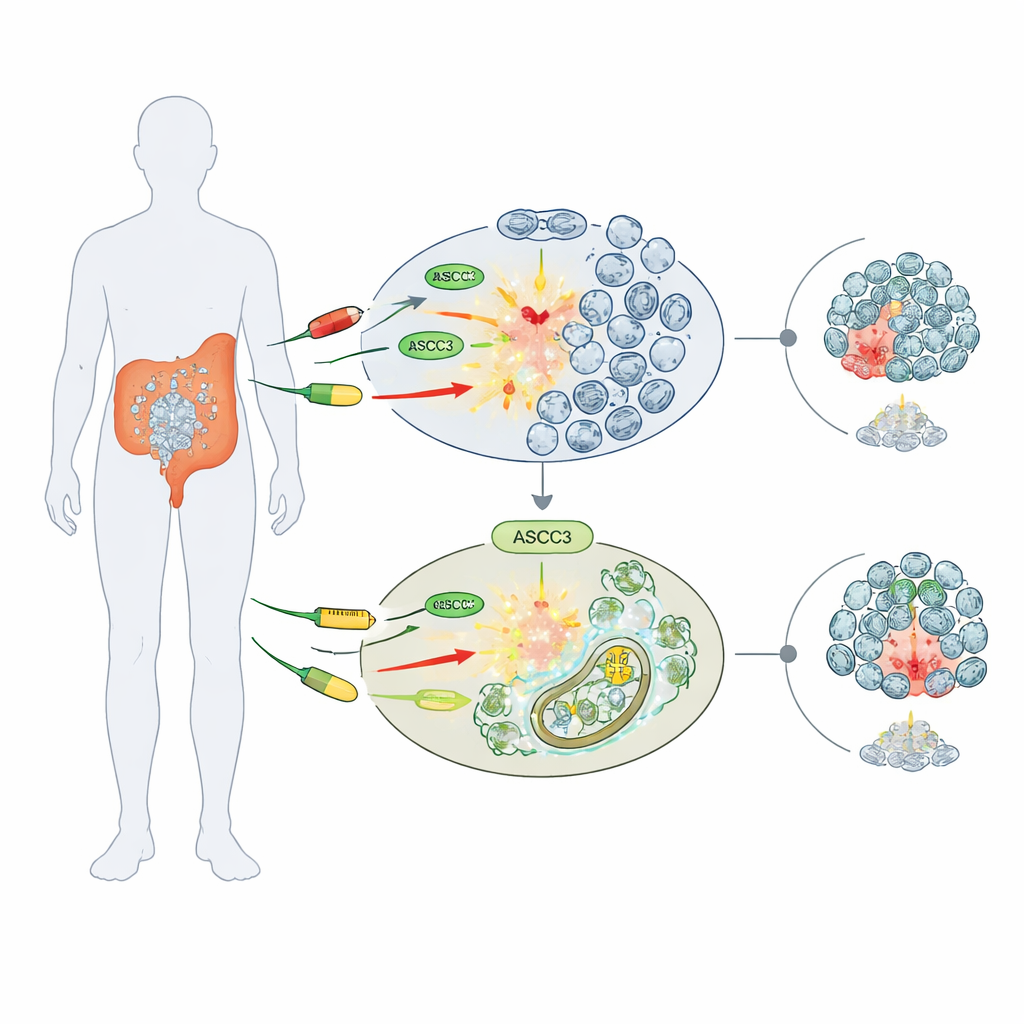
حارس لباب حساسية الدواء
ركز الباحثون على ثلاثة عوامل كيميائية مستخدمة على نطاق واسع تسبب تلفًا في الحمض النووي أو تعيق تصنيعه: 5-فلورويوراسيل (5-FU)، سيسبلاتين، وهيدروكسي يوريا. بالعمل مع عدة سلاسل خلوية بشرية لسرطان القولون والمستقيم، قارنوا الخلايا الطبيعية بخلايا محرّفة وراثيًا لفقدان ASCC3. وللمفاجأة، نجت الخلايا الخالية من ASCC3 من هذه الأدوية بشكل أفضل، حيث شكلت مستعمرات أكثر واحتفظت بقدرة بقاء أعلى من نظيراتها الطبيعية. كان هذا التأثير المتمثل في «مقاومة كيميائية» محددًا: في خلايا سرطان العظام (أوستيوساركوما)، لم يغير إزالة ASCC3 حساسية الدواء، ما يشير إلى أن دوره يعتمد على نوع السرطان.
مزيد من تلف الحمض النووي، ومع ذلك مزيد من البقاء
للوهلة الأولى، يبدو تحسن بقاء الخلايا الخالية من ASCC3 متناقضًا. أظهرت أعمال سابقة أن ASCC3 يساعد الخلايا على التعامل مع تعثر تضاعف الحمض النووي، مانعًا انكسار الكروموسومات. في هذه الدراسة، عندما عُولجت خلايا سرطان القولون والمستقيم بالعلاج الكيميائي، أدى فقدان ASCC3 إلى مزيد من علامات تلف الحمض النووي—بؤر نووية ساطعة للحمض النووي المتضرر وقطع إضافية من الكروموسومات تسمى النوى الدقيقة. بكلمات أخرى، كانت الخلايا أقل استقرارًا جينيًا، ومع ذلك كانت أصعب في القتل. يشير هذا الانفصال إلى أن مسارات حماية أخرى، تتجاوز إصلاح الحمض النووي البسيط، سمحت للخلايا المتضررة بالاستمرار.
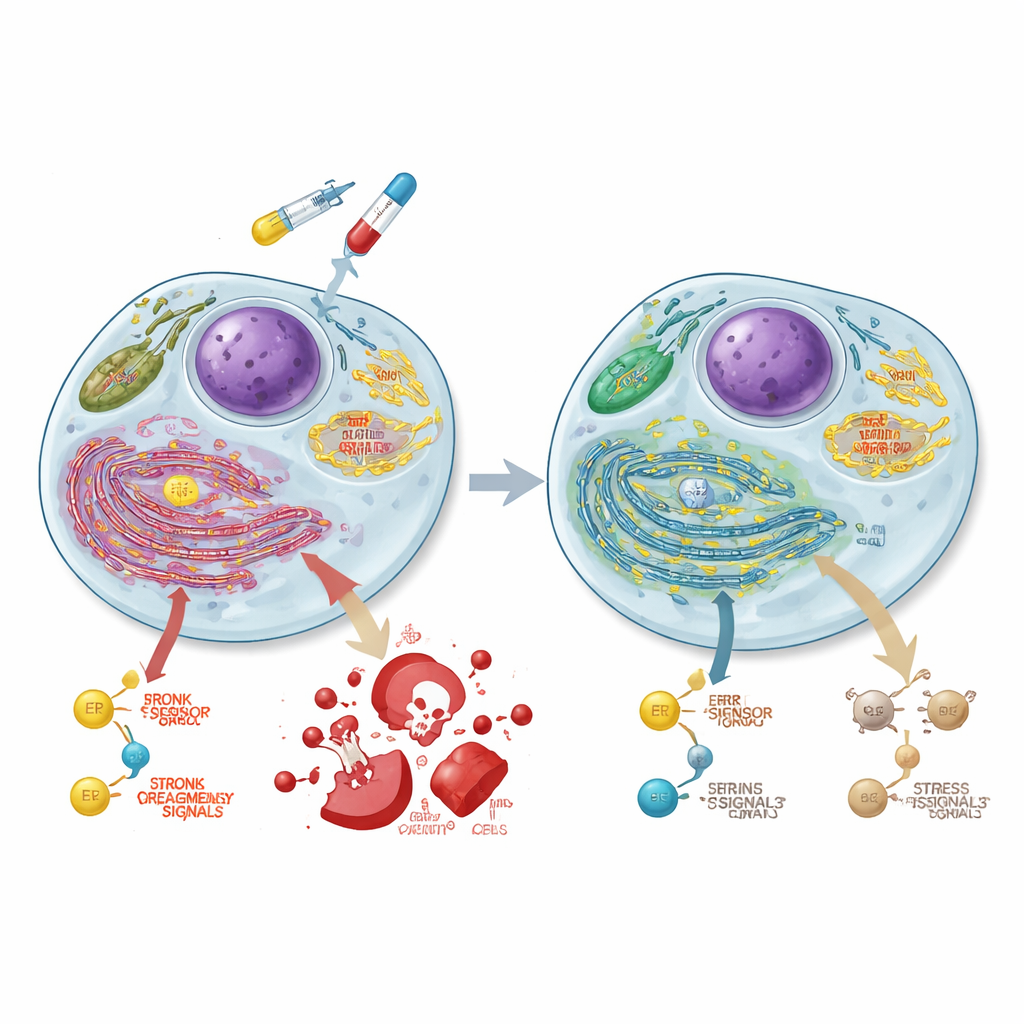
إعادة توصيل كيفية إنتاج الخلايا للطاقة
لفهم ما يتغير أيضًا عند فقدان ASCC3، قاس الفريق نشاط الجينات عبر الجينوم بأكمله. وجدوا أن ASCC3 يعزّز عادة مجموعات من الجينات المشاركة في تكسير السكر (التحلل السكري)، ومحور إشارة مرتبط بالنمو يسمى mTORC1، ومسارات طي البروتينات في الشبكة الإندوبلازمية. باستخدام اختبارات استقلابية متخصصة، أظهروا أن الخلايا التي تفتقر إلى ASCC3 تحولت بعيدًا عن التحلل السكري واعتمدت بدلًا من ذلك بشكل كبير على الميتوكوندريا—محطات طاقة الخلية—مما زاد إنتاج الطاقة القائم على الأكسجين. أكدت تجارب التتبع باستخدام جلوكوز معنّن أن هذه الخلايا وجهت مزيدًا من السكر إلى دورة حمض الريبوتريك الثلاثي الكربوكسيل (TCA) والأحماض الأمينية المرتبطة بها، مع تقليل استخدامه لبعض اللبنات مثل الألانين والسيرين. دعم ASCC3 أيضًا قدرة الخلية على تصنيع السيرين ذاتيًا والنمو عندما يكون هذا الحمض الأميني نادرًا، رغم أن الآليات الدقيقة اختلفت بين سلالات الخلايا.
تخفيف إشارة إجهاد ذاتي التدمير
تراقب الشبكة الإندوبلازمية ما إذا كانت البروتينات مطوية بشكل صحيح؛ عند حدوث حمل زائد، تطلق استجابات إجهاد يمكن أن تساعد الخلايا على التكيف أو تدفعها نحو الموت. أحد مجسات الشبكة الإندوبلازمية الرئيسية، PERK، يمكنه في نهاية المطاف تفعيل برنامج مميت يشمل البروتينات CHOP وكاسبيز-3. وجد الباحثون أن ASCC3 ضروري لتراكم بروتين PERK أثناء إجهاد الشبكة الإندوبلازمية في خلايا سرطان القولون والمستقيم، رغم أنه لا يغير نسخة جين PERK أو معدل تفككه. عند علاج الخلايا بـ5-FU، أظهرت الخلايا الطبيعية زيادات قوية مع الزمن في PERK وCHOP وكاسبيز-3 النشط، متسقة مع موت الخلايا الناتج عن العلاج الكيميائي. بالمقابل، فشلت الخلايا الخالية من ASCC3 في تحفيز هذه البروتينات بالكامل، وكانت استجابتهم للوفاة منخفضة بشكل ملحوظ، ما يساعد على تفسير مقاومتهم الكيميائية رغم زيادة تلف الحمض النووي.
ماذا يعني هذا للمرضى
بالجمع بين النتائج، يرسم البحث صورة ASCC3 كنوع من الحليف الداخلي للعلاج الكيميائي في خلايا سرطان القولون والمستقيم. عندما يكون ASCC3 حاضرًا، يدعم استقلابًا يركز أكثر على التحلل السكري، وإنتاجًا قويًا للسيرين، وإشارة إجهاد شبكية قوية عبر PERK يمكن أن تدفع الخلايا المتضررة نحو التدمير الذاتي. عندما يُفقد ASCC3، تتراكم الخلايا مزيدًا من الضرر الجيني لكنها تبقى على قيد الحياة عن طريق تحويل إنتاج الطاقة نحو الميتوكوندريا وتخفيف مسار الموت PERK–CHOP. تشير هذه الرؤى إلى أن مستويات ASCC3 قد تساعد في التنبؤ أي أورام القولون والمستقيم ستستجيب جيدًا لأدوية مثل 5-FU وأوكساليبلاتين، وأن استهداف الاستقلاب أو استجابات الإجهاد المتغيرة في الأورام الفقيرة بـASCC3 قد يوفر استراتيجيات جديدة للتغلب على المقاومة الكيميائية.
الاستشهاد: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
الكلمات المفتاحية: سرطان القولون والمستقيم, مقاومة الأدوية الكيميائية, استقلاب الخلايا, إجهاد الشبكة الإندوبلازمية, إشارة PERK