Clear Sky Science · de
ASCC3 fördert Chemosensitivität in Kolorektalkrebszellen
Warum diese Forschung wichtig ist
Chemotherapie ist eine Standardbehandlung bei fortgeschrittenem kolorektalem Krebs, doch viele Tumoren lernen im Laufe der Zeit, diesen harten Wirkstoffen zu widerstehen. Diese Studie untersucht ein weniger gut bekanntes Protein namens ASCC3 und zeigt überraschend, dass es kolorektale Krebszellen empfindlicher gegenüber gängigen Chemotherapeutika macht. Indem beschrieben wird, wie ASCC3 DNA-Schäden, zellulären Stoffwechsel und Stresssignale innerhalb der Zelle verknüpft, weist die Arbeit auf mögliche neue Wege hin, vorherzusagen, welche Patientinnen und Patienten auf eine Behandlung ansprechen — und wie resistente Tumoren womöglich gezielt geschwächt werden können.
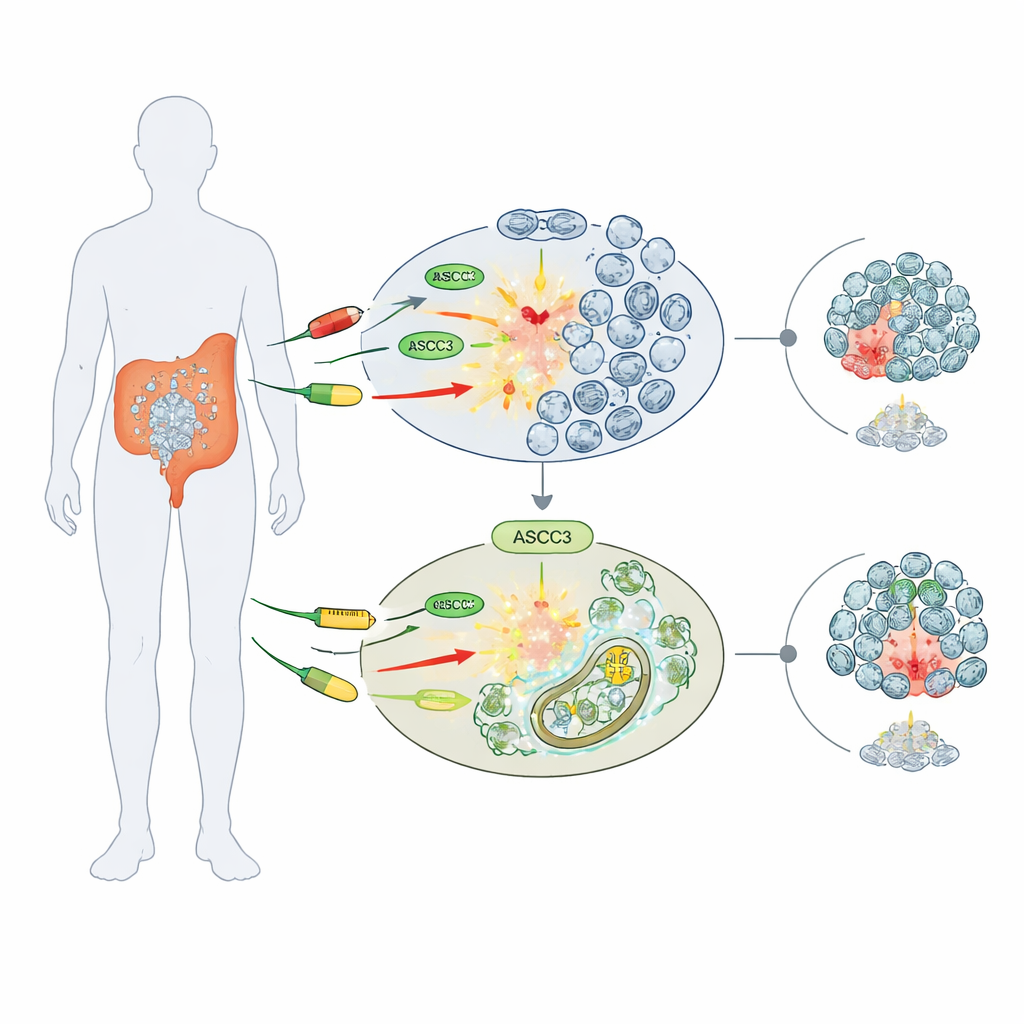
Ein Wächter der Arzneimittelempfindlichkeit
Die Forschenden konzentrierten sich auf drei breit eingesetzte Chemotherapeutika, die DNA schädigen oder deren Synthese blockieren: 5‑Fluorouracil (5‑FU), Cisplatin und Hydroxyurea. In mehreren humanen kolorektalen Krebszelllinien verglichen sie normale Zellen mit solchen, aus denen ASCC3 genetisch entfernt wurde. Überraschenderweise überlebten Zellen ohne ASCC3 diese Wirkstoffe besser, bildeten mehr Kolonien und behielten eine höhere Vitalität als die Kontrollzellen. Dieser Effekt der „Chemoresistenz“ war spezifisch: In Knochenkrebszellen (Osteosarkom) veränderte das Entfernen von ASCC3 die Arzneimittelempfindlichkeit nicht, was nahelegt, dass seine Rolle vom Tumortyp abhängt.
Mehr DNA-Schäden, aber besseres Überleben
Auf den ersten Blick wirkt das verbesserte Überleben ASCC3‑defizienter Zellen paradox. Frühere Arbeiten zeigten, dass ASCC3 Zellen dabei hilft, mit gestoppter DNA-Replikation klarzukommen und Brüche in Chromosomen zu verhindern. In dieser Studie führte der Verlust von ASCC3 in kolorektalen Krebszellen, die mit Chemotherapie behandelt wurden, jedoch zu stärkeren Hinweisen auf DNA‑Schäden — helle nukleäre Foci beschädigter DNA und zusätzliche Chromosomenfragmente (Mikronuklei). Mit anderen Worten: Die Zellen waren genetisch instabiler, waren aber dennoch schwerer zu töten. Diese Diskrepanz deutet darauf hin, dass andere Schutzwege neben einfacher DNA‑Reparatur den beschädigten Zellen das Überleben ermöglichen.
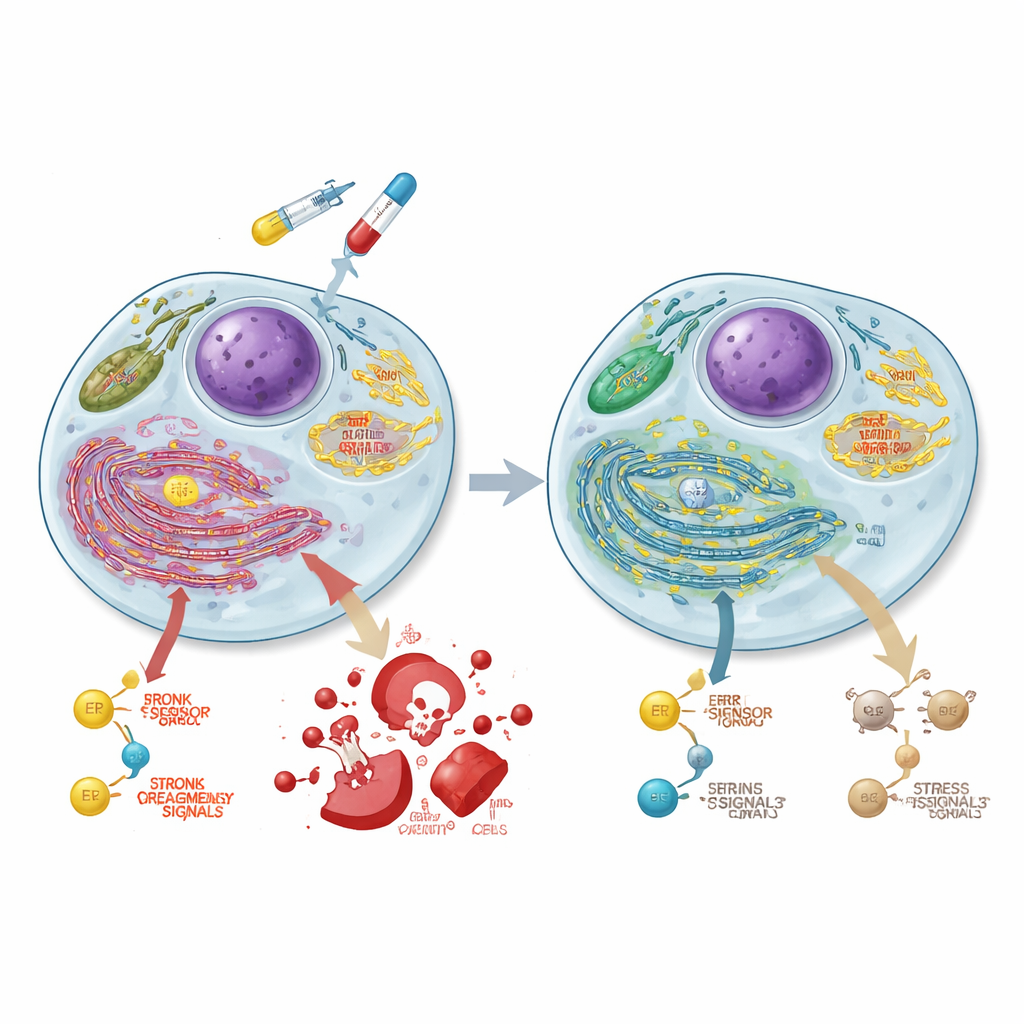
Umschaltung der Energiegewinnung in Krebszellen
Um zu verstehen, was sich noch ändert, wenn ASCC3 fehlt, bestimmten die Forschenden die Genaktivität über das gesamte Genom. Sie fanden heraus, dass ASCC3 normalerweise Genprogramme fördert, die am Zuckerabbau (Glykolyse), am wachstumsbezogenen Signalzentrum mTORC1 und an der Proteinfaltungs‑Maschinerie des endoplasmatischen Retikulums beteiligt sind. Mithilfe spezieller metabolischer Tests zeigten sie, dass Zellen ohne ASCC3 von der Glykolyse wegschalten und stattdessen stark auf ihre Mitochondrien als Energiequelle setzen, wodurch die Sauerstoff‑abhängige Energieproduktion steigt. Tracer‑Experimente mit markiertem Glukose bestätigten, dass diese Zellen mehr Zucker in den Tricarbonsäurezyklus (TCA) und in damit verwandte Aminosäuren lenken, während die Nutzung für bestimmte Bausteine wie Alanin und Serin abnimmt. ASCC3 unterstützte außerdem die Fähigkeit der Zellen, Serin de novo zu synthetisieren und bei Serinmangel zu wachsen, wobei die genauen Mechanismen zwischen den Zelllinien variierten.
Abschwächung eines selbstzerstörerischen Stresssignals
Das endoplasmatische Retikulum (ER) überwacht, ob Proteine korrekt gefaltet werden; bei Überlastung löst es Stressantworten aus, die Zellen entweder an die Anpassung heranführen oder in den Zelltod treiben können. Ein zentraler ER‑Sensor, PERK, kann schließlich ein pro‑apoptotisches Programm über die Proteine CHOP und Caspase‑3 aktivieren. Die Forschenden stellten fest, dass ASCC3 für den Aufbau des PERK‑Proteins während ER‑Stress in kolorektalen Krebszellen essenziell ist, obwohl es das PERK‑Transkript oder dessen Abbaurate nicht verändert. Bei Behandlung mit 5‑FU zeigten normale Zellen im Zeitverlauf starke Anstiege von PERK, CHOP und aktiver Caspase‑3, konsistent mit chemotherapieinduziertem Zelltod. Im Gegensatz dazu konnten ASCC3‑defiziente Zellen diese Proteine nicht vollständig induzieren, und ihre Todesantwort war deutlich reduziert — ein Befund, der ihre Chemoresistenz trotz verstärkter DNA‑Schäden erklärt.
Was das für Patientinnen und Patienten bedeutet
In der Summe zeichnet die Studie ASCC3 als eine Art inneren Verbündeten der Chemotherapie in kolorektalen Krebszellen. Wenn ASCC3 vorhanden ist, fördert es einen stärker glykolyseorientierten Stoffwechsel, eine robuste Serinproduktion und ein starkes ER‑Stresssignal über PERK, das beschädigte Zellen in Richtung Selbstzerstörung treiben kann. Geht ASCC3 verloren, sammeln sich zwar mehr genetische Schäden an, die Zellen überleben aber, indem sie ihre Energieproduktion auf Mitochondrien verlagern und den PERK–CHOP‑Todesweg abschwächen. Diese Einsichten legen nahe, dass ASCC3‑Level dabei helfen könnten vorherzusagen, welche kolorektalen Tumoren gut auf Wirkstoffe wie 5‑FU und Oxaliplatin ansprechen, und dass das gezielte Angreifen des veränderten Stoffwechsels oder der Stressantworten von ASCC3‑armen Tumoren neue Strategien zur Überwindung von Chemoresistenz bieten könnte.
Zitation: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Schlüsselwörter: kolorektaler Krebs, Chemoresistenz, Zellstoffwechsel, ER-Stress, PERK-Signalgebung