Clear Sky Science · nl
ASCC3 bevordert chemosensitiviteit in colorectale kankercellen
Waarom dit onderzoek ertoe doet
Chemotherapie is een standaardbehandeling bij gevorderde colorectale kanker, maar veel tumoren leren uiteindelijk te overleven onder deze harde therapieën. Deze studie onderzoekt een minder bekend eiwit, ASCC3, en toont aan dat het onverwacht colorectale kankercellen juist gevoeliger maakt voor gangbare chemotherapiemiddelen. Door te ontrafelen hoe ASCC3 DNA-schade, celmetabolisme en stresssignalen binnen de cel verbindt, wijst het werk op mogelijke nieuwe manieren om te voorspellen welke patiënten op behandeling reageren — en hoe resistente tumoren mogelijk uitgeschakeld kunnen worden.
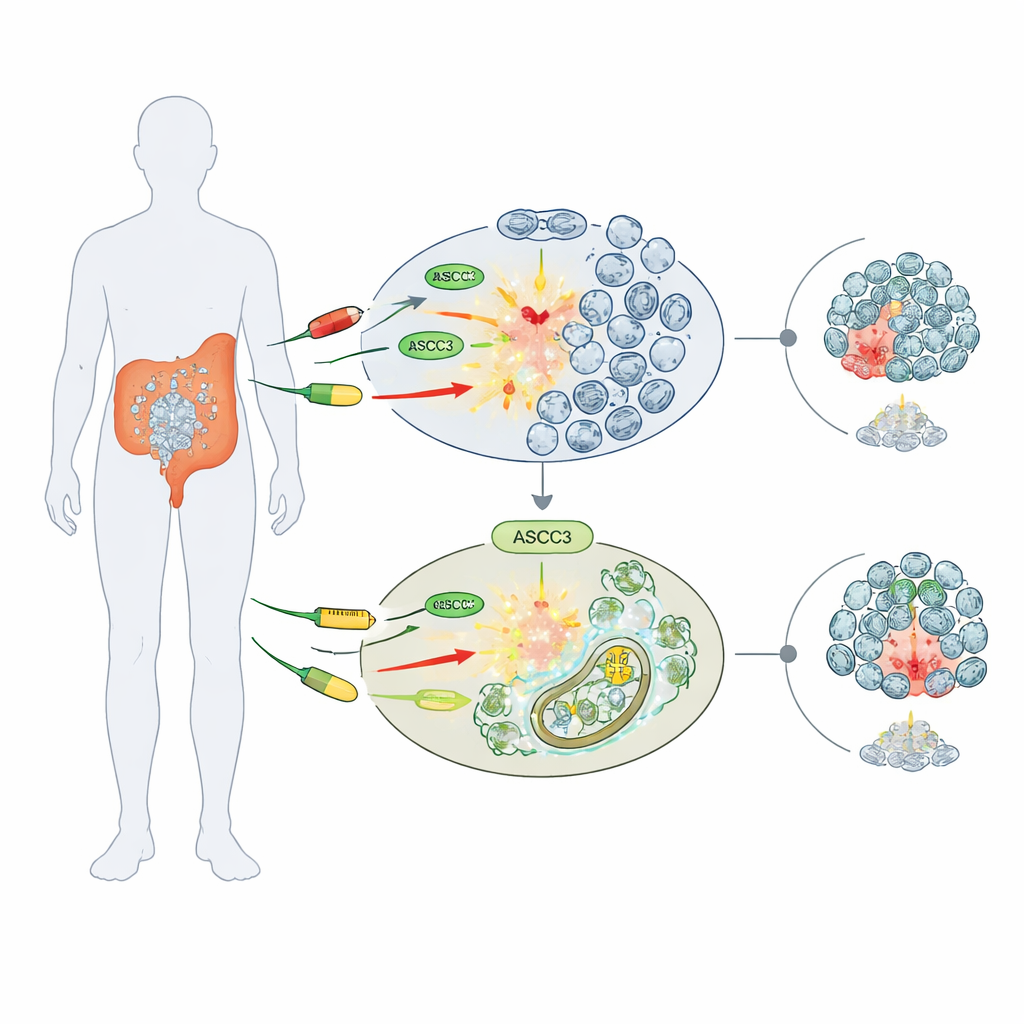
Een poortwachter voor gevoeligheid voor geneesmiddelen
De onderzoekers concentreerden zich op drie veelgebruikte chemotherapeutica die DNA beschadigen of de DNA-synthese blokkeren: 5-fluorouracil (5-FU), cisplatin en hydroxyureum. Met meerdere menselijke colorectale kankercellijnen vergeleken ze normale cellen met cellen die genetisch zo waren aangepast dat ze geen ASCC3 meer hadden. Verrassend genoeg overleefden cellen zonder ASCC3 deze middelen beter: ze vormden meer kolonies en behielden een hogere levensvatbaarheid dan hun normale tegenhangers. Dit effect van “chemoresistentie” was specifiek: in botkankercellen (osteosarcoom) veranderde het verwijderen van ASCC3 de gevoeligheid voor geneesmiddelen niet, wat suggereert dat de rol ervan afhankelijk is van het kankertype.
Meer DNA-schade, maar toch meer overleving
Op het eerste gezicht lijkt de verbeterde overleving van ASCC3-deficiënte cellen paradoxaal. Eerder werk toonde aan dat ASCC3 cellen helpt om met vastgelopen DNA-replicatie om te gaan en gebroken chromosomen te voorkomen. In deze studie leidde het verlies van ASCC3, wanneer colorectale kankercellen met chemotherapie werden behandeld, tot meer aanwijzingen voor DNA-schade — heldere nucleaire focussen van beschadigd DNA en extra chromosoomfragmenten die micronuclei worden genoemd. Met andere woorden: de cellen waren genetisch minder stabiel, maar moeilijker te doden. Deze kloof suggereerde dat andere beschermende routes, verder dan eenvoudige DNA-reparatie, de beschadigde cellen in leven hielden.
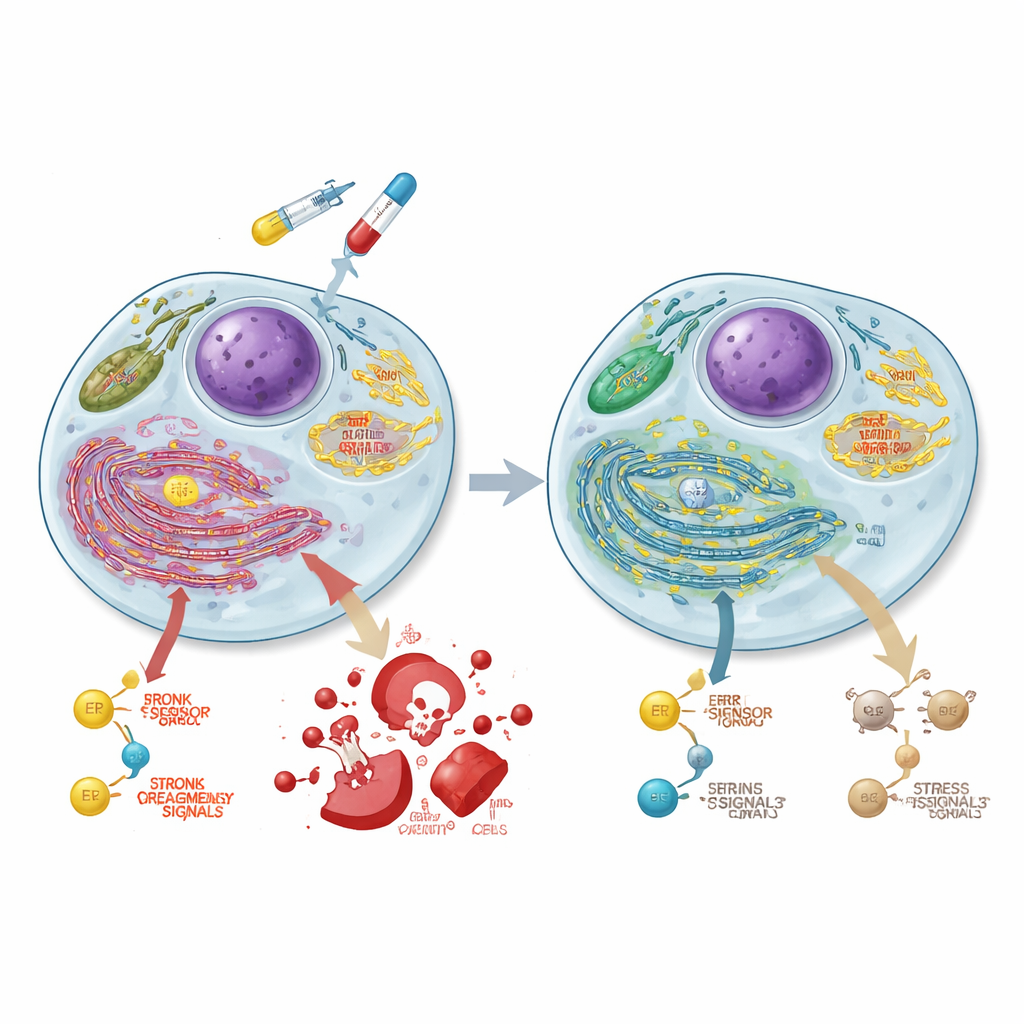
Hernieuwd energiegebruik in kankercellen
Om te begrijpen wat er nog meer verandert bij verlies van ASCC3, maten de onderzoekers de genactiviteit over het hele genoom. Ze ontdekten dat ASCC3 normaal gesproken groepen genen stimuleert die betrokken zijn bij suikerafbraak (glycolyse), een groeigerelateerde signaalhub genaamd mTORC1, en eiwitvouwing in het endoplasmatisch reticulum. Met gespecialiseerde metabolische tests toonden ze aan dat cellen zonder ASCC3 minder op glycolyse vertrouwden en in plaats daarvan zwaar leunden op hun mitochondriën, de energiecentrales van de cel, met verhoogde zuurstofafhankelijke energieproductie. Tracerexperimenten met gelabelde glucose bevestigden dat deze cellen meer suiker naar de tricarbonzuurcyclus (TCA-cyclus) en verwante aminozuren leidden, terwijl het gebruik voor bepaalde bouwstenen zoals alanine en serine afnam. ASCC3 ondersteunde ook het vermogen van de cel om serine zelf te synthetiseren en te groeien wanneer dit aminozuur schaars was, hoewel de exacte mechanismen tussen cellijnen verschilden.
Een zelfvernietigend stressesignaal dempen
Het endoplasmatisch reticulum (ER) controleert of eiwitten goed gevouwen zijn; wanneer het overbelast raakt, activeert het stressreacties die cellen kunnen helpen zich aan te passen of hen richting celdood kunnen duwen. Een belangrijke ER-sensor, PERK, kan uiteindelijk een pro-doodprogramma activeren dat de eiwitten CHOP en caspase 3 omvat. De onderzoekers vonden dat ASCC3 essentieel is voor de opbouw van PERK-eiwit tijdens ER-stress in colorectale kankercellen, ook al verandert het niet het PERK-mRNA of de afbraaksnelheid ervan. Wanneer cellen met 5-FU werden behandeld, lieten normale cellen sterke verhogingen in PERK, CHOP en actieve caspase 3 zien in de loop van de tijd, wat consistent is met chemotherapie-geïnduceerde celdood. In tegenstelling daarmee slaagden ASCC3-deficiënte cellen er niet in deze eiwitten volledig te induceren en was hun doodsrespons duidelijk verminderd, wat helpt verklaren waarom ze chemoresistent zijn ondanks grotere DNA-schade.
Wat dit betekent voor patiënten
Samengevat schetst de studie ASCC3 als een interne bondgenoot van chemotherapie in colorectale kankercellen. Wanneer ASCC3 aanwezig is, ondersteunt het een meer op glycolyse gericht metabolisme, robuuste serinesynthese en een sterk ER-stresssignaal via PERK dat beschadigde cellen naar zelfvernietiging kan leiden. Wanneer ASCC3 verloren gaat, stapelen cellen meer genetische schade op maar overleven ze door hun energieproductie naar mitochondriën te verschuiven en het PERK–CHOP-doodsignaal af te zwakken. Deze inzichten suggereren dat ASCC3-niveaus kunnen helpen voorspellen welke colorectale tumoren goed zullen reageren op middelen zoals 5-FU en oxaliplatin, en dat het gericht aanpakken van het veranderde metabolisme of de stressreacties van ASCC3-arme tumoren nieuwe strategieën kan bieden om chemoresistentie te overwinnen.
Bronvermelding: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Trefwoorden: colorectale kanker, chemoresistentie, celmetabolisme, ER-stress, PERK-signaleringsroute