Clear Sky Science · ru
ASCC3 способствует хемочувствительности клеток колоректального рака
Почему это исследование важно
Химиотерапия — основное лечение при распространённом колоректальном раке, однако многие опухоли со временем учатся выживать при воздействии этих жёстких препаратов. В этой работе изучается малоизвестный белок ASCC3 и показано, что он неожиданно делает клетки колоректального рака более уязвимыми к распространённым химиопрепаратам. Раскрывая, как ASCC3 связывает повреждение ДНК, клеточный метаболизм и внутриклеточные сигналы стресса, исследование указывает на возможные новые способы предсказать, какие пациенты ответят на лечение, и как можно нейтрализовать резистентные опухоли.
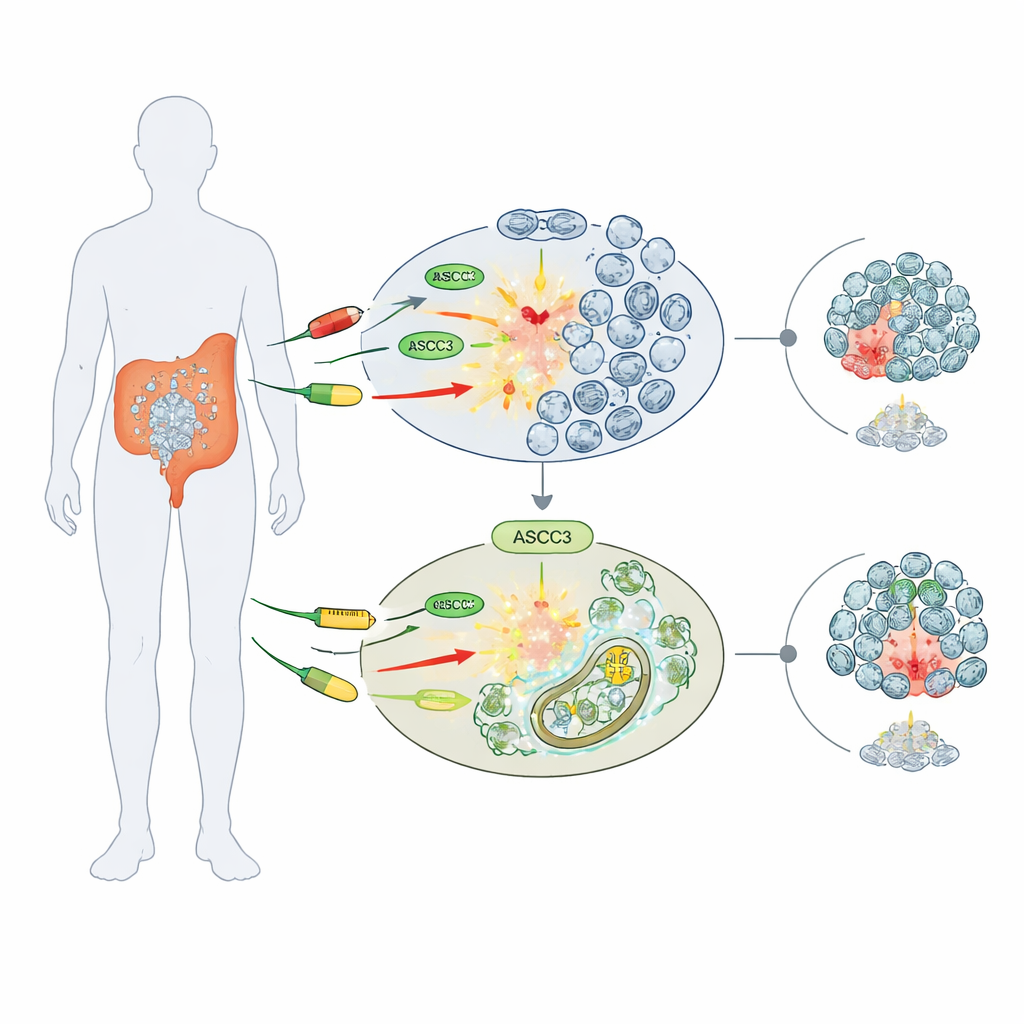
«Шлюз» чувствительности к препаратам
Исследователи сосредоточились на трёх широко используемых химиопрепаратах, повреждающих ДНК или блокирующих её синтез: 5‑фторурацил (5‑FU), цисплатин и гидроксикислота (гидроксиуреа). На нескольких линиях человеческих клеток колоректального рака они сравнили нормальные клетки и клетки, генетически лишённые ASCC3. К их удивлению, клетки без ASCC3 лучше переносили эти препараты, формируя больше колоний и сохраняя более высокую жизнеспособность по сравнению с нормальными клетками. Этот эффект «хеморезистентности» был специфичен: в клетках остеосаркомы удаление ASCC3 не изменяло чувствительность к препаратам, что указывает на зависимость роли ASCC3 от типа рака.
Больше повреждений ДНК, но больше выживаемости
На первый взгляд повышенная выживаемость клеток, лишённых ASCC3, кажется парадоксальной. Ранее показано, что ASCC3 помогает клеткам справляться с остановленной репликацией ДНК, предотвращая ломки хромосом. В этом исследовании при лечении колоректальных клеток химиопрепаратами потеря ASCC3 приводила к большему числу признаков повреждения ДНК — ярким ядерным фокусам повреждённой ДНК и дополнительным фрагментам хромосом, называемым микроядрами. Иными словами, клетки были генетически менее стабильны, но их было труднее уничтожить. Такое расхождение указывает на то, что другие защитные пути, помимо простого ремонта ДНК, позволяют повреждённым клеткам сохраняться.
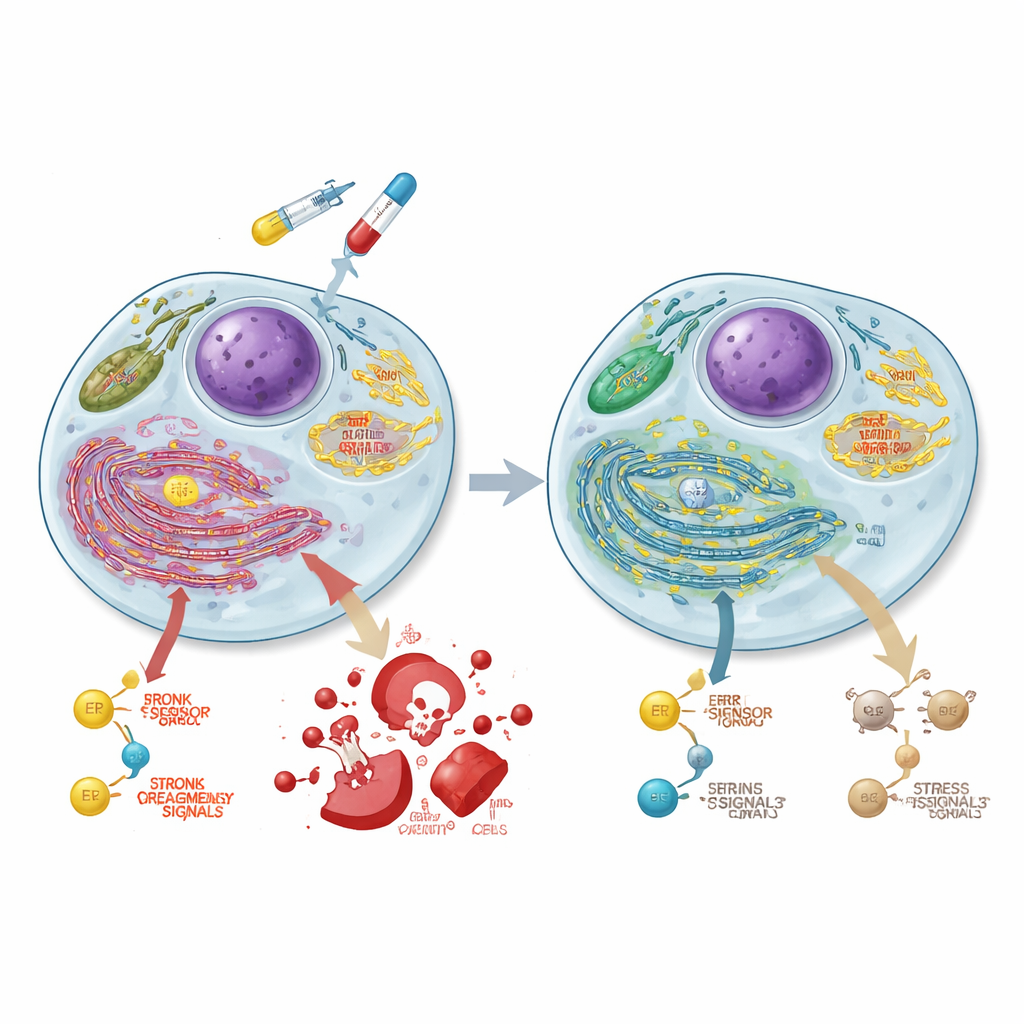
Перенастройка энергетического метаболизма опухолевых клеток
Чтобы понять, что ещё меняется при потере ASCC3, команда измерила активность генов по всему геному. Они обнаружили, что ASCC3 обычно усиливает наборы генов, участвующих в расщеплении сахаров (гликолизе), в сигнальном центре роста mTORC1 и в путях сворачивания белков в эндоплазматическом ретикулуме. Специализированные метаболические тесты показали, что клетки без ASCC3 отходят от гликолиза и вместо этого значительно опираются на митохондрии — клеточные электростанции — повышая аэробное производство энергии. Эксперименты с меченым глюкозой тракером подтвердили, что эти клетки направляют больше сахара в цикл трикарбоновых кислот (TCA) и связанные аминокислоты, сокращая его использование для синтеза некоторых строительных блоков, таких как аланин и серин. ASCC3 также поддерживал способность клетки синтезировать серин «с нуля» и расти при дефиците этой аминокислоты, хотя точные механизмы варьировали между линиями клеток.
Подавление сигнала самоуничтожения при стрессе
Эндоплазматический ретикулум (ЭПР) контролирует, правильно ли сворачиваются белки; при перегрузке он запускает стресс‑ответы, которые могут либо помочь клетке адаптироваться, либо направить её на смерть. Один ключевой сенсор ЭПР, PERK, в конечном счёте может активировать протеасмертную программу с участием белков CHOP и каспазы‑3. Исследователи обнаружили, что ASCC3 необходим для накопления белка PERK во время стресса ЭПР в клетках колоректального рака, хотя он не изменяет транскрипт PERK или скорость его распада. При обработке 5‑FU нормальные клетки демонстрировали сильное повышение PERK, CHOP и активной каспазы‑3 со временем, что согласуется с индуцированной химиотерапией гибелью клеток. Напротив, клетки, лишённые ASCC3, не смогли полностью индуцировать эти белки, и их ответ гибели был значительно снижен, что помогает объяснить хеморезистентность при более выраженных повреждениях ДНК.
Что это означает для пациентов
В сумме исследование рисует ASCC3 как нечто вроде внутреннего союзника химиотерапии в клетках колоректального рака. При наличии ASCC3 он поддерживает метаболизм, ориентированный на гликолиз, надёжный синтез серина и сильный сигнал стресса ЭПР через PERK, который может направлять повреждённые клетки на самоуничтожение. При потере ASCC3 клетки накапливают больше генетических повреждений, но выживают, переключая производство энергии на митохондрии и ослабляя путь смерти PERK–CHOP. Эти знания позволяют предположить, что уровни ASCC3 могут помочь предсказать, какие опухоли колоректального рака хорошо ответят на препараты вроде 5‑FU и оксалиплатина, а также что таргетирование изменённого метаболизма или стрессовых ответов в опухолях с низким ASCC3 может предложить новые стратегии для преодоления хеморезистентности.
Цитирование: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Ключевые слова: колоректальный рак, хеморезистентность, метаболизм клеток, стресс ЭПР, сигнальная передача PERK