Clear Sky Science · ja
ASCC3は大腸がん細胞の化学療法感受性を促進する
この研究が重要な理由
化学療法は進行大腸がんの主要な治療法ですが、多くの腫瘍はやがてこれらの強力な薬剤を回避して生き残るようになります。本研究はあまり知られていないタンパク質ASCC3に着目し、それが意外にも大腸がん細胞を一般的な化学療法薬に対して脆弱にすることを明らかにしました。ASCC3がどのようにDNA障害、細胞代謝、細胞内ストレス信号をつなぐかを解明することで、治療に反応する患者を予測する方法や、薬剤耐性を獲得した腫瘍を無力化する新たな手がかりを示しています。
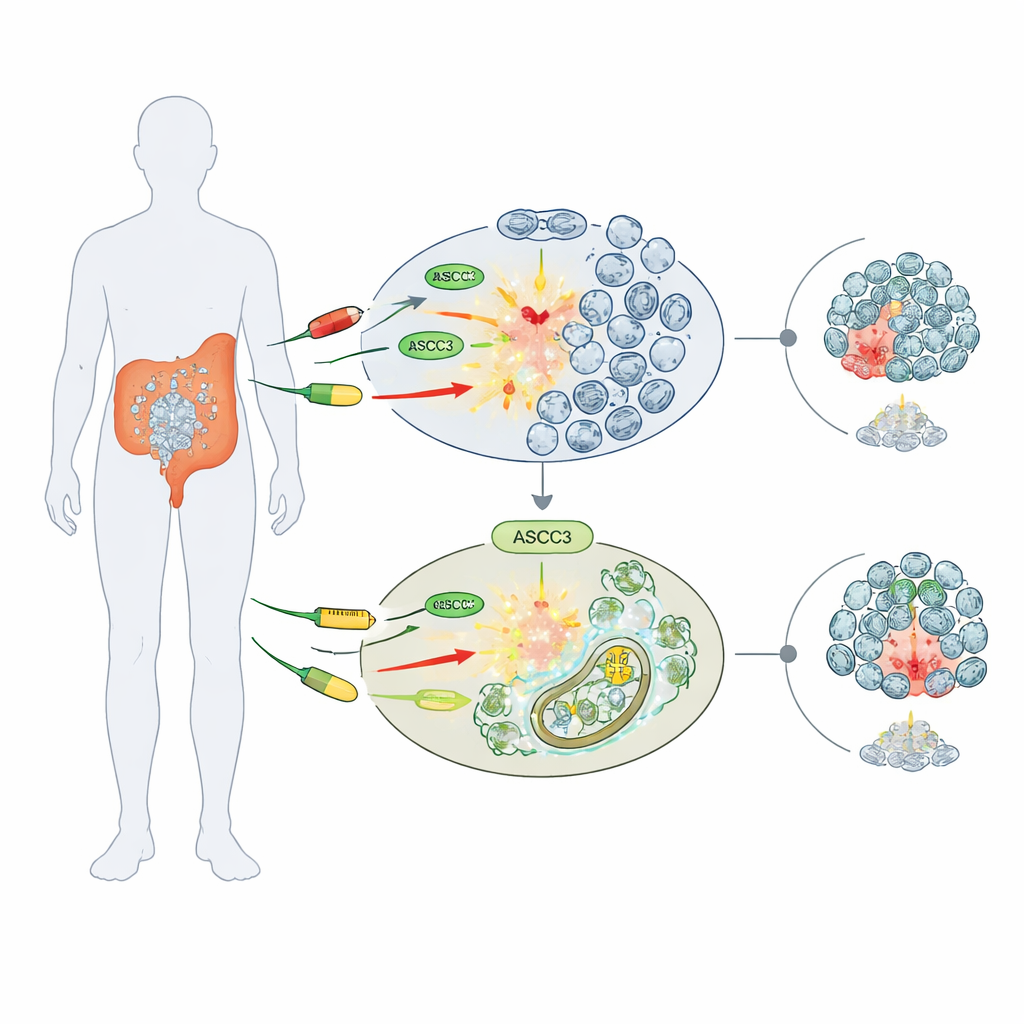
薬剤感受性のゲートキーパー
研究者らはDNAを損傷させるかその合成を阻害する、広く用いられる三つの化学療法剤(5-フルオロウラシル(5-FU)、シスプラチン、ヒドロキシウレア)に着目しました。複数のヒト大腸がん細胞株を用い、ASCC3を欠損させた細胞と通常の細胞を比較したところ、驚くべきことにASCC3を欠く細胞の方がこれらの薬剤に対して生存しやすく、コロニー形成や生存率が高いことがわかりました。この「化学療法耐性」効果は特異的で、骨肉腫(骨がん)細胞ではASCC3を除去しても薬剤感受性に変化がなく、その役割ががんの種類によって異なることを示唆しています。
より多くのDNA損傷、それでも生存
一見すると、ASCC3欠損細胞の生存性の向上は逆説的です。以前の研究ではASCC3が複製の停止に対処し、染色体破損を防ぐのに役立つことが示されていました。本研究では、大腸がん細胞に化学療法を作用させた際、ASCC3を失うと損傷DNAの明瞭な核内フォーカスや小核(micronuclei)といったDNA損傷の兆候が増加しました。言い換えれば、これらの細胞は遺伝的に不安定であるにもかかわらず、死ににくくなっていました。この不一致は、単純なDNA修復以外の保護経路が損傷細胞の存続を可能にしていることを示唆しています。
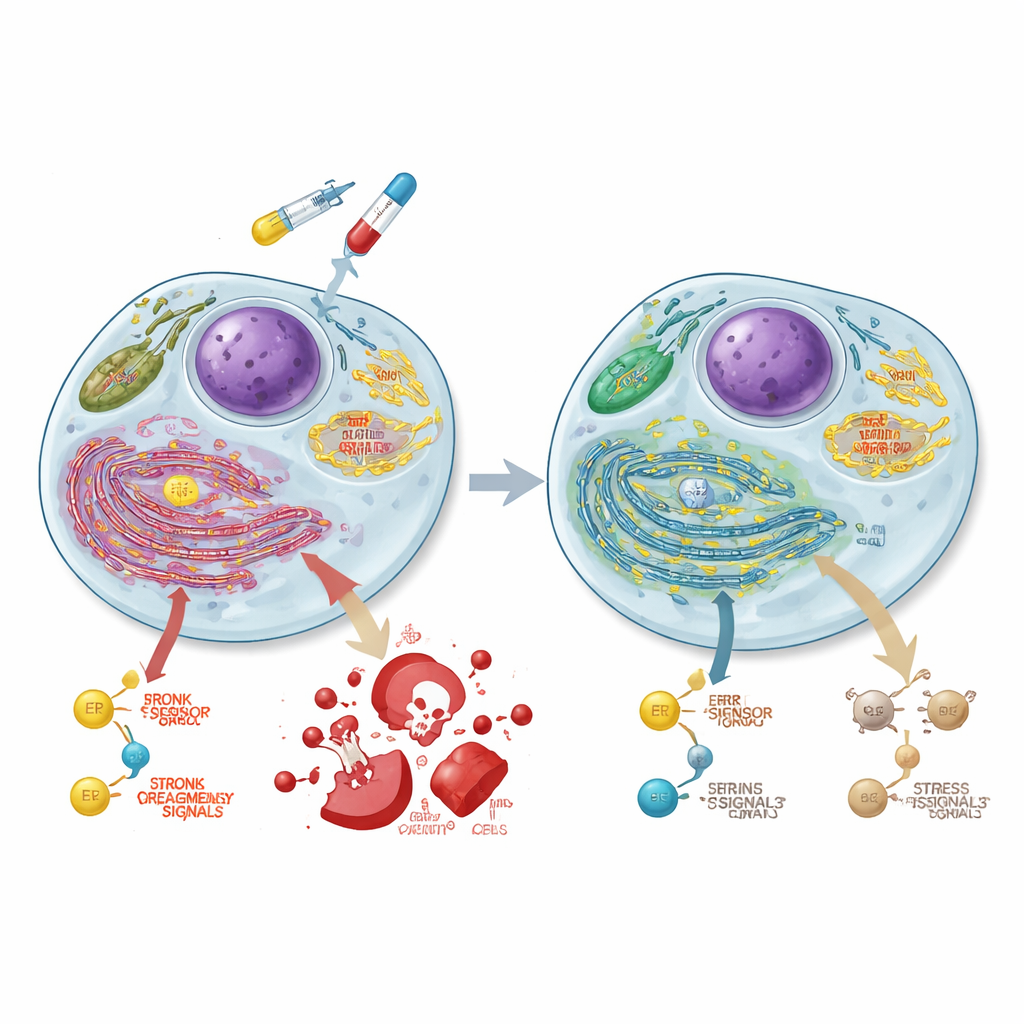
がん細胞のエネルギー生産の再配線
ASCC3喪失時に他に何が変わるかを調べるため、研究チームはゲノム全体の遺伝子発現を測定しました。その結果、ASCC3は通常、糖分解(解糖)や成長関連のシグナルハブであるmTORC1、そして小胞体におけるタンパク質立体構造形成(フォールディング)経路に関与する一群の遺伝子を促進していることが分かりました。専用の代謝解析では、ASCC3欠損細胞は解糖から離れ、代わりにミトコンドリア(細胞の発電所)に大きく依存して酸素を用いたエネルギー生産を増やすことが示されました。標識グルコースを用いたトレーサー実験では、これらの細胞が糖を三酸化炭素回路(TCA回路)や関連するアミノ酸へより多く流し、アラニンやセリンのような特定の合成用途への供給を減らしていることが確認されました。ASCC3はまた、細胞がセリンを自前で合成する能力や、セリンが不足した環境での増殖を支持していましたが、その正確な仕組みは細胞株によって異なっていました。
自己破壊的なストレス信号の鈍化
小胞体(ER)はタンパク質が正しく折りたたまれているかを監視し、過負荷になると細胞が適応するか死へ向かうストレス応答を起動します。主要なERセンサーの一つであるPERKは最終的にCHOPやカスパーゼ3を含むプロデスプログラムを活性化し得ます。研究者らは、ASCC3が大腸がん細胞のERストレス時にPERKタンパク質の蓄積に必須であることを見出しました。これはPERKの転写量や分解速度を変えるわけではありません。5-FU処理では、通常の細胞でPERK、CHOP、活性化カスパーゼ3が時間とともに強く増加し、化学療法による細胞死を示していました。対照的にASCC3欠損細胞はこれらのタンパク質を十分に誘導できず、細胞死応答が著しく抑えられており、重度のDNA損傷にもかかわらず化学療法耐性を示す理由を説明しています。
患者への意義
総じて、この研究はASCC3を大腸がん細胞における化学療法の内部的な味方のようなものとして描き出します。ASCC3が存在すると、解糖に傾いた代謝、堅牢なセリン合成、そしてPERKを介した強いERストレス信号が支持され、損傷を受けた細胞が自己破壊へ向かいやすくなります。ASCC3が失われると、細胞はより多くの遺伝的損傷を蓄積するものの、代謝をミトコンドリア依存へと切り替え、PERK–CHOPの死経路を鈍化させて生き延びます。これらの知見は、ASCC3の発現レベルが5-FUやオキサリプラチンのような薬剤に良く反応する大腸腫瘍を予測する手がかりになり得ること、そしてASCC3が低い腫瘍の変化した代謝やストレス応答を標的にすることが化学療法耐性克服の新しい戦略を提供する可能性を示唆しています。
引用: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
キーワード: 大腸がん, 化学療法耐性, 細胞代謝, 小胞体ストレス, PERKシグナル伝達