Clear Sky Science · pt
ASCC3 promove quimiossensibilidade em células de câncer colorretal
Por que esta pesquisa importa
A quimioterapia é um tratamento fundamental para câncer colorretal avançado, mas muitos tumores acabam aprendendo a sobreviver a esses fármacos agressivos. Este estudo investiga uma proteína menos conhecida chamada ASCC3 e revela que, de forma inesperada, ela torna as células de câncer colorretal mais vulneráveis aos quimioterápicos comuns. Ao descobrir como o ASCC3 conecta dano ao DNA, metabolismo celular e sinais de estresse intracelular, o trabalho aponta para possíveis novas maneiras de prever quais pacientes responderão ao tratamento — e como tumores resistentes podem ser desarmados.
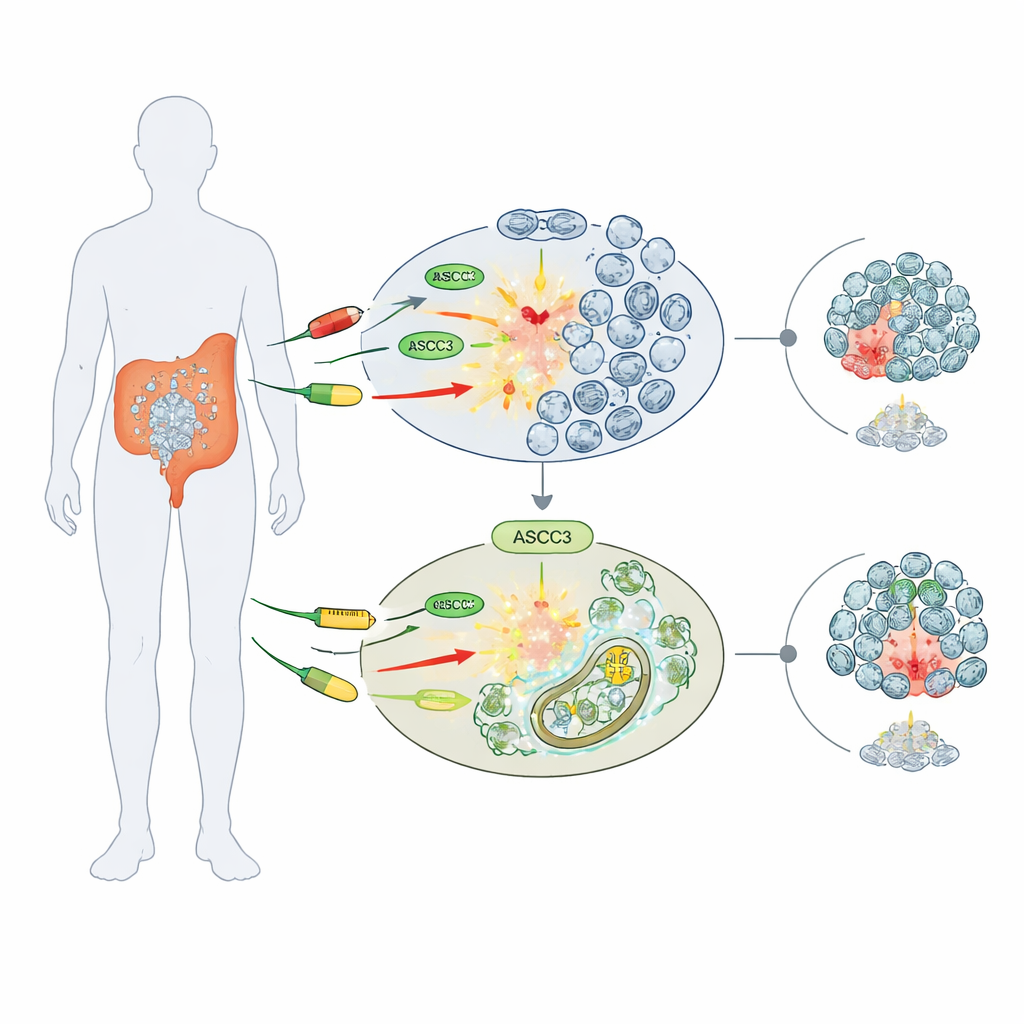
Um porteiro da sensibilidade aos medicamentos
Os pesquisadores concentraram-se em três agentes quimioterápicos amplamente usados que danificam o DNA ou bloqueiam sua produção: 5-fluorouracil (5-FU), cisplatina e hidroxiureia. Trabalhando com várias linhagens humanas de células de câncer colorretal, compararam células normais com células geneticamente modificadas para não expressar ASCC3. Surpreendentemente, as células sem ASCC3 sobreviveram melhor a esses fármacos, formando mais colônias e mantendo maior viabilidade do que suas contrapartes normais. Esse efeito de “quimiorresistência” foi específico: em células de câncer ósseo (osteossarcoma), remover o ASCC3 não alterou a sensibilidade aos medicamentos, sugerindo que seu papel depende do tipo de câncer.
Mais dano ao DNA, porém mais sobrevivência
À primeira vista, a melhor sobrevivência das células deficientes em ASCC3 parece paradoxal. Trabalhos anteriores mostraram que o ASCC3 ajuda as células a lidar com a replicação do DNA interrompida, prevenindo cromossomos quebrados. Neste estudo, quando células de câncer colorretal foram tratadas com quimioterapia, a perda de ASCC3 levou a mais sinais de dano ao DNA — focos nucleares intensos de DNA danificado e fragmentos extras de cromossomos chamados micronúcleos. Em outras palavras, as células eram geneticamente menos estáveis, mas eram mais difíceis de eliminar. Essa desconexão sugeriu que outras vias de proteção, além do reparo simples do DNA, permitiam que as células danificadas persistissem.
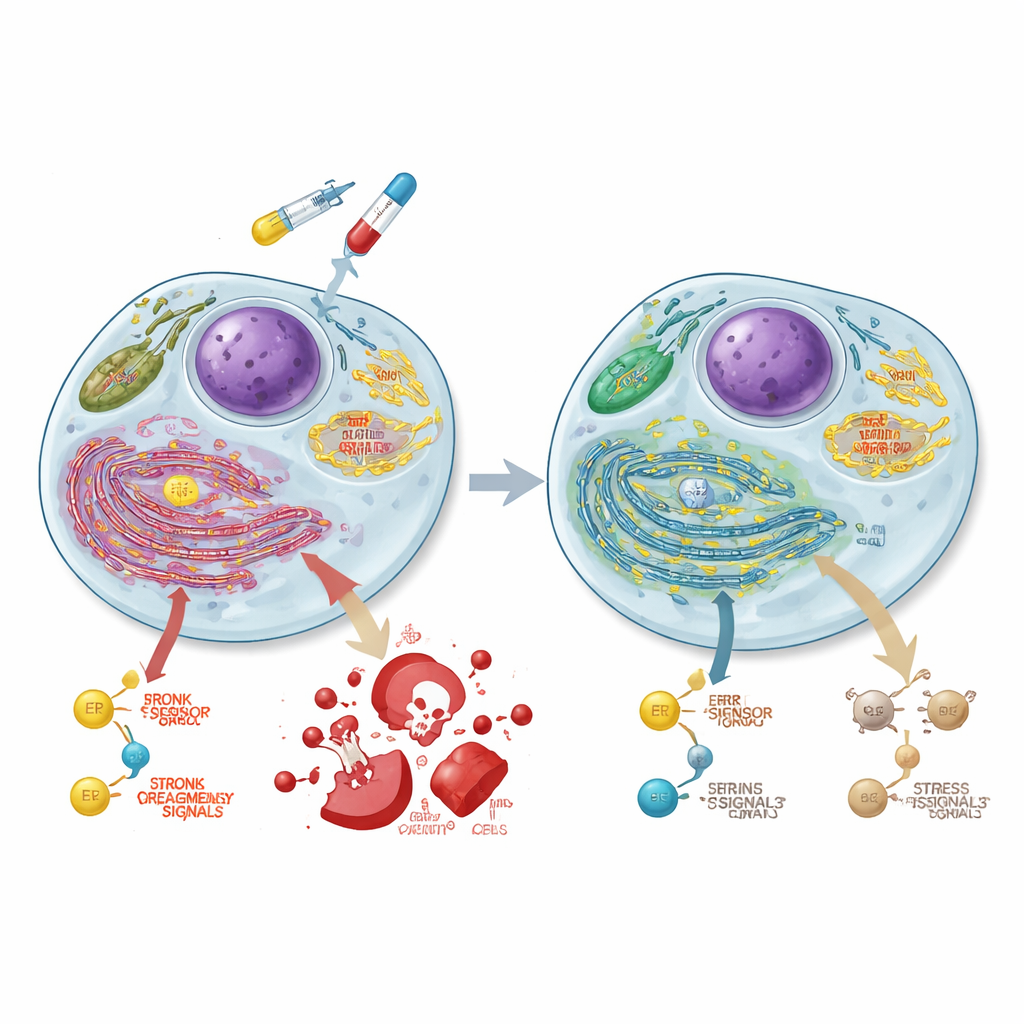
Reprogramando como células cancerosas produzem energia
Para entender o que mais muda quando o ASCC3 é perdido, a equipe mediu a atividade gênica em todo o genoma. Eles descobriram que o ASCC3 normalmente reforça conjuntos de genes envolvidos na quebra de açúcar (glicólise), em um centro de sinalização relacionado ao crescimento chamado mTORC1 e em vias de dobramento de proteínas no retículo endoplasmático da célula. Usando testes metabólicos especializados, mostraram que células sem ASCC3 desviaram-se da glicólise e passaram a depender fortemente das mitocôndrias, as usinas de energia da célula, aumentando a produção de energia baseada em oxigênio. Experimentos com traçadores usando glicose marcada confirmaram que essas células canalizaram mais açúcar para o ciclo do ácido tricarboxílico (TCA) e aminoácidos relacionados, enquanto reduziram seu uso para certos blocos de construção como alanina e serina. O ASCC3 também apoiou a capacidade da célula de sintetizar serina de novo e de crescer quando esse aminoácido era escasso, embora os mecanismos exatos variassem entre as linhas celulares.
Atenuando um sinal de estresse autodestrutivo
O retículo endoplasmático (RE) monitora se as proteínas estão corretamente dobradas; quando sobrecarregado, ele desencadeia respostas ao estresse que podem ajudar a célula a se adaptar ou empurrá-la rumo à morte. Um sensor chave do RE, PERK, pode eventualmente ativar um programa pró-morte envolvendo as proteínas CHOP e caspase 3. Os pesquisadores descobriram que o ASCC3 é essencial para a acumulação da proteína PERK durante o estresse do RE em células de câncer colorretal, embora não altere o transcrito gênico de PERK nem sua taxa de degradação. Quando as células foram tratadas com 5-FU, células normais mostraram aumentos fortes em PERK, CHOP e caspase 3 ativa ao longo do tempo, consistente com morte celular induzida pela quimioterapia. Em contraste, células deficientes em ASCC3 não conseguiram induzir plenamente essas proteínas, e sua resposta de morte foi marcadamente reduzida, ajudando a explicar sua quimiorresistência apesar do dano ao DNA mais intenso.
O que isso significa para os pacientes
Em conjunto, o estudo pinta o ASCC3 como uma espécie de aliado interno da quimioterapia em células de câncer colorretal. Quando o ASCC3 está presente, ele sustenta um metabolismo mais focado na glicólise, produção robusta de serina e um forte sinal de estresse do RE via PERK que pode levar células danificadas à autodestruição. Quando o ASCC3 é perdido, as células acumulam mais danos genéticos, mas sobrevivem mudando sua produção de energia para as mitocôndrias e atenuando a via de morte PERK–CHOP. Essas descobertas sugerem que os níveis de ASCC3 poderiam ajudar a prever quais tumores colorretais responderão bem a fármacos como 5-FU e oxaliplatina, e que mirar o metabolismo alterado ou as respostas ao estresse em tumores com pouca expressão de ASCC3 pode oferecer novas estratégias para superar a quimiorresistência.
Citação: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Palavras-chave: câncer colorretal, quimiorresistência, metabolismo celular, estresse do RE, sinalização PERK