Clear Sky Science · it
ASCC3 favorisce la chemosensibilità nelle cellule del cancro colorettale
Perché questa ricerca è importante
La chemioterapia è un trattamento fondamentale per il cancro colorettale avanzato, eppure molti tumori finiscono per imparare a sopravvivere a questi farmaci aggressivi. Questo studio esplora una proteina poco nota chiamata ASCC3 e rivela che, inaspettatamente, rende le cellule del cancro colorettale più vulnerabili ai comuni farmaci chemioterapici. Svelando come ASCC3 connetta il danno al DNA, il metabolismo cellulare e i segnali di stress intracellulare, il lavoro indica possibili nuovi modi per prevedere quali pazienti risponderanno al trattamento e come i tumori resistenti potrebbero essere neutralizzati.
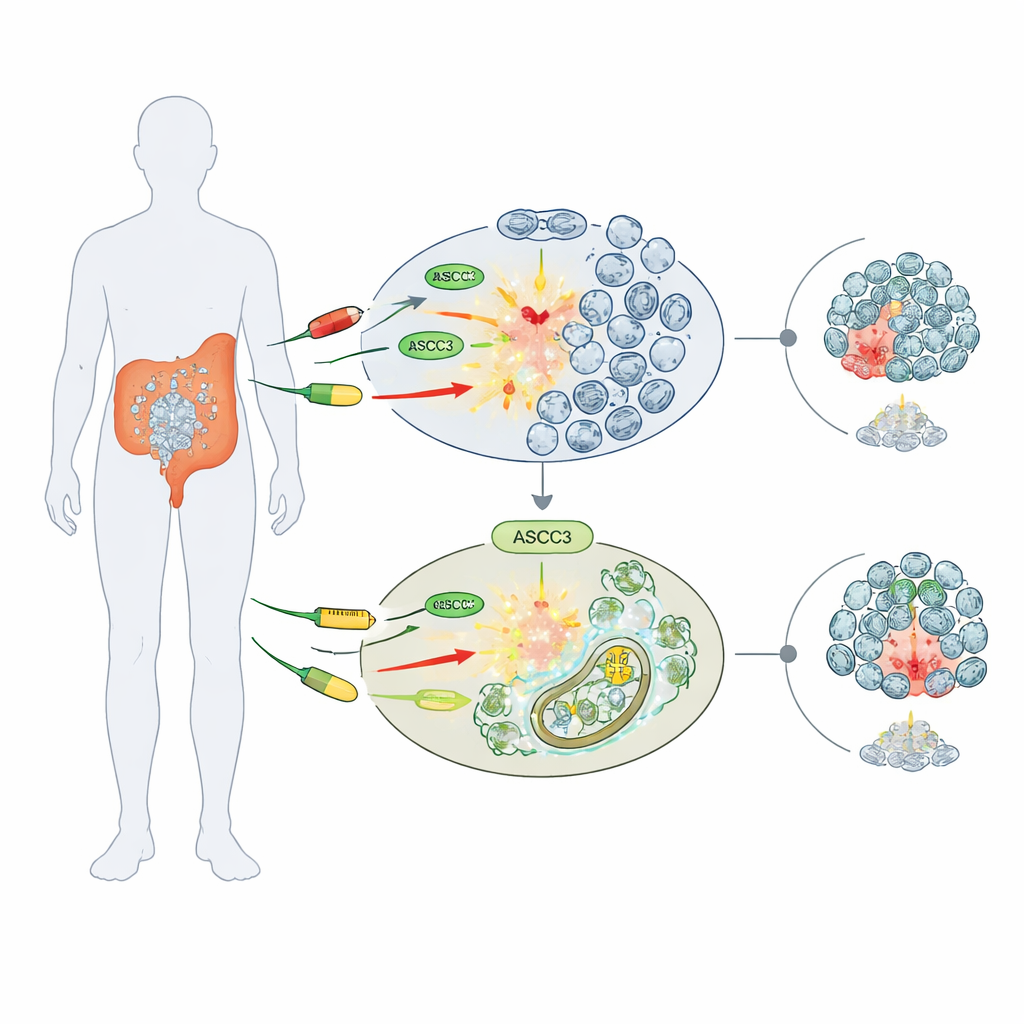
Un guardiano della sensibilità ai farmaci
I ricercatori si sono concentrati su tre agenti chemioterapici ampiamente usati che danneggiano il DNA o ne bloccano la produzione: 5-fluorouracile (5-FU), cisplatino e idrossiurea. Lavorando con diverse linee cellulari umane di cancro colorettale, hanno confrontato cellule normali con cellule geneticamente ingegnerizzate prive di ASCC3. Sorprendentemente, le cellule senza ASCC3 sopravvivevano meglio a questi farmaci, formando più colonie e mantenendo una maggiore vitalità rispetto alle controparti normali. Questo effetto di “chemi-resistenza” era specifico: nelle cellule di cancro osseo (osteosarcoma), la rimozione di ASCC3 non modificava la sensibilità ai farmaci, suggerendo che il suo ruolo dipende dal tipo di tumore.
Più danni al DNA, ma più sopravvivenza
A prima vista, la migliore sopravvivenza delle cellule prive di ASCC3 sembra paradossale. Lavori precedenti avevano mostrato che ASCC3 aiuta le cellule a gestire la replicazione del DNA bloccata, prevenendo la rottura dei cromosomi. In questo studio, quando le cellule del cancro colorettale sono state trattate con chemioterapia, la perdita di ASCC3 ha portato a più segni di danno al DNA: focolai nucleari luminosi di DNA danneggiato e frammenti cromosomici extra chiamati micronuclei. In altre parole, le cellule erano geneticamente meno stabili, eppure più difficili da uccidere. Questa disconnessione suggerisce che altre vie protettive, oltre alla semplice riparazione del DNA, permettono alle cellule danneggiate di persistere.
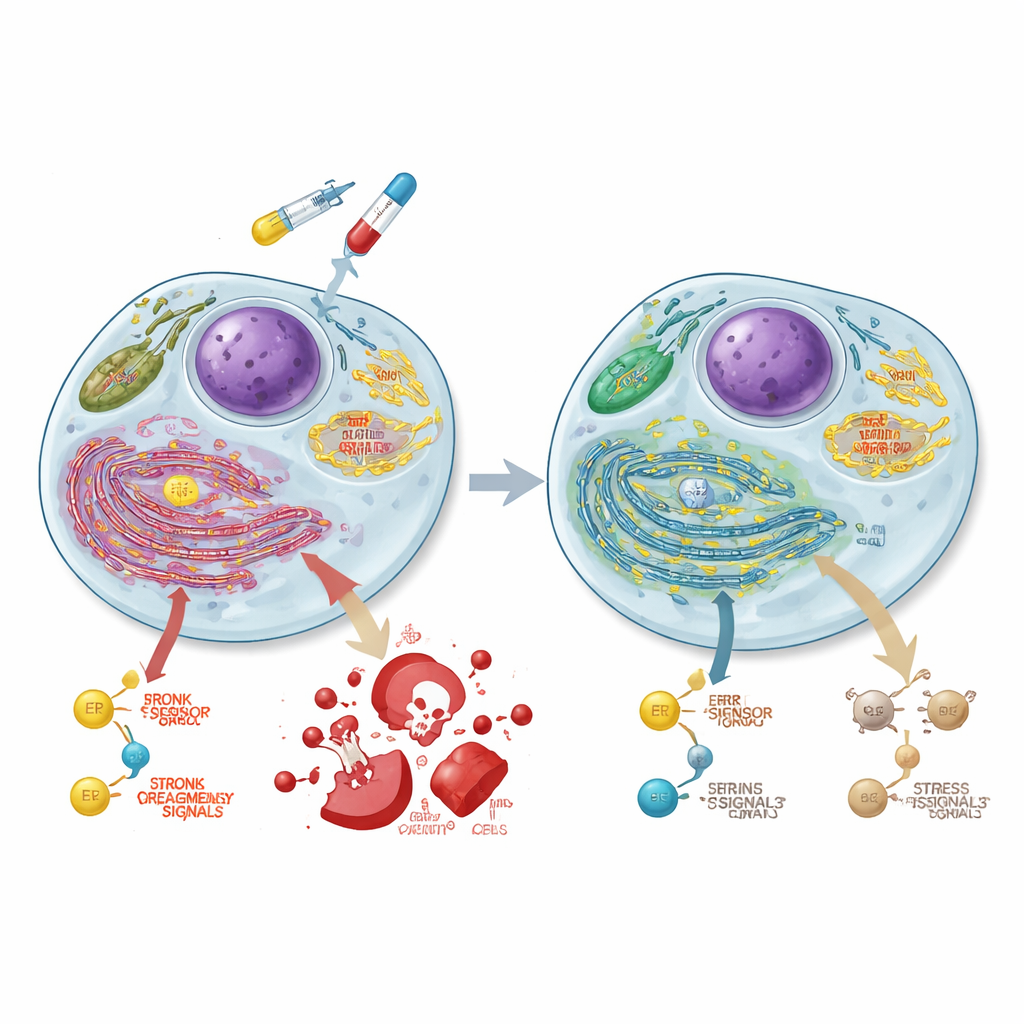
Rimodellamento della produzione di energia nelle cellule tumorali
Per capire cos’altro cambia quando ASCC3 viene perso, il gruppo ha misurato l’attività genica sull’intero genoma. Hanno scoperto che ASCC3 normalmente potenzia insiemi di geni coinvolti nella degradazione degli zuccheri (glicolisi), in un centro di segnalazione legato alla crescita chiamato mTORC1, e nelle vie di piegatura delle proteine nel reticolo endoplasmatico. Tramite test metabolici specializzati, hanno mostrato che le cellule prive di ASCC3 si spostano dalla glicolisi e fanno invece forte affidamento sui mitocondri, le centrali energetiche della cellula, aumentando la produzione di energia basata sull’ossigeno. Esperimenti con traccianti di glucosio marcato hanno confermato che queste cellule canalizzano più zucchero nel ciclo degli acidi tricarbossilici (TCA) e negli aminoacidi correlati, riducendone l’uso per alcuni mattoni come alanina e serina. ASCC3 supportava anche la capacità della cellula di sintetizzare serina da zero e di crescere quando questo amminoacido era scarso, sebbene i meccanismi esatti variassero tra le linee cellulari.
Smorzare un segnale di stress autodistruttivo
Il reticolo endoplasmatico (RE) controlla se le proteine sono correttamente ripiegate; quando è sovraccarico, attiva risposte di stress che possono aiutare la cellula ad adattarsi o portarla verso la morte. Un sensore chiave del RE, PERK, può infine attivare un programma pro-morte che coinvolge le proteine CHOP e la caspasi 3. I ricercatori hanno riscontrato che ASCC3 è essenziale per l’accumulo della proteina PERK durante lo stress del RE nelle cellule del cancro colorettale, sebbene non modifichi il trascritto genico di PERK né la sua velocità di degradazione. Quando le cellule sono state trattate con 5-FU, le cellule normali mostravano forti aumenti di PERK, CHOP e caspasi 3 attiva nel tempo, coerenti con la morte cellulare indotta dalla chemioterapia. Al contrario, le cellule prive di ASCC3 non sono riuscite a indurre pienamente queste proteine e la loro risposta di morte è risultata sensibilmente ridotta, contribuendo a spiegare la chemi-resistenza nonostante il maggiore danno al DNA.
Cosa significa per i pazienti
Nel complesso, lo studio delinea ASCC3 come una sorta di alleato interno della chemioterapia nelle cellule del cancro colorettale. Quando ASCC3 è presente, sostiene un metabolismo più incentrato sulla glicolisi, una robusta produzione di serina e un forte segnale di stress del RE attraverso PERK che può spingere le cellule danneggiate verso l’autodistruzione. Quando ASCC3 viene perso, le cellule accumulano più danni genetici ma sopravvivono spostando la produzione di energia verso i mitocondri e smorzando la via di morte PERK–CHOP. Queste intuizioni suggeriscono che i livelli di ASCC3 potrebbero aiutare a prevedere quali tumori colorettali risponderanno bene a farmaci come 5-FU e oxaliplatino, e che mirare al metabolismo o alle risposte di stress alterate dei tumori poveri di ASCC3 potrebbe offrire nuove strategie per superare la chemi-resistenza.
Citazione: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Parole chiave: cancro colorettale, chemi-resistenza, metabolismo cellulare, stress del RE, segnalazione PERK