Clear Sky Science · es
ASCC3 promueve la quimiosensibilidad en células de cáncer colorrectal
Por qué importa esta investigación
La quimioterapia es un tratamiento fundamental para el cáncer colorrectal avanzado, pero muchos tumores acaban aprendiendo a sobrevivir a estos fármacos agresivos. Este estudio explora una proteína poco conocida llamada ASCC3 y revela que, de forma inesperada, hace que las células de cáncer colorrectal sean más vulnerables a los fármacos quimioterápicos habituales. Al desvelar cómo ASCC3 conecta el daño en el ADN, el metabolismo celular y las señales de estrés dentro de la célula, el trabajo apunta a posibles formas nuevas de predecir qué pacientes responderán al tratamiento y cómo podrían neutralizarse los tumores resistentes.
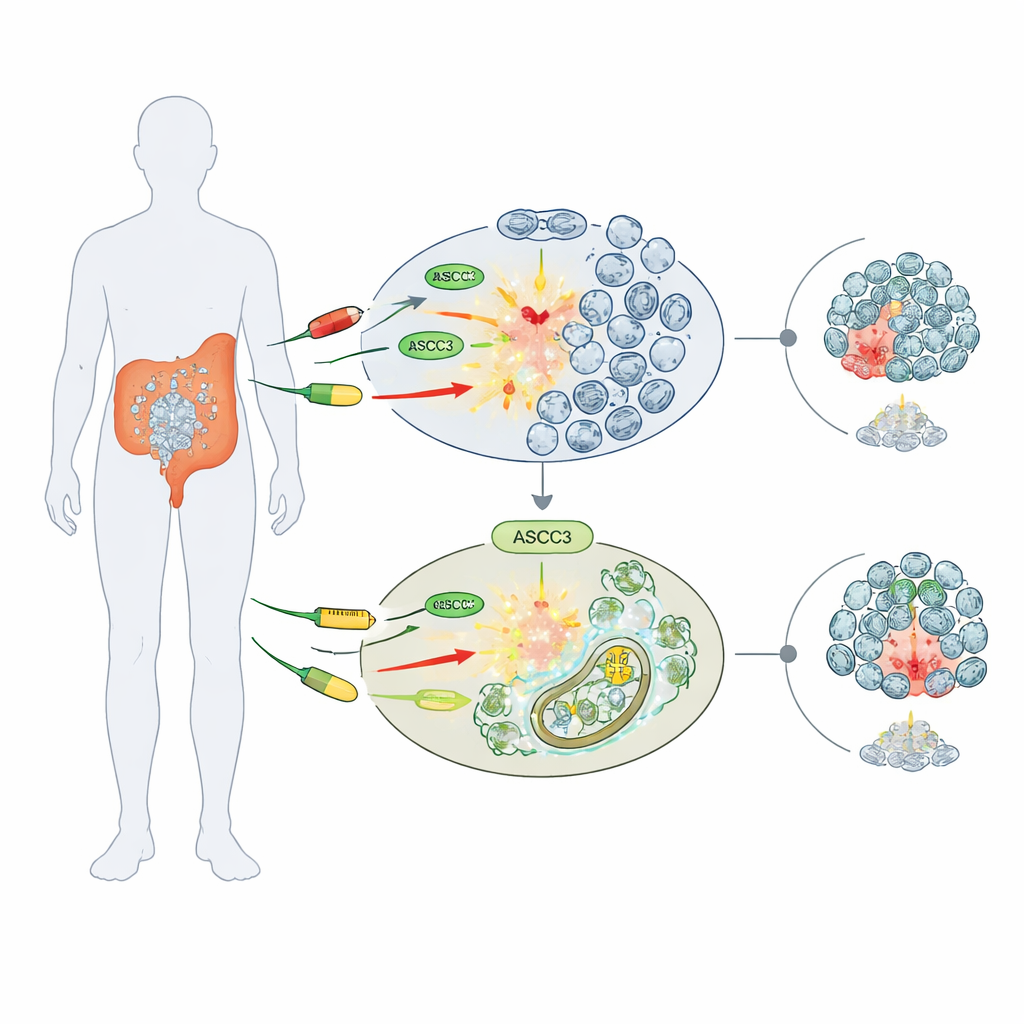
Un guardián de la sensibilidad a los fármacos
Los investigadores se centraron en tres agentes quimioterápicos de uso general que dañan el ADN o bloquean su producción: 5-fluoruracilo (5-FU), cisplatino e hidroxiurea. Trabajando con varias líneas celulares humanas de cáncer colorrectal, compararon células normales con células modificadas genéticamente para carecer de ASCC3. Sorprendentemente, las células sin ASCC3 sobrevivieron mejor a estos fármacos, formando más colonias y manteniendo mayor viabilidad que sus homólogas normales. Este efecto de «quimiorresistencia» fue específico: en células de cáncer óseo (osteosarcoma), eliminar ASCC3 no cambió la sensibilidad a los fármacos, lo que sugiere que su papel depende del tipo de cáncer.
Más daño en el ADN, pero más supervivencia
A primera vista, la mejor supervivencia de las células deficientes en ASCC3 parece paradójica. Trabajos anteriores mostraron que ASCC3 ayuda a las células a manejar la replicación del ADN atascada, evitando la rotura de cromosomas. En este estudio, cuando las células colorrectales se trataron con quimioterapia, la pérdida de ASCC3 condujo a más signos de daño en el ADN: focos nucleares intensos de ADN dañado y fragmentos cromosómicos adicionales llamados micronúcleos. En otras palabras, las células eran genéticamente menos estables, pero eran más difíciles de eliminar. Esta desconexión sugiere que otras vías protectoras, más allá de la reparación simple del ADN, permitían que las células dañadas persistieran.
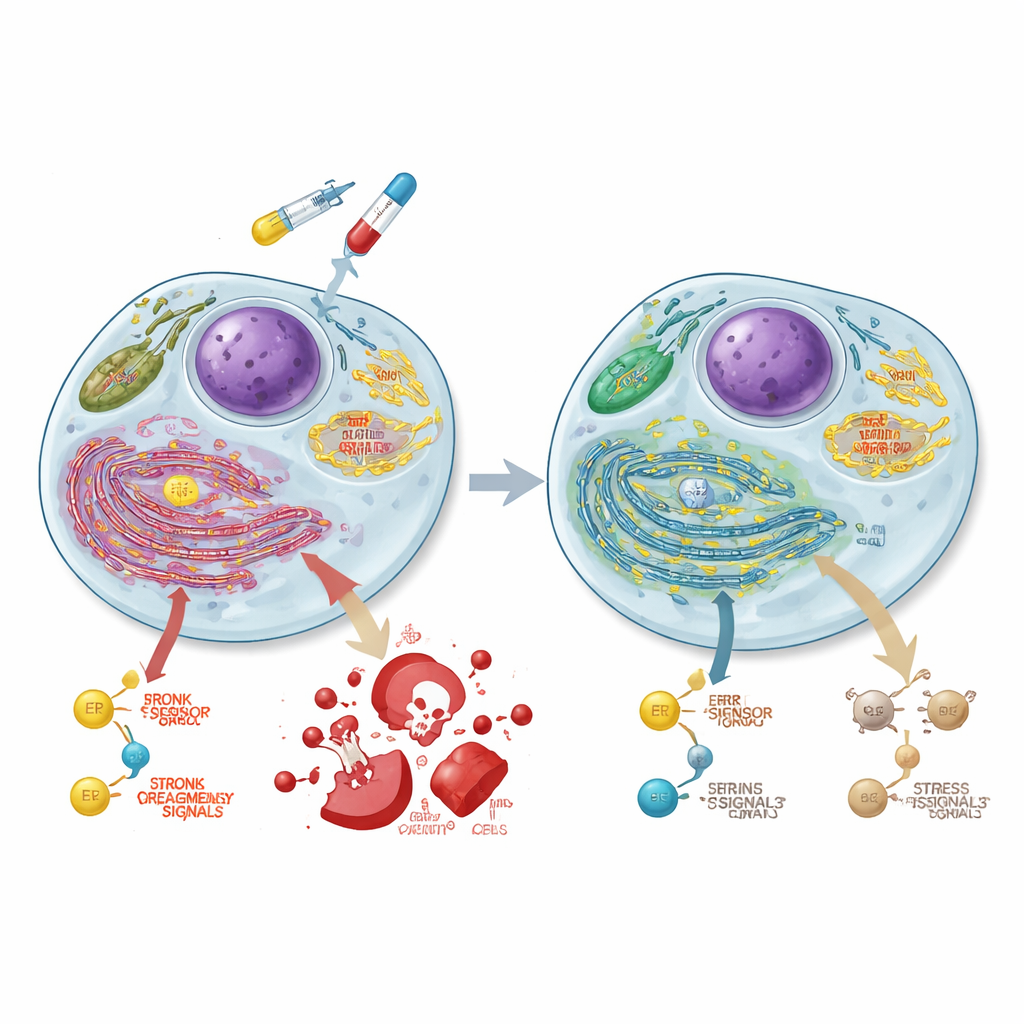
Reconfiguración de cómo las células cancerosas generan energía
Para entender qué más cambia cuando se pierde ASCC3, el equipo midió la actividad génica en todo el genoma. Encontraron que ASCC3 normalmente potencia conjuntos de genes implicados en la degradación de azúcares (glucólisis), un nodo de señalización relacionado con el crecimiento llamado mTORC1 y vías de plegamiento de proteínas en el retículo endoplásmico. Mediante pruebas metabólicas especializadas, mostraron que las células que carecían de ASCC3 se alejaron de la glucólisis y, en su lugar, dependieron en gran medida de sus mitocondrias, las centrales energéticas celulares, aumentando la producción de energía basada en oxígeno. Experimentos con trazadores de glucosa marcados confirmaron que estas células canalizaban más azúcar hacia el ciclo del ácido tricarboxílico (TCA) y aminoácidos relacionados, mientras reducían su uso para ciertos bloques de construcción como alanina y serina. ASCC3 también sostenía la capacidad de la célula para sintetizar serina de novo y proliferar cuando este aminoácido escaseaba, aunque los mecanismos exactos variaron entre líneas celulares.
Atenuando una señal de estrés autodestructiva
El retículo endoplásmico (RE) vigila que las proteínas se plieguen correctamente; cuando se sobrecarga, desencadena respuestas de estrés que pueden ayudar a las células a adaptarse o empujarlas hacia la muerte. Un sensor clave del RE, PERK, puede activar finalmente un programa pro-muerte que implica las proteínas CHOP y caspasa 3. Los investigadores hallaron que ASCC3 es esencial para acumular proteína PERK durante el estrés del RE en células de cáncer colorrectal, aunque no altera el transcrito génico de PERK ni su tasa de degradación. Cuando las células se trataron con 5-FU, las células normales mostraron incrementos marcados en PERK, CHOP y caspasa 3 activa con el tiempo, coherente con la muerte celular inducida por quimioterapia. En contraste, las células deficientes en ASCC3 no lograron inducir plenamente estas proteínas y su respuesta de muerte se redujo notablemente, lo que ayuda a explicar su quimiorresistencia pese al mayor daño en el ADN.
Qué significa esto para los pacientes
En conjunto, el estudio dibuja a ASCC3 como una suerte de aliado interno de la quimioterapia en las células de cáncer colorrectal. Cuando ASCC3 está presente, favorece un metabolismo más orientado a la glucólisis, una producción robusta de serina y una señal de estrés del RE potente a través de PERK que puede conducir a las células dañadas hacia la autodestrucción. Cuando ASCC3 se pierde, las células acumulan más daño genético pero sobreviven al desplazar su producción de energía hacia las mitocondrias y atenuar la vía de muerte PERK–CHOP. Estos hallazgos sugieren que los niveles de ASCC3 podrían ayudar a predecir qué tumores colorrectales responderán bien a fármacos como 5-FU y oxaliplatino, y que dirigir el metabolismo alterado o las respuestas de estrés de los tumores pobres en ASCC3 puede ofrecer nuevas estrategias para vencer la quimiorresistencia.
Cita: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Palabras clave: cáncer colorrectal, quimiorresistencia, metabolismo celular, estrés del RE, señalización PERK