Clear Sky Science · sv
ASCC3 främjar kemokänslighet i kolorektala cancerceller
Varför denna forskning är viktig
Kemoterapi är en grundpelare i behandlingen av avancerad kolorektal cancer, men många tumörer lär sig så småningom att överleva dessa hårda läkemedel. Denna studie undersöker ett mindre känt protein kallat ASCC3 och visar att det oväntat gör kolorektala cancerceller mer sårbara för vanliga cytostatika. Genom att klarlägga hur ASCC3 kopplar samman DNA-skada, cellens metabolism och stressignaler inuti cellen pekar arbetet mot möjliga nya sätt att förutsäga vilka patienter som kommer att svara på behandling — och hur resistenta tumörer kan oskadliggöras.
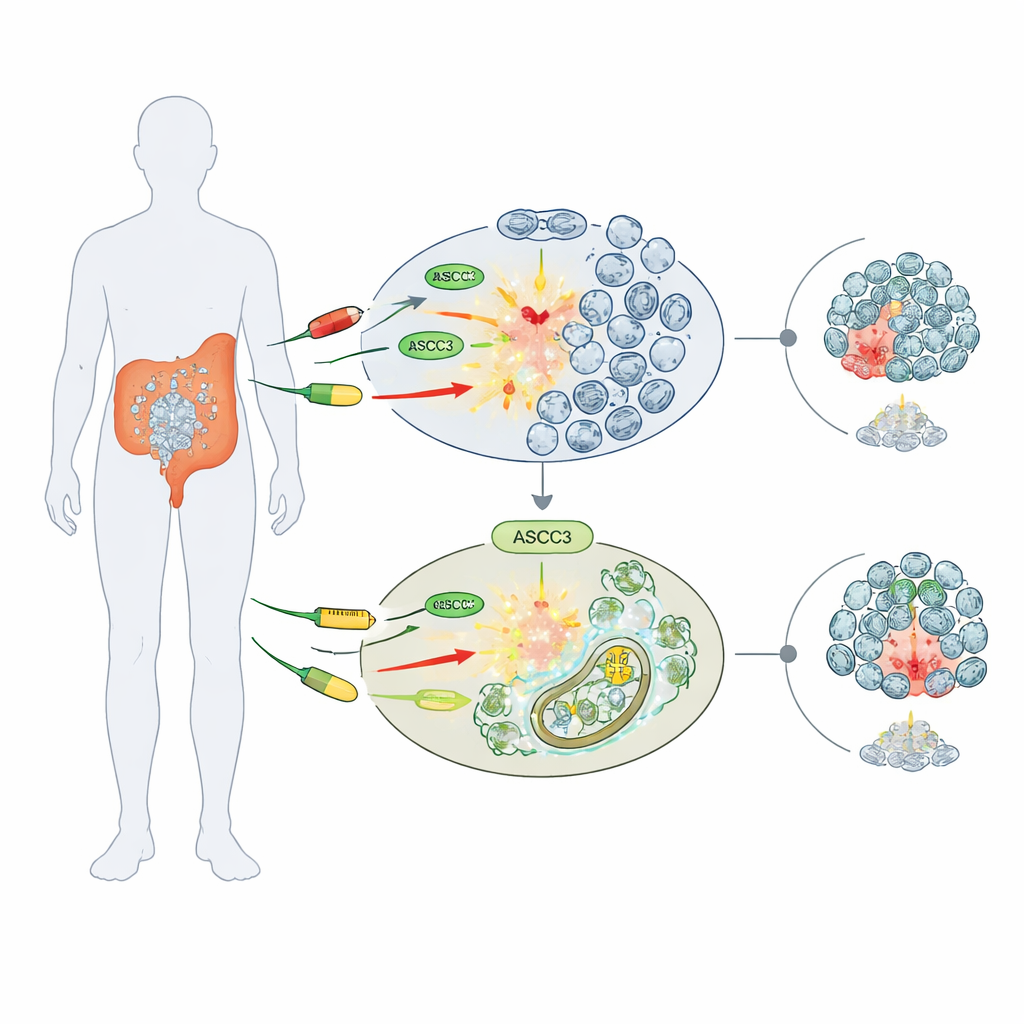
En grindvakt för läkemedelskänslighet
Forskarna fokuserade på tre i stor utsträckning använda kemoterapiläkemedel som skadar DNA eller hindrar dess produktion: 5-fluorouracil (5-FU), cisplatin och hydroxyurea. Med flera humana kolorektala cancercellinjer jämförde de normala celler med celler genetiskt modifierade att sakna ASCC3. Överraskande nog överlevde celler utan ASCC3 dessa läkemedel bättre, bildade fler kolonier och behöll högre livsduglighet än sina normala motsvarigheter. Denna effekt av ”kemoresistens” var specifik: i bencancerceller (osteosarkom) förändrade borttagandet av ASCC3 inte läkemedelskänsligheten, vilket tyder på att dess roll beror på cancerarten.
Mer DNA-skada, men ändå större överlevnad
Vid första anblick verkar den förbättrade överlevnaden hos ASCC3-bristfälliga celler paradoxal. Tidigare arbete visade att ASCC3 hjälper celler hantera avstannad DNA-replikation och förebygga klyvda kromosomer. I denna studie ledde förlust av ASCC3, när kolorektala cancerceller behandlades med kemoterapi, till fler tecken på DNA-skada — starka nukleära fokus av skadat DNA och extra kromosomfragment kallade mikronukleer. Med andra ord var cellerna genetiskt mindre stabila, men svårare att döda. Denna diskrepans tyder på att andra skyddande vägar, bortom enkel DNA-reparation, tillåter de skadade cellerna att bestå.
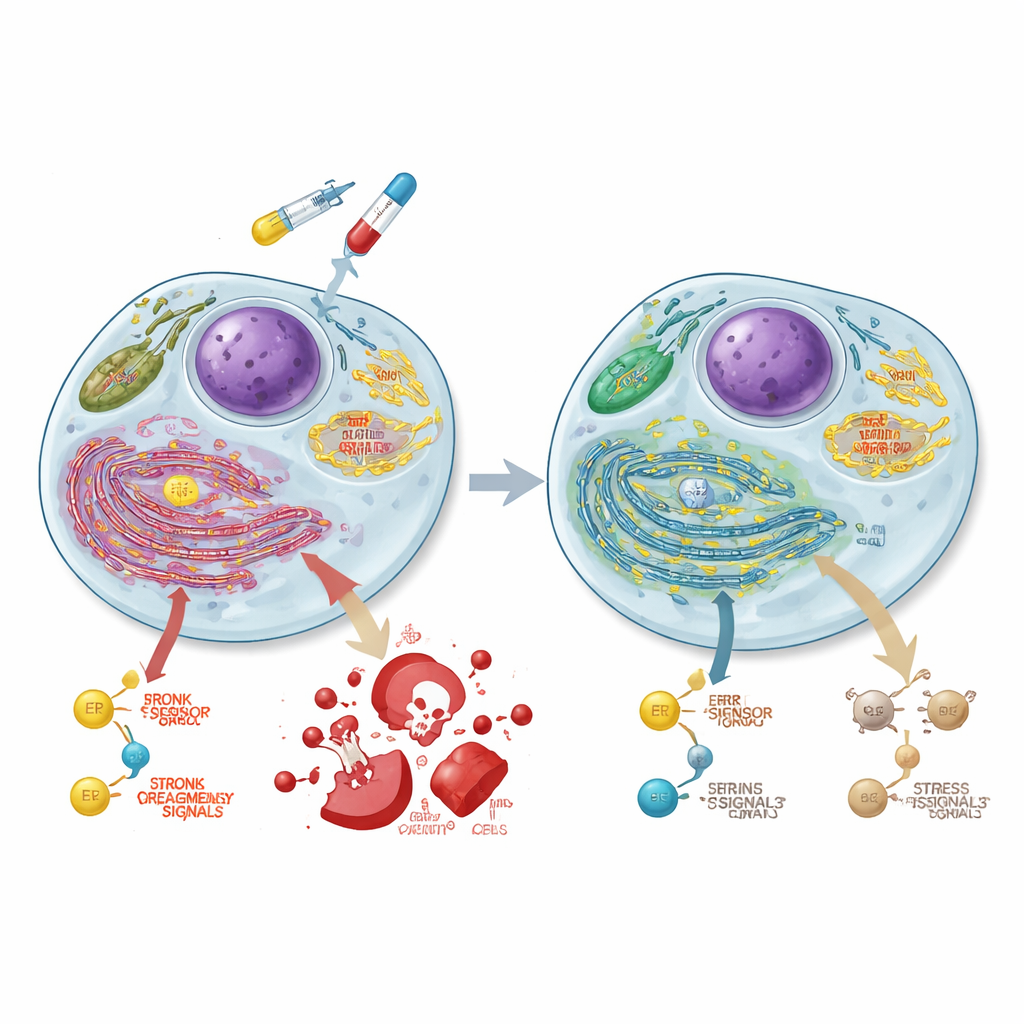
Omsvängning av hur cancerceller skaffar energi
För att förstå vad som mer förändras när ASCC3 försvinner mätte teamet genaktivitet över hela genomet. De fann att ASCC3 normalt stärker grupper av gener involverade i sockernedbrytning (glykolys), en tillväxtrelaterad signalknutpunkt kallad mTORC1, samt proteinfoldningsvägar i det endoplasmatiska retiklet. Med specialiserade metabola tester visade de att celler som saknar ASCC3 rörde sig bort från glykolys och istället lutade sig tungt mot sina mitokondrier, cellens kraftverk, vilket ökade syrebaserad energiproduktion. Spårningsexperiment med märkt glukos bekräftade att dessa celler kanaliserade mer socker in i trikarboxylsyracykeln (TCA) och relaterade aminosyror, samtidigt som användningen för vissa byggstenar som alanin och serin minskade. ASCC3 stödde också cellens förmåga att syntetisera serin från grunden och att växa när denna aminosyra var knapp, även om de exakta mekanismerna varierade mellan cellinjer.
Dämpning av en självdestruktiv stressignal
Det endoplasmatiska retiklet (ER) övervakar om proteiner veckas korrekt; när det överbelastas utlöser det stressreaktioner som antingen hjälper cellerna att anpassa sig eller driver dem mot död. En viktig ER-sensor, PERK, kan så småningom aktivera ett pro-död-program som involverar proteinerna CHOP och kaspas 3. Forskarna fann att ASCC3 är nödvändigt för uppbyggnaden av PERK-protein under ER-stress i kolorektala cancerceller, även om det inte ändrar PERK:s genutsnitt eller dess nedbrytningshastighet. När celler behandlades med 5-FU visade normala celler starka ökningar av PERK, CHOP och aktivt kaspas 3 över tid, i linje med kemoterapidriven celldöd. I kontrast misslyckades ASCC3-bristfälliga celler att fullt ut inducera dessa proteiner, och deras dödsrespons var markant reducerad, vilket hjälper till att förklara deras kemoresistens trots större DNA-skada.
Vad detta betyder för patienterna
Sammantaget framställer studien ASCC3 som en sorts intern allierad till kemoterapin i kolorektala cancerceller. När ASCC3 är närvarande stödjer det en mer glykolysfokuserad metabolism, robust serinsyntes och en stark ER-stressignal via PERK som kan driva skadade celler mot självdestruktion. När ASCC3 försvinner ackumulerar cellerna mer genetisk skada men överlever genom att omdirigera sin energiproduktion mot mitokondrier och dämpa PERK–CHOP-dödsvägen. Dessa insikter tyder på att ASCC3-nivåer skulle kunna hjälpa till att förutsäga vilka kolorektala tumörer som svarar väl på läkemedel som 5-FU och oxaliplatin, och att rikta in sig på den förändrade metabolismen eller stressresponserna hos ASCC3-fattiga tumörer kan erbjuda nya strategier för att övervinna kemoresistens.
Citering: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Nyckelord: kolorektal cancer, kemoresistens, cellmetabolism, ER-stress, PERK-signalering