Clear Sky Science · fr
ASCC3 favorise la chimiosensibilité des cellules de cancer colorectal
Pourquoi cette recherche est importante
La chimiothérapie reste un traitement de référence pour le cancer colorectal avancé, mais de nombreuses tumeurs finissent par apprendre à survivre à ces médicaments agressifs. Cette étude explore une protéine peu connue, ASCC3, et révèle qu’elle rend de manière inattendue les cellules de cancer colorectal plus vulnérables aux médicaments chimiothérapeutiques courants. En montrant comment ASCC3 relie les dommages à l’ADN, le métabolisme cellulaire et les signaux de stress intracellulaires, ce travail suggère de nouvelles façons possibles de prédire quels patients répondront au traitement — et comment neutraliser les tumeurs résistantes.
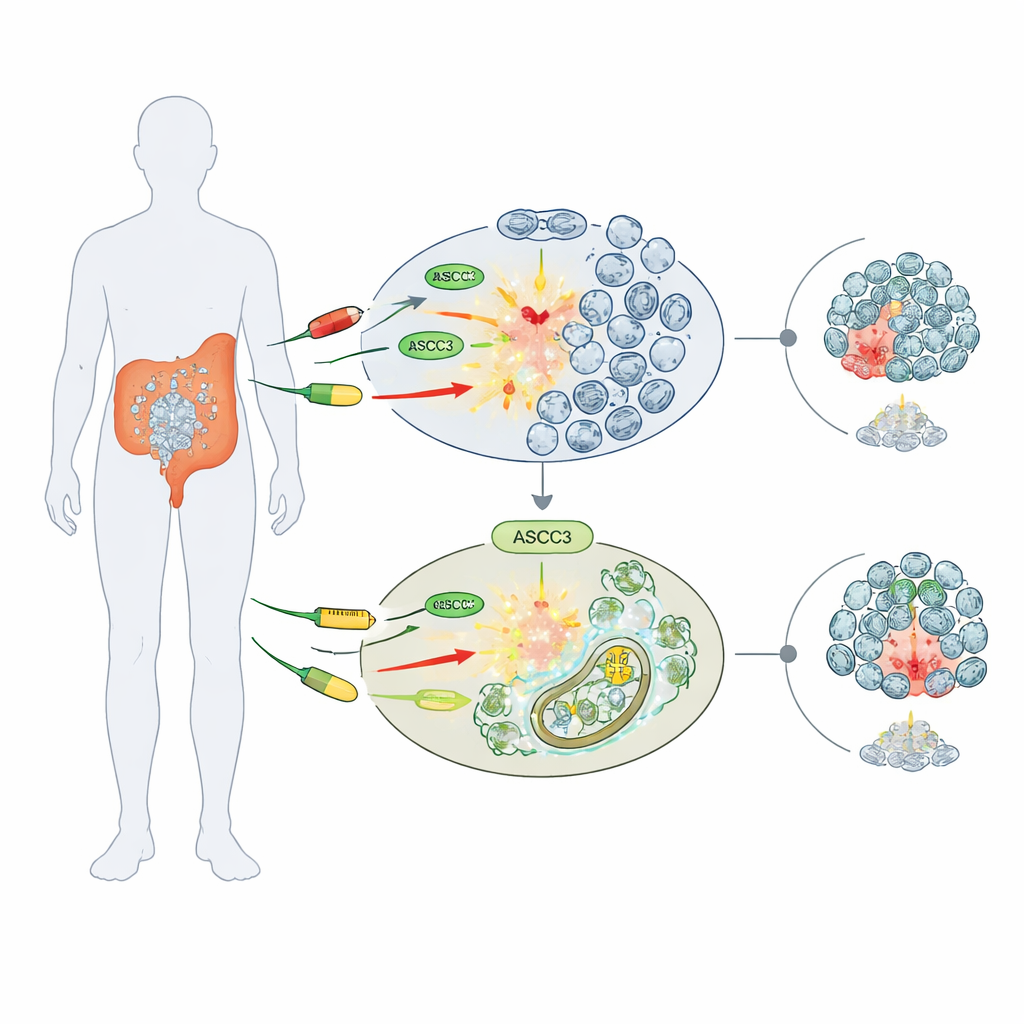
Un gardien de la sensibilité aux médicaments
Les chercheurs se sont concentrés sur trois agents chimiothérapeutiques largement utilisés qui endommagent l’ADN ou bloquent sa synthèse : le 5-fluorouracile (5-FU), le cisplatine et l’hydroxyurée. En travaillant sur plusieurs lignées cellulaires humaines de cancer colorectal, ils ont comparé des cellules normales à des cellules génétiquement modifiées pour ne pas exprimer ASCC3. De façon surprenante, les cellules dépourvues d’ASCC3 survivaient mieux à ces traitements, formant plus de colonies et conservant une viabilité plus élevée que leurs homologues normales. Cet effet de « chimiorésistance » était spécifique : dans des cellules de cancer osseux (ostéosarcome), la suppression d’ASCC3 n’altérait pas la sensibilité aux médicaments, ce qui suggère que son rôle dépend du type de cancer.
Plus de dommages à l’ADN, et pourtant plus de survie
À première vue, la meilleure survie des cellules déficientes en ASCC3 paraît paradoxale. Des travaux antérieurs montraient qu’ASCC3 aide les cellules à faire face à la réplication de l’ADN bloquée, en évitant la rupture des chromosomes. Dans cette étude, lorsque les cellules de cancer colorectal ont été traitées par chimiothérapie, la perte d’ASCC3 entraînait davantage de signes de dommages à l’ADN — des foyers nucléaires intenses d’ADN endommagé et des fragments chromosomiques supplémentaires appelés micronoyaux. Autrement dit, les cellules étaient génétiquement moins stables, mais plus difficiles à tuer. Cette dissociation suggère que d’autres voies protectrices, au-delà de la simple réparation de l’ADN, permettaient à ces cellules endommagées de persister.
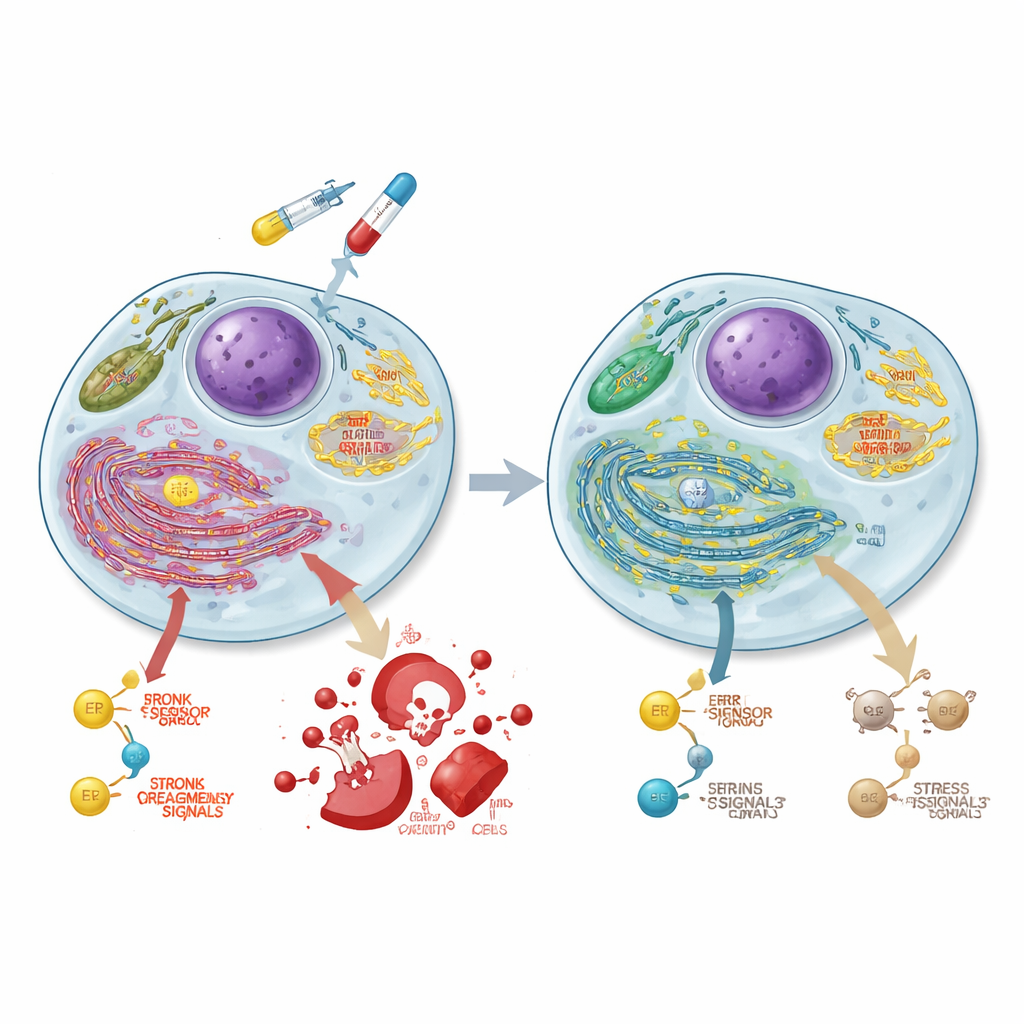
Reprogrammation de la production d’énergie des cellules cancéreuses
Pour comprendre ce qui changeait encore quand ASCC3 était perdu, l’équipe a mesuré l’activité génique sur l’ensemble du génome. Ils ont constaté qu’ASCC3 stimule normalement des ensembles de gènes impliqués dans la dégradation du glucose (glycolyse), dans un centre de signalisation lié à la croissance appelé mTORC1, et dans les voies de repliement des protéines du réticulum endoplasmique. À l’aide de tests métaboliques spécialisés, ils ont montré que les cellules dépourvues d’ASCC3 s’éloignaient de la glycolyse et s’appuyaient plutôt fortement sur leurs mitochondries, les centrales énergétiques de la cellule, augmentant la production d’énergie basée sur l’oxygène. Des expériences de suivi avec du glucose marqué ont confirmé que ces cellules acheminaient davantage de sucre vers le cycle tricarboxylique (TCA) et les acides aminés associés, tout en réduisant son utilisation pour certains éléments de construction comme l’alanine et la sérine. ASCC3 soutenait aussi la capacité de la cellule à synthétiser la sérine de novo et à croître lorsque cet acide aminé manquait, bien que les mécanismes exacts varient selon les lignées cellulaires.
Atténuation d’un signal de stress auto-destructeur
Le réticulum endoplasmique (RE) surveille le repliement correct des protéines ; lorsqu’il est surchargé, il déclenche des réponses de stress qui peuvent soit aider la cellule à s’adapter, soit la pousser vers la mort. Un senseur clé du RE, PERK, peut à terme activer un programme pro-apoptotique impliquant les protéines CHOP et la caspase 3. Les chercheurs ont découvert qu’ASCC3 est essentiel pour accumuler la protéine PERK lors du stress du RE dans les cellules de cancer colorectal, bien qu’elle n’altère pas le niveau de l’arnm de PERK ni son taux de dégradation. Lorsque les cellules ont été traitées par le 5-FU, les cellules normales montraient au fil du temps de fortes augmentations de PERK, CHOP et de la caspase 3 active, concordant avec la mort cellulaire induite par la chimiothérapie. En revanche, les cellules déficientes en ASCC3 n’ont pas réussi à induire pleinement ces protéines, et leur réponse de mort était nettement réduite, ce qui aide à expliquer leur chimiorésistance malgré des dommages à l’ADN plus importants.
Ce que cela signifie pour les patients
Pris ensemble, les résultats dépeignent ASCC3 comme une sorte d’allié interne de la chimiothérapie dans les cellules de cancer colorectal. Lorsque ASCC3 est présent, il favorise un métabolisme davantage centré sur la glycolyse, une production robuste de sérine et un signal de stress du RE fort via PERK, qui peut pousser les cellules endommagées vers l’autodestruction. Lorsque ASCC3 est perdu, les cellules accumulent plus de dommages génétiques mais survivent en basculant leur production d’énergie vers les mitochondries et en atténuant la voie de mort PERK–CHOP. Ces conclusions suggèrent que le niveau d’ASCC3 pourrait aider à prédire quelles tumeurs colorectales répondront bien à des médicaments comme le 5-FU et l’oxaliplatine, et que cibler le métabolisme ou les réponses au stress altérés des tumeurs pauvres en ASCC3 pourrait offrir de nouvelles stratégies pour surmonter la chimiorésistance.
Citation: Tu, A., Martyn, R.D.C., Cui, S. et al. ASCC3 promotes chemosensitivity in colorectal cancer cells. Sci Rep 16, 13863 (2026). https://doi.org/10.1038/s41598-026-43173-9
Mots-clés: cancer colorectal, chimiorésistance, métabolisme cellulaire, stress du RE, signalisation PERK