Clear Sky Science · tr
Yüksek boyutlu protein belirteç verilerinde imputation ve özellik seçiminin hayatta kalma risk tahminini iyileştirmesi
Hastalar için neden önemli
Hekimler, bir kişinin kanserinin nasıl davranacağını—tekrar edip etmeyeceğini veya yayılma eğiliminde olup olmayacağını—öngörmek ve tedaviyi buna göre kişiselleştirmek için giderek daha fazla kan testine başvurmak istiyor. Modern protein testleri aynı anda yüzlerce molekülü ölçebiliyor, ancak elde edilen veriler dağınık, eksik değerlerle dolu ve hasta sayısından çok daha fazla ölçüm içeriyor. Bu çalışma, böyle karmaşık verileri dikkatle temizleyip analiz etmenin, hayatta kalma tahminlerini daha güvenilir ve klinisyenlerin yorumlaması için daha anlaşılır kıldığını gösteriyor.
Düzgün olmayan laboratuvar sonuçlarını yararlı sinyallere dönüştürmek
Yazarlar, tümördeki büyümeyi, bağışıklık sisteminin yanıtını ve hastanın tedaviye tepkisini yansıtabilen kan protein belirteçlerine odaklanıyor. Gerçek dünyadaki çalışmalarda bu belirteçler zaman içinde tekrarlı olarak ölçülüyor, ancak teknik sorunlar veya hastaların çalışmayı bırakması nedeniyle bazı ölçümler genellikle eksik oluyor. Eksik kayıtları basitçe atmak veya boşlukları kaba ortalamalarla doldurmak, özellikle küçük hasta gruplarında yüzlerce protein izleniyorsa sonuçları ciddi şekilde çarpıtabilir. Bu nedenle çalışma, yanıltıcı kestirmelerden kaçınırken mümkün olduğunca fazla bilgiyi koruyacak adım adım bir analiz hattı oluşturuyor.
Sonuçlara bakmadan boşlukları doldurmak
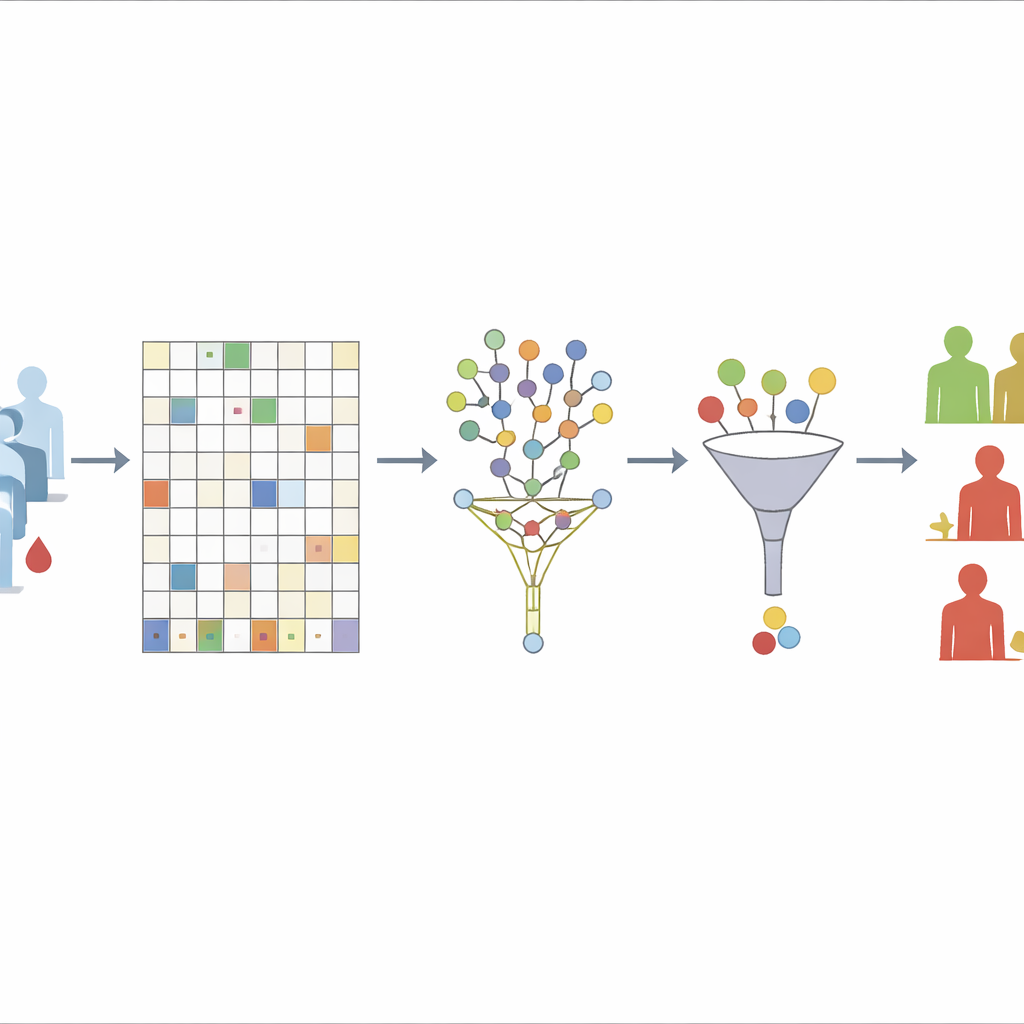
Ekip tarafından ele alınan ilk zorluk eksik veriler. Öncelikle, hastaların %30'undan fazlasında eksik olan yalnızca o proteinleri eliyorlar; bunun kararlılık ile bilgi kaybı arasında iyi bir denge olduğunu gösteriyorlar. Kalan proteinler için, eksik değerleri tahmin etmek amacıyla "denetimsiz" bir rastgele orman yaklaşımı kullanıyorlar. Özetle, algoritma proteinlerin birbirleriyle nasıl ilişkilendiğine dayanarak—kimlerin nüks yaptığına veya metastaz geliştirdiğine bakmadan—birçok karar ağacı tekrar tekrar kuruyor. Birçok ağaçta birbirine benzer görünen örnekler komşu olarak kabul ediliyor; bu komşulardaki bilinen değerler boşlukları doldurmak için kullanılıyor. Bu adımda sağkalım sonuçlarını kasıtlı olarak dışlayarak yazarlar, veri temizleme sürecinin yanıtı kazara veriye dahil etmesinin önüne geçmiş oluyorlar.
Yüzlerce belirteci anlamlı birkaç taneye indirgemek
Tamamlanmış protein tablosu ile bir sonraki adım, hangi belirteçlerin gerçekten nüks veya metastaz için geçen zamanı tahmin etmede önemli olduğunu belirlemek. Yazarlar önce zayıf öngörücüleri sıfıra doğru çekip daha güçlü olanları koruyan bir teknik kullanıyor; bu, en bilgilendirici proteinlere yalnızca geçit veren bir eleğe benziyor. Bu yöntemin korele belirteç gruplarını veya ince doğrusal olmayan desenleri kaçırabileceği için, hayatta kalma verilerine dayalı çok sayıda rastgeleleştirilmiş karar ağacına dayanan ikinci bir araçla kalanlar yeniden inceleniyor. Bu ikinci aşama aynı regresyonu yeniden uydurmuyor; bunun yerine her bir belirtecin ağaçların hastaları farklı sonuçlara göre ayırmasında ne sıklıkta yardımcı olduğuna puan veriyor. Sürekli olarak ağaçların üst sıralarında görünen belirteçler daha kararlı ve önemli kabul ediliyor.
Seçilen belirteçlerden hasta düzeyinde risk gruplarına
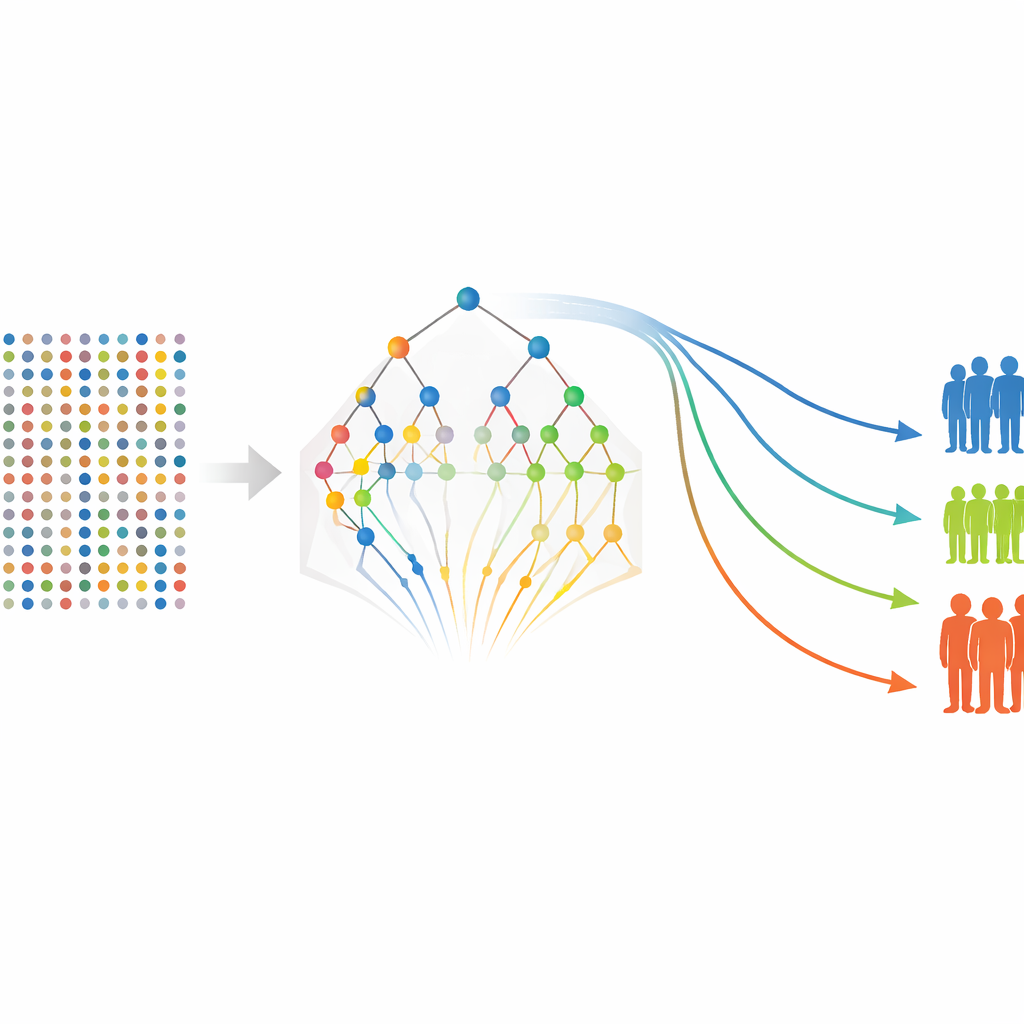
Düzeltilmiş bir protein listesiyle yazarlar, her bir belirtecin—ve tümör evresi gibi bazı klinik özelliklerin—nükssüz veya uzak yayılmasız kalma olasılıklarıyla nasıl ilişkili olduğunu tahmin etmek için daha geleneksel sağkalım modellerine geri dönüyor. Nükssüz sağkalım ve metastazsız sağkalım için ayrı modeller kuruyor, ardından her hasta için protein düzeyleri ve klinik özelliklere dayalı bir risk puanı hesaplıyorlar. Hastalar düşük, orta ve yüksek risk kategorilerine ayrılıyor ve standart sağkalım eğrileri, çalışma sadece 80 hasta içerse bile bu gruplar arasında belirgin ayrım gösteriyor. FGF-5, Neuropilin-2 ve Siglec-5 ile ilişkili ölçümler de dahil olmak üzere birkaç protein, yineleyen şekilde daha kötü sonuçların güçlü göstergeleri olarak ortaya çıkıyor; bazı belirteçler ise koruyucu görünmekte.
Zorlu koşullar altında hattı test etmek
Yaklaşımlarının bu küçük veri kümesine aşırı uyumdan ibaret olmadığını kontrol etmek için araştırmacılar, yaygın model varsayımlarının güçlü ihlallerini ve farklı eksik veri desenlerini taklit eden yüksek boyutlu protein çalışmalarını andıran kapsamlı bilgisayar simülasyonları çalıştırıyor. Bu stres testlerinde, aynı analiz hattı gerçekten önemli olan küçük bir belirteç setini belirlemeye ve düşük ile yüksek risk gruplarını ayırmaya devam ediyor; klasik sağkalım modellerinin arkasındaki olağan varsayımlar geçerli olmadığında bile. Ayrıca eksik veri eşiklerini değiştiriyorlar ve anahtar belirteçlerin ile genel sonuçların büyük ölçüde sabit kaldığını gösteriyorlar.
İleriye dönük anlamı
Yepyeni bir istatistik hilesi icat etmek yerine, bu çalışma karmaşık protein ölçümlerini klinik açıdan anlamlı risk tahminlerine dönüştürmek için pratik bir tarif derleyip doğruluyor. Eksik değerleri dikkatle ele alarak, kararlı bir belirteç setine odaklanmayı daraltarak ve güçlü iç doğrulama ve simülasyonlarla performansı kontrol ederek, bu hat şeffaf bir şekilde umut verici belirteçleri tanımlamak ve küçük, veri açısından zengin kanser çalışmalarında risk puanları oluşturmak için bir yol sunuyor. Yazarlar, belirli proteinlerin rutin klinik testler olarak doğrulanması için daha büyük, bağımsız kohortların hâlâ gerekli olduğunu vurguluyor; ancak önerdikleri çerçeve gelecekte belirteç odaklı hayatta kalma araştırmaları için sağlam, yeniden kullanılabilir bir şablon sağlıyor.
Atıf: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Anahtar kelimeler: kanser belirteçleri, hayatta kalma tahmini, proteomik, eksik veri, hedefe yönelik tıp