Clear Sky Science · ru
Повышение точности прогнозирования риска выживания с помощью иммутации и отбора признаков в высокоразмерных данных белковых биомаркеров
Почему это важно для пациентов
Врачи всё чаще хотят использовать анализы крови, чтобы предсказать, как будет вести себя рак — вернётся ли он или распространится — и подбирать лечение соответственно. Современные тесты белков измеряют сотни молекул одновременно, но получаемые данные часто бывают «грязными»: с многочисленными пропусками и с большим количеством измерений по сравнению с числом пациентов. В этой работе показано, как аккуратно очистить и проанализировать такие сложные данные, чтобы прогнозы выживания были более надёжными и понятными клиницистам.
Превращение небрежных лабораторных результатов в полезные сигналы
Авторы сосредотачиваются на белковых биомаркерах — молекулах в крови, уровни которых могут указывать на то, как растёт опухоль, как реагирует иммунная система и как пациент переносит терапию. В реальных исследованиях эти маркеры измеряются неоднократно во времени, но некоторые показания часто отсутствуют из‑за технических проблем или выбывания пациентов. Простое удаление неполных записей или заполнение пробелов грубыми средними значениями может серьёзно исказить результаты, особенно когда сотни белков отслеживают в небольшой группе пациентов. Поэтому в исследовании построен пошаговый аналитический конвейер, призванный сохранить как можно больше информации и одновременно избежать вводящих в заблуждение упрощений.
Заполнение пробелов без «подсматривания» за исходами
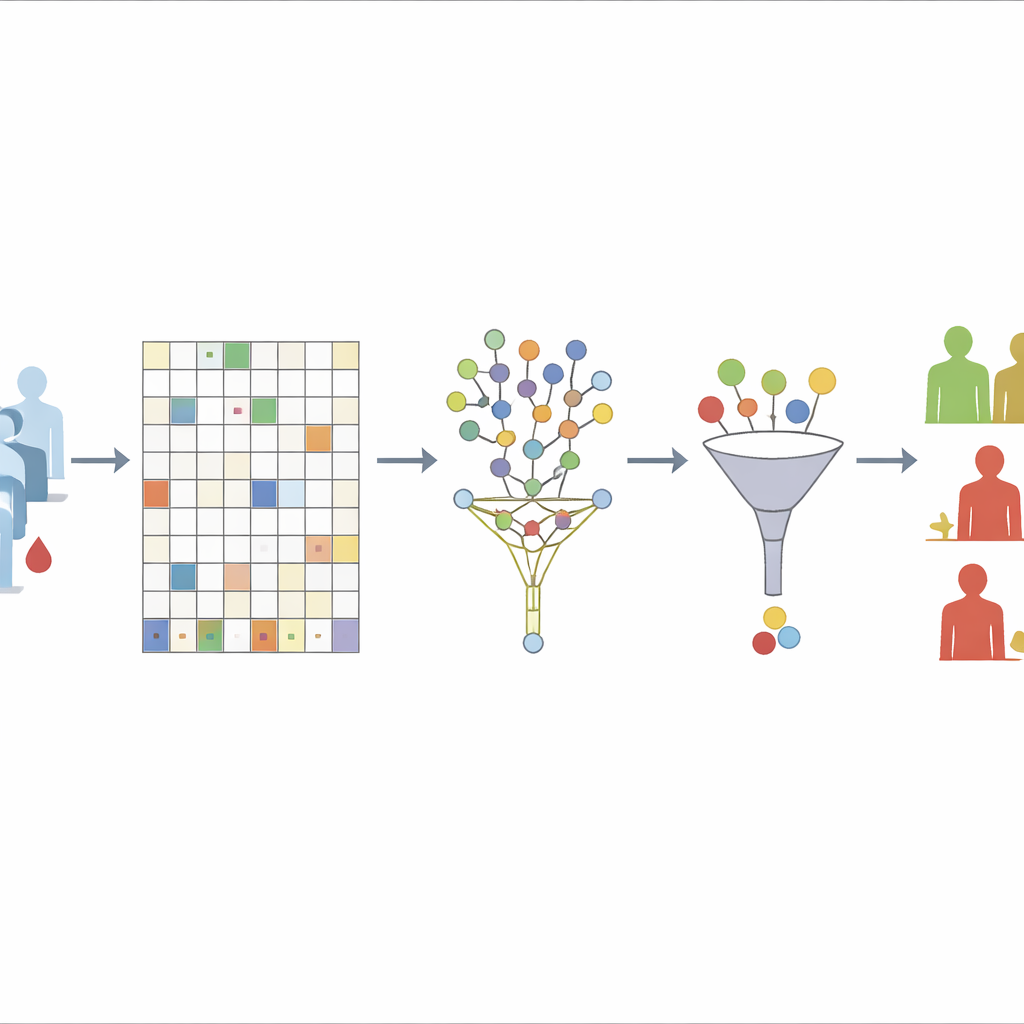
Первая задача, с которой справляется команда, — это пропущенные данные. Они начинают с удаления только тех белков, которые отсутствуют более чем у 30% пациентов — уровень, который, по их показаниям, обеспечивает хороший баланс между стабильностью и потерей информации. Для оставшихся белков используется «несупервайзед» подход на основе случайного леса для восстановления пропусков. По сути, алгоритм многократно строит множество деревьев решений, опираясь только на взаимосвязи между белками, а не на то, у кого был рецидив или метастаз. Образцы, которые часто выглядят похожими во многих деревьях, рассматриваются как соседи; известные значения у этих соседей затем используются для заполнения пропусков. Целенаправленное исключение исходов выживания из этого шага позволяет авторам избежать непреднамеренного «впекания» ответа в процесс очистки данных.
Сужение сотен маркеров до значимого малого числа
Когда таблица белков заполнена, следующий шаг — выбрать маркеры, действительно важные для прогнозирования времени до рецидива или метастазирования. Сначала авторы используют метод, который сжимает слабые предикторы к нулю, сохраняя более сильные — по сути, действуя как сито, через которое проходят только наиболее информативные белки. Поскольку этот метод может пропустить связанные группы маркеров или тонкие нелинейные закономерности, далее они повторно исследуют оставшиеся признаки с помощью второго инструмента на основе множества рандомизированных деревьев, специально настроенных для данных о выживании. Эта вторая стадия не перестраивает ту же регрессию, а оценивает, как часто каждый маркер помогает деревьям разделять пациентов с разными исходами. Маркеры, которые стабильно появляются в верхних узлах деревьев, считаются более устойчивыми и важными.
От отобранных маркеров к группам риска на уровне пациента
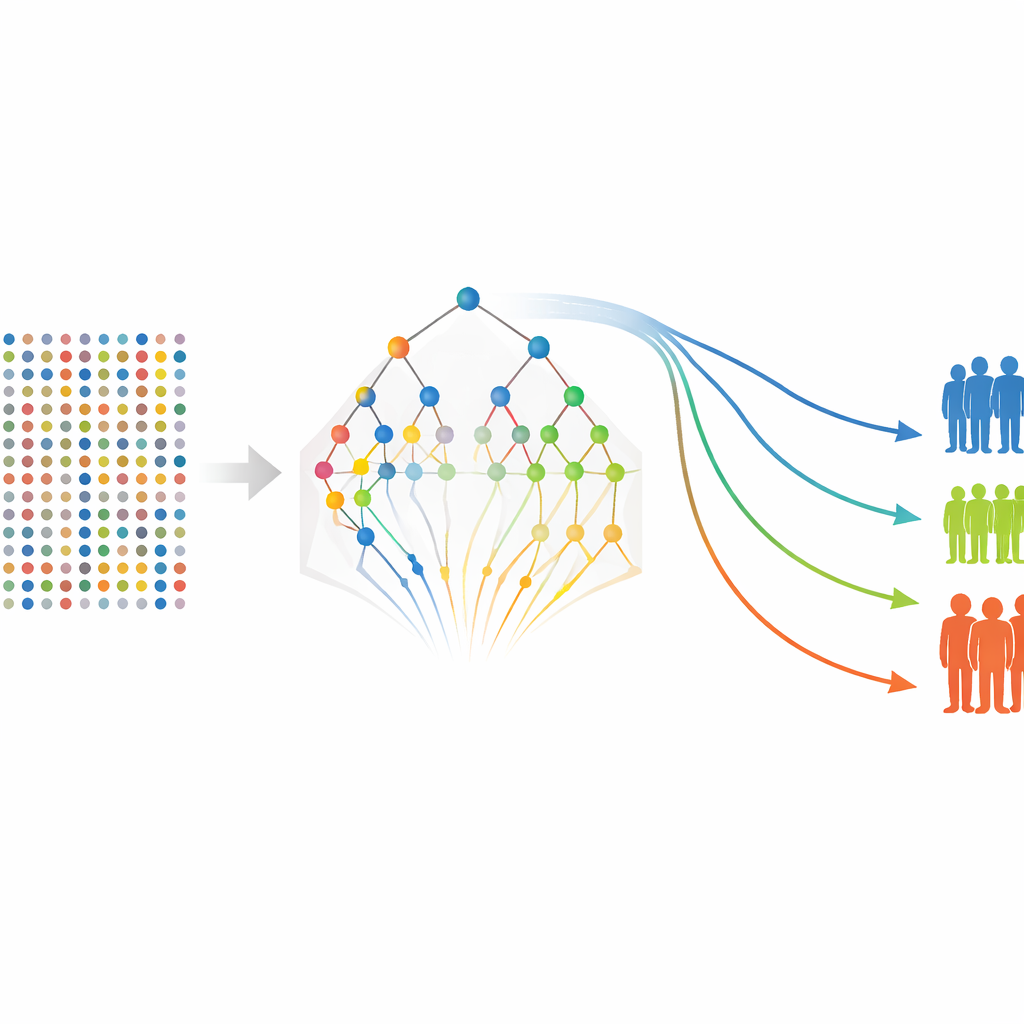
Имея уточнённый список белков, авторы возвращаются к более традиционным моделям выживания, чтобы оценить, как каждый маркер — и некоторые клинические признаки, такие как стадия опухоли — связаны с шансом оставаться свободным от рецидива или отдалённого распространения. Модели строят отдельно для выживания без рецидива и выживания без метастаз, затем вычисляют риск‑скор для каждого пациента на основе уровня белков и клинических характеристик. Пациентов группируют на низко-, средне- и высокорисковые категории, и стандартные кривые выживания показывают чёткое разделение между этими группами, несмотря на то, что в исследовании всего 80 пациентов. Несколько белков, включая FGF‑5, Neuropilin‑2 и показатели, связанные с Siglec‑5, регулярно выявляются как сильные индикаторы худших исходов, в то время как некоторые маркеры оказываются защитными.
Тестирование конвейера в жёстких условиях
Чтобы убедиться, что их подход не просто подгоняет модель под маленький набор данных, исследователи проводят обширные компьютерные симуляции, имитирующие высокоразмерные белковые исследования со значительными нарушениями обычных предпосылок моделирования и с разными схемами пропуска данных. В этих стресс‑тестах тот же конвейер по‑прежнему выявляет компактный набор действительно важных маркеров и разделяет низко‑ и высокорисковые группы, даже когда стандартные предпосылки классических моделей выживания не выполняются. Они также меняют пороги по пропущенным данным и показывают, что ключевые маркеры и общие выводы в основном остаются стабильными.
Что это значит для дальнейшей работы
Вместо изобретения нового статистического трюка эта работа собирает и верифицирует практический рецепт превращения сложных белковых измерений в клинически значимые прогнозы рисков. За счёт аккуратной обработки пропусков, сужения фокуса до устойчивого набора биомаркеров и проверки производительности с помощью надёжной внутренней валидации и симуляций, конвейер предлагает прозрачный способ выявления перспективных маркеров и построения скоринговых систем в небольших, но насыщенных данными онкологических исследованиях. Авторы подчёркивают, что для утверждения конкретных белков в качестве рутинных клинических тестов всё ещё требуются большие независимые когорты, но их подход даёт прочную, пригодную для повторного использования схему для будущих исследований биомаркер‑ориентированного прогнозирования выживания.
Цитирование: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Ключевые слова: биомаркеры рака, прогнозирование выживания, протеомика, пропущенные данные, персонализированная медицина