Clear Sky Science · pl
Poprawa przewidywania ryzyka przeżycia poprzez imputację i selekcję cech w wysokowymiarowych danych białkowych biomarkerów
Dlaczego to ma znaczenie dla pacjentów
Lekarze coraz częściej chcą korzystać z badań krwi, aby przewidzieć, jak prawdopodobnie zachowa się nowotwór — czy nawróci lub da przerzuty — i odpowiednio dopasować leczenie. Nowoczesne testy białkowe mogą jednocześnie mierzyć setki cząsteczek, ale uzyskane dane są chaotyczne, pełne braków i zawierają znacznie więcej pomiarów niż pacjentów. Artykuł pokazuje, jak starannie oczyszczać i analizować takie złożone dane, aby prognozy przeżycia były bardziej wiarygodne i łatwiejsze do interpretacji przez klinicystów.
Jak przekształcić nieporządne wyniki badań w użyteczne sygnały
Autorzy koncentrują się na białkowych biomarkerach, cząsteczkach we krwi, których poziomy mogą wskazywać, jak rozwija się guz, jak reaguje układ odpornościowy i jak pacjent reaguje na terapię. W badaniach typu „real world” markery te są mierzone wielokrotnie w czasie, ale niektóre odczyty często brakują z powodu problemów technicznych lub wycofania pacjentów z badania. Proste odrzucenie niepełnych rekordów lub wypełnianie luk grubymi średnimi może poważnie zniekształcić wyniki, szczególnie gdy setki białek są śledzone w niewielkiej grupie pacjentów. Dlatego badanie buduje krok po kroku pipeline analityczny zaprojektowany tak, by zachować jak najwięcej informacji, unikając jednocześnie mylących uproszczeń.
Wypełnianie luk bez podglądania wyników
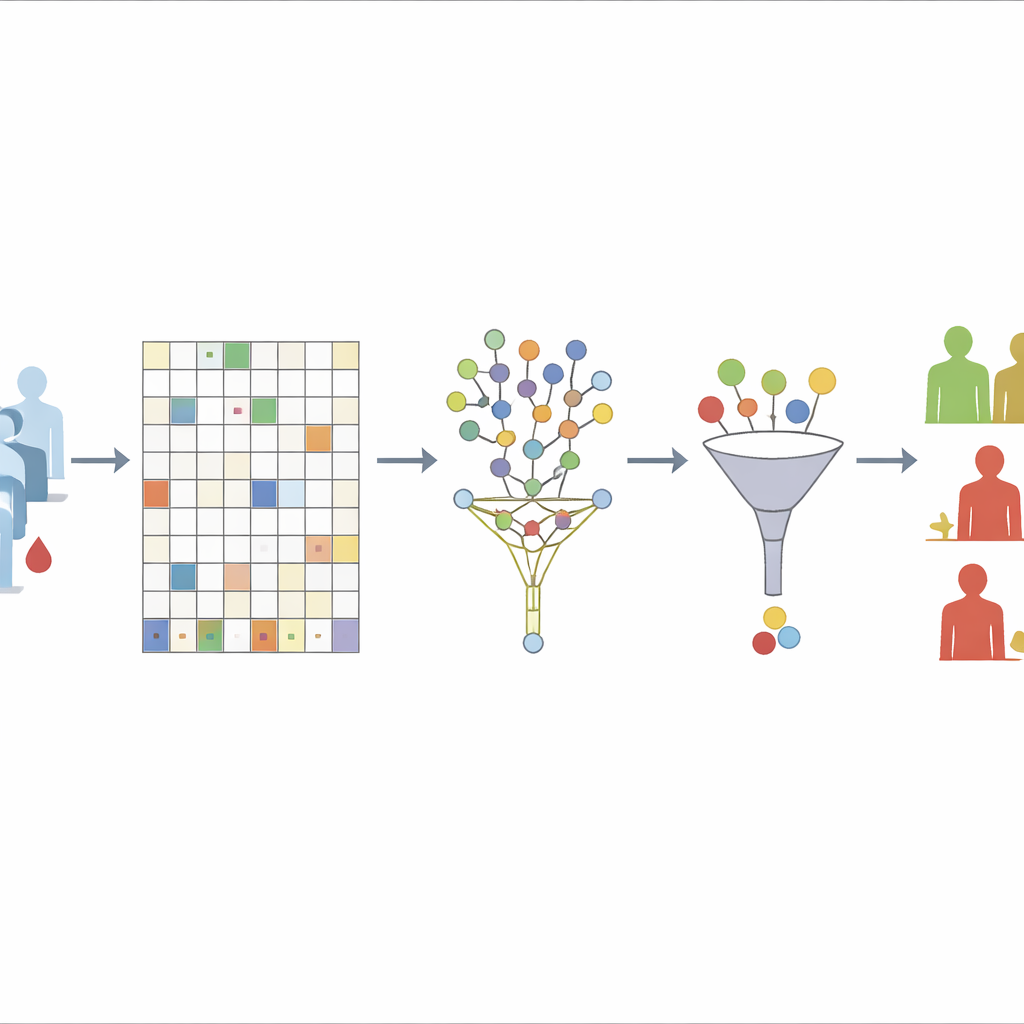
Pierwszym wyzwaniem, które zespół podejmuje, są brakujące dane. Zaczynają od odrzucenia tylko tych białek, które brakują u ponad 30% pacjentów — poziomu, który pokazują jako dobry kompromis między stabilnością a utratą informacji. Dla pozostałych białek stosują „nadzorowane” podejście z wykorzystaniem lasu losowego (random forest) w trybie niesuperwizowanym do oszacowania brakujących wartości. W istocie algorytm wielokrotnie buduje wiele drzew decyzyjnych wyłącznie na podstawie tego, jak białka odnoszą się do siebie nawzajem, a nie na podstawie tego, kto doznał nawrotu czy rozwoju przerzutów. Próbki, które często wyglądają podobnie w wielu drzewach, traktowane są jako sąsiedzi; znane wartości w tych sąsiadach służą następnie do wypełnienia luk. Celowe wyłączenie wyników przeżycia z tego etapu pozwala autorom uniknąć przypadkowego „wbudowania” odpowiedzi w proces oczyszczania danych.
Zawężenie setek markerów do znaczącej garstki
Gdy tabela białkowa jest kompletna, kolejnym krokiem jest decyzja, które markery naprawdę mają znaczenie dla przewidywania czasu do nawrotu lub przerzutów. Autorzy najpierw stosują technikę, która kurczy słabe predyktory w kierunku zera, pozostawiając silniejsze — działając w praktyce jak sito, przez które przechodzą tylko najbardziej informatywne białka. Ponieważ ta metoda może pominąć grupy skorelowanych markerów lub subtelne nieliniowe wzorce, ponownie analizują wyłonione kandydatury drugim narzędziem opartym na wielu zrandomizowanych drzewach decyzyjnych dostosowanych do danych przeżycia. Ten drugi etap nie dopasowuje ponownie tej samej regresji, lecz ocenia, jak często każdy marker pomaga drzewom rozdzielić pacjentów o różnych wynikach. Markery, które konsekwentnie pojawiają się blisko korzeni drzew, uznawane są za bardziej stabilne i istotne.
Od wybranych markerów do grup ryzyka na poziomie pacjenta
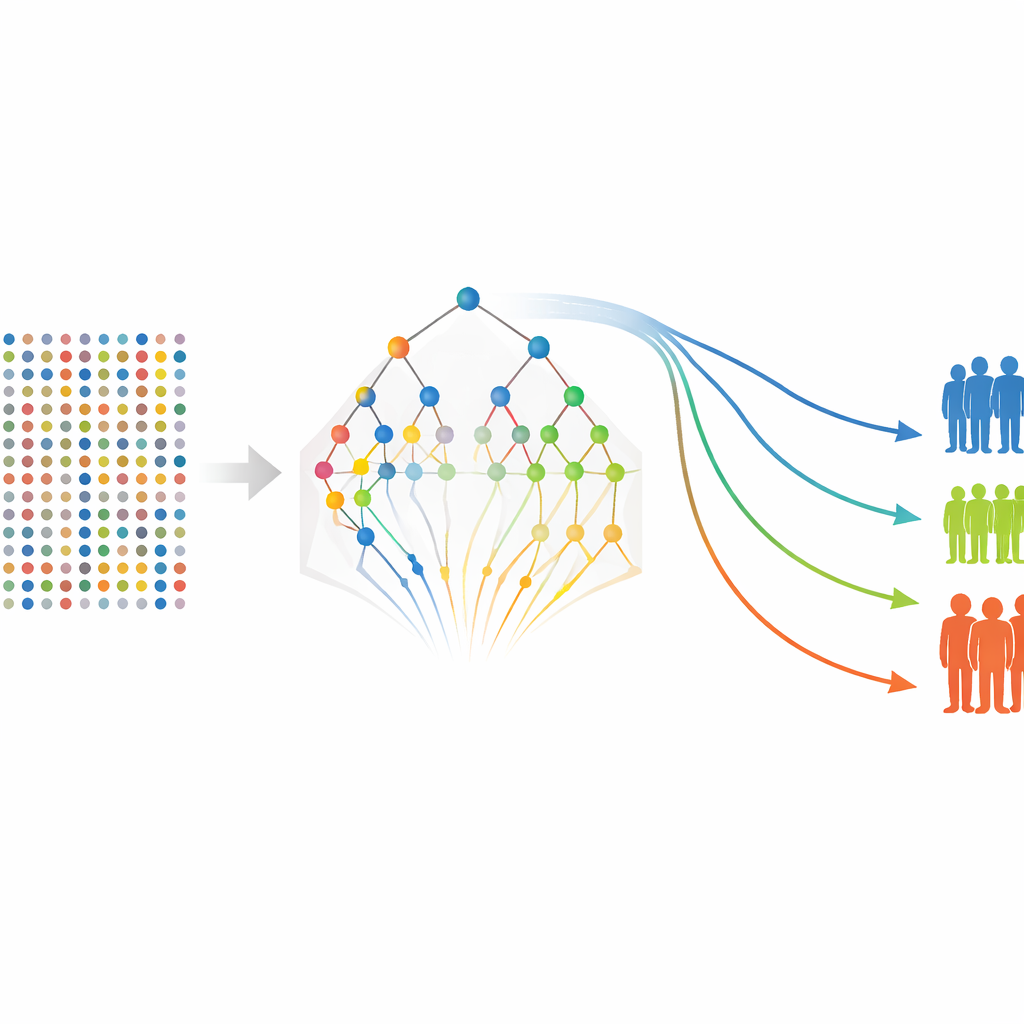
Z dopracowaną listą białek w ręku autorzy wracają do bardziej tradycyjnych modeli przeżycia, aby oszacować, jak każdy marker — oraz niektóre cechy kliniczne, takie jak stopień zaawansowania guza — wiążą się z prawdopodobieństwem pozostania wolnym od nawrotu lub odległych przerzutów. Budują modele osobno dla przeżycia bez nawrotu i bez przerzutów, a następnie obliczają dla każdego pacjenta wynik ryzyka na podstawie poziomów białek i cech klinicznych. Pacjenci są grupowani w kategorie niskiego, średniego i wysokiego ryzyka, a standardowe krzywe przeżycia pokazują wyraźne rozdzielenie tych grup, mimo że badanie obejmuje tylko 80 pacjentów. Kilka białek, w tym FGF-5, Neuropilina-2 i miary związane z Siglec-5, wielokrotnie ujawnia się jako silne wskaźniki gorszych wyników, podczas gdy niektóre markery wydają się działać ochronnie.
Testowanie pipeline’u w trudnych warunkach
Aby sprawdzić, czy ich podejście nie jest jedynie przeuczeniem na tym małym zbiorze danych, badacze przeprowadzają obszerne symulacje komputerowe, które naśladują wysokowymiarowe badania białkowe z silnymi naruszeniami powszechnych założeń modelowych i różnymi wzorcami braków danych. W tych testach obciążeniowych ten sam pipeline nadal identyfikuje zwarte zestawy rzeczywiście istotnych markerów i rozdziela grupy niskiego i wysokiego ryzyka, nawet gdy zwykłe założenia stojące za klasycznymi modelami przeżycia nie są spełnione. Również modyfikują progi brakujących danych i pokazują, że kluczowe markery oraz ogólne wnioski pozostają w dużej mierze stabilne.
Co to oznacza na przyszłość
Zamiast wynajdywać zupełnie nowy trik statystyczny, praca ta łączy i weryfikuje praktyczny przepis na przekształcenie złożonych pomiarów białkowych w klinicznie istotne prognozy ryzyka. Poprzez ostrożne traktowanie brakujących wartości, zawężenie uwagi do stabilnego zestawu biomarkerów oraz sprawdzenie wydajności za pomocą solidnej walidacji wewnętrznej i symulacji, pipeline oferuje przejrzysty sposób identyfikacji obiecujących markerów i budowy skali ryzyka w małych, bogatych w dane badaniach onkologicznych. Autorzy podkreślają, że wciąż potrzebne są większe, niezależne kohorty, aby potwierdzić konkretne białka jako rutynowe testy kliniczne, ale ich ramy dostarczają solidnego, wielokrotnego do użycia planu dla przyszłych badań nad biomarkerami i przeżyciem.
Cytowanie: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Słowa kluczowe: biomarkery nowotworowe, prognozowanie przeżycia, proteomika, brakujące dane, medycyna precyzyjna