Clear Sky Science · ja
高次元タンパク質バイオマーカーデータにおける補完と特徴選択による生存リスク予測の強化
患者にとってなぜ重要か
医師は、血液検査を用いて患者のがんがどのように進行するか(再発や転移の有無)を予測し、それに基づいて治療を個別化したいとますます考えるようになっています。現代のタンパク質検査は一度に何百もの分子を測定できますが、得られるデータは散発的で欠測が多く、患者数に比して測定項目がはるかに多いという問題があります。本論文は、このような複雑なデータを注意深く整備・解析することで、生存予測をより信頼でき、臨床医が解釈しやすくする手法を示しています。
乱雑な検査結果を有用な信号に変える
著者らは血中タンパク質バイオマーカーに着目しています。これらは腫瘍の増殖の様子、免疫応答、治療への反応を示唆する分子です。実臨床に近い研究ではこれらのマーカーが複数時点で測定されますが、技術的な問題や脱落のために測定値が抜けることがよくあります。不完全な記録を単純に捨てたり粗い平均で埋めたりすると、特に少数の患者で何百ものタンパク質を追う場合に結果が大きく歪む可能性があります。そこで本研究は、誤解を招く近道を避けつつ可能な限り情報を保持するための段階的な解析パイプラインを構築しています。
アウトカムをのぞき見せずに欠損を埋める
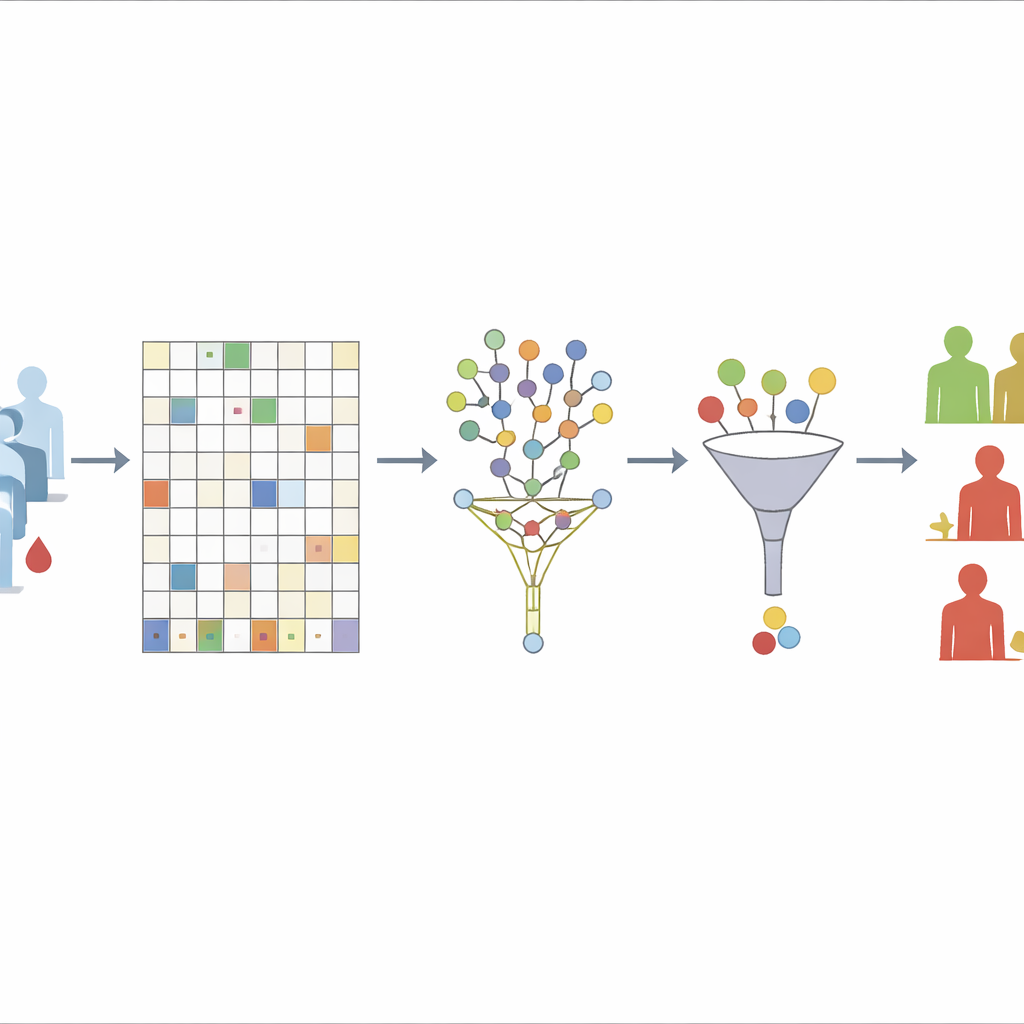
まずチームが取り組む課題は欠測データです。彼らは最初に、患者の30%以上で欠測しているタンパク質のみを除外します。これは安定性と情報損失のバランスが良い水準であると示されています。残ったタンパク質については「教師なし」のランダムフォレストを用いて欠測値を推定します。本質的には、このアルゴリズムはタンパク質同士の関係だけに基づいて何本もの決定木を繰り返し構築し、再発や転移といった生存アウトカムは利用しません。多くの木で似た振る舞いを示すサンプルは近隣とみなされ、その近隣の既知の値を使って欠損が埋められます。この段階で生存アウトカムを意図的に除外することで、データ前処理の段階で答えを知らず知らず埋め込んでしまうリスクを避けています。
何百もの指標を意味ある少数に絞る
タンパク質テーブルが完成したら、次に再発や転移までの時間を予測するうえで本当に重要なマーカーを決めます。著者らはまず弱い予測因子をゼロに近づけつつ強い因子を残す縮小手法を用い、実質的に最も情報のあるタンパク質だけを通すふるいのように働かせます。この方法は相関のあるマーカー群や微妙な非線形パターンを見落とすことがあるため、残った候補を生存データ向けに多数のランダム化決定木で再評価する二段階目の手法を採ります。この第二段階では同じ回帰モデルを再適合するのではなく、各マーカーが患者のアウトカムを分離するためにどれだけ木の分岐に寄与するかをスコア化します。木の上位近傍に一貫して現れるマーカーは、より安定して重要とみなされます。
選択されたマーカーから患者レベルのリスク群へ
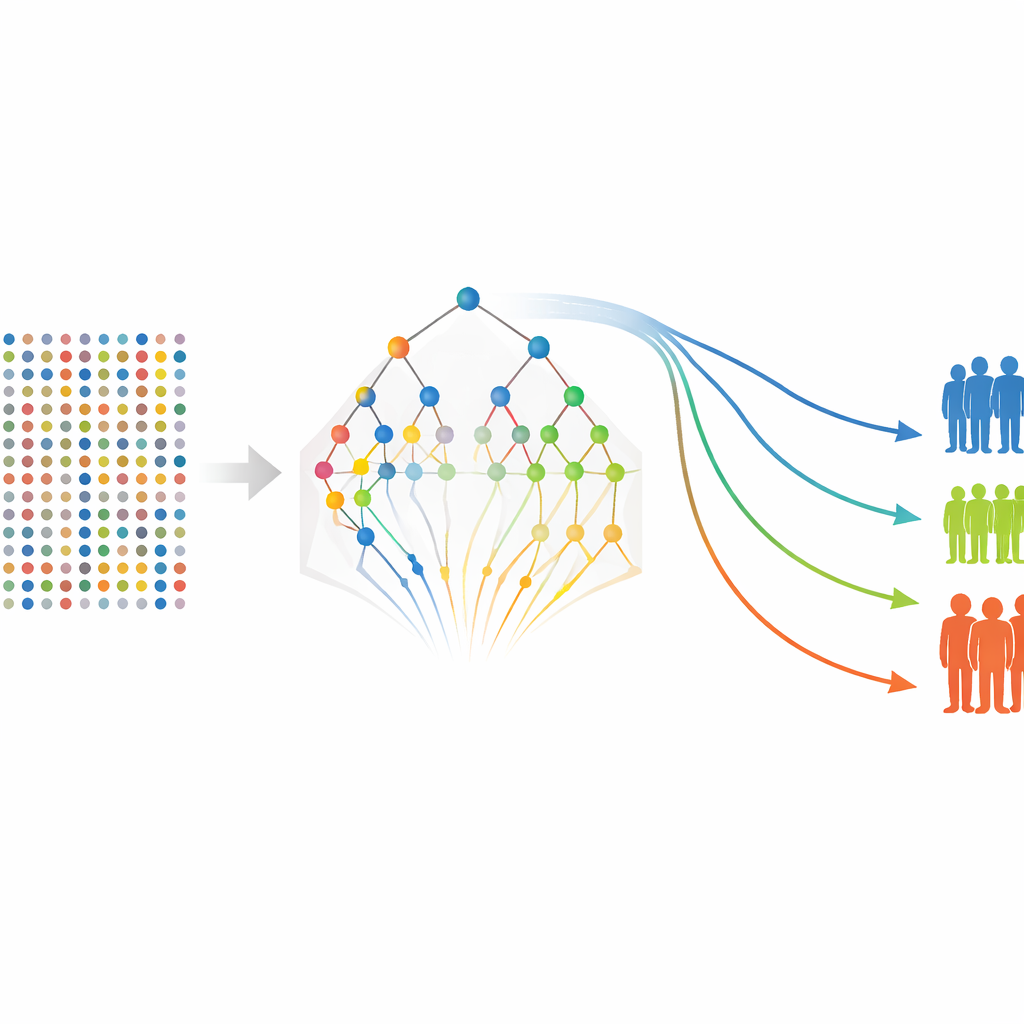
絞り込まれたタンパク質リストをもとに、著者らは従来型の生存モデルに戻り、各マーカーと腫瘍ステージなどの臨床特徴が再発や遠隔転移の発生確率にどう関係するかを推定します。再発無増悪生存と転移無増悪生存で別々にモデルを構築し、各患者についてタンパク質レベルと臨床情報からリスクスコアを算出します。患者は低・中・高のリスク群に分類され、標準的な生存曲線はこれらの群間で明瞭な分離を示します。対象は80名と小規模でしたが、FGF-5、Neuropilin-2、Siglec-5関連の指標などいくつかのタンパク質は一貫して悪化の強い指標として浮かび上がり、一方で保護的に見えるマーカーもありました。
厳しい条件下でのパイプライン検証
この手法が小規模データに過剰適合しているだけでないことを確かめるため、研究者らは一般的なモデリングの仮定が強く破られるケースやさまざまな欠測パターンを模した高次元タンパク質研究の広範なコンピュータシミュレーションを実行しました。これらのストレステストにおいても、同じパイプラインは本当に重要なコンパクトなマーカー群を識別し、古典的生存モデルの背後にある通常の仮定が成り立たない場合でも低リスクと高リスク群を分けることができました。また欠測データの閾値を変えても、主要なマーカーと全体的な結論は概ね安定していることを示しています。
今後の意味合い
新たな統計学的トリックを発明するのではなく、本研究は複雑なタンパク質測定を臨床的に意味あるリスク予測に変えるための実用的な手順を組み立てて検証しました。欠測値を慎重に扱い、安定したバイオマーカー群に焦点を絞り、内部検証とシミュレーションで性能を確認することで、このパイプラインは小規模だがデータ豊富ながん研究における有望なマーカーの同定とリスクスコア構築のための透明な方法を提供します。著者らは特定のタンパク質を日常的な臨床検査として確定するにはより大きな独立コホートでの検証が依然必要であると強調していますが、本フレームワークは将来のバイオマーカー駆動型生存研究に対する堅牢で再利用可能な青写真を示しています。
引用: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
キーワード: がんバイオマーカー, 生存予測, プロテオミクス, 欠測データ, 精密医療