Clear Sky Science · pt
Melhorando a previsão de risco de sobrevida por meio de imputação e seleção de características em dados proteicos de alta dimensão
Por que isso importa para os pacientes
Médicos cada vez mais querem usar exames de sangue para prever como o câncer de uma pessoa provavelmente vai se comportar — se voltará ou se espalhará — e assim ajustar o tratamento. Testes proteicos modernos podem medir centenas de moléculas ao mesmo tempo, mas os dados resultantes são bagunçados, cheios de valores faltantes e contêm muito mais medições do que pacientes. Este artigo mostra como limpar e analisar cuidadosamente esses dados complexos para que as previsões de sobrevida sejam mais confiáveis e mais fáceis de interpretar pelos clínicos.
Transformando resultados laboratoriais confusos em sinais úteis
Os autores se concentram em biomarcadores proteicos, moléculas no sangue cujos níveis podem indicar como um tumor está crescendo, como o sistema imunológico está respondendo e como um paciente está reagindo à terapia. Em estudos do mundo real, esses marcadores são medidos repetidamente ao longo do tempo, mas algumas leituras costumam estar faltando por questões técnicas ou desistência de pacientes. Simplesmente descartar registros incompletos ou preencher lacunas com médias grosseiras pode distorcer severamente os resultados, especialmente quando centenas de proteínas são monitoradas em um pequeno grupo de pacientes. O estudo constrói, portanto, um fluxo de análise passo a passo projetado para manter o máximo de informação possível evitando atalhos enganosos.
Preenchendo as lacunas sem espiar os desfechos
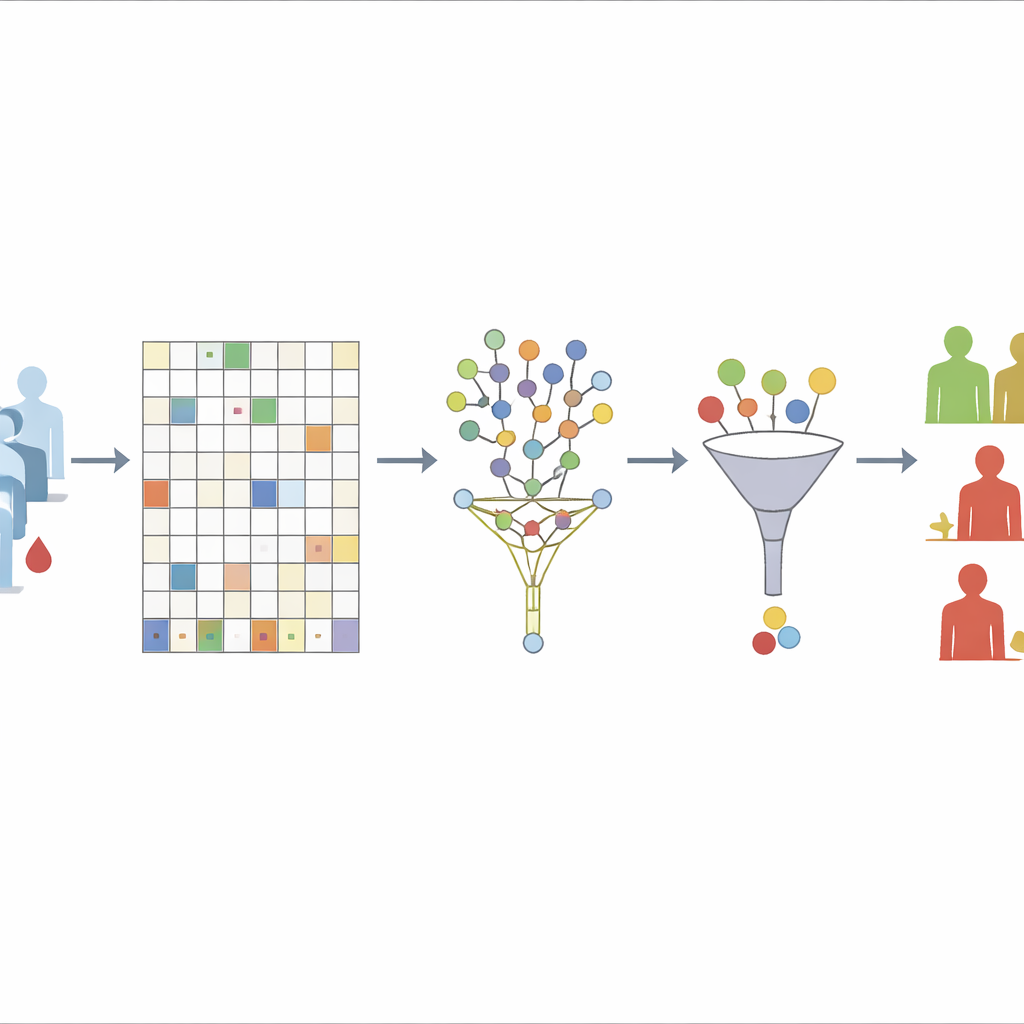
O primeiro desafio que a equipe enfrenta é o dos dados faltantes. Eles começam descartando apenas aquelas proteínas que faltam em mais de 30% dos pacientes, um nível que mostram ser um bom equilíbrio entre estabilidade e perda de informação. Para as proteínas restantes, usam uma abordagem de floresta aleatória “não supervisionada” para estimar os valores ausentes. Essencialmente, o algoritmo constrói repetidamente muitas árvores de decisão com base apenas em como as proteínas se relacionam entre si, não em quem teve recidiva ou desenvolveu metástase. Amostras que tendem a se parecer em muitas árvores são tratadas como vizinhas; os valores conhecidos nessas vizinhas são então usados para preencher as lacunas. Ao excluir deliberadamente os desfechos de sobrevida desta etapa, os autores evitam inserir acidentalmente a resposta no processo de limpeza dos dados.
Reduzindo centenas de marcadores a poucos significativos
Uma vez que a tabela de proteínas está completa, o próximo passo é decidir quais marcadores realmente importam para prever o tempo até recidiva ou metástase. Os autores primeiro usam uma técnica que encolhe preditores fracos em direção a zero enquanto preserva os mais fortes, atuando efetivamente como uma peneira que deixa passar apenas as proteínas mais informativas. Como esse método pode perder grupos de marcadores correlacionados ou padrões não lineares sutis, eles reexaminam os sobreviventes com uma segunda ferramenta baseada em muitas árvores de decisão randomizadas construídas para dados de sobrevida. Esta segunda etapa não re-ajusta a mesma regressão, mas pontua com que frequência cada marcador ajuda as árvores a separar pacientes com desfechos diferentes. Marcadores que aparecem consistentemente perto do topo das árvores são considerados mais estáveis e importantes.
Dos marcadores selecionados para grupos de risco a nível do paciente
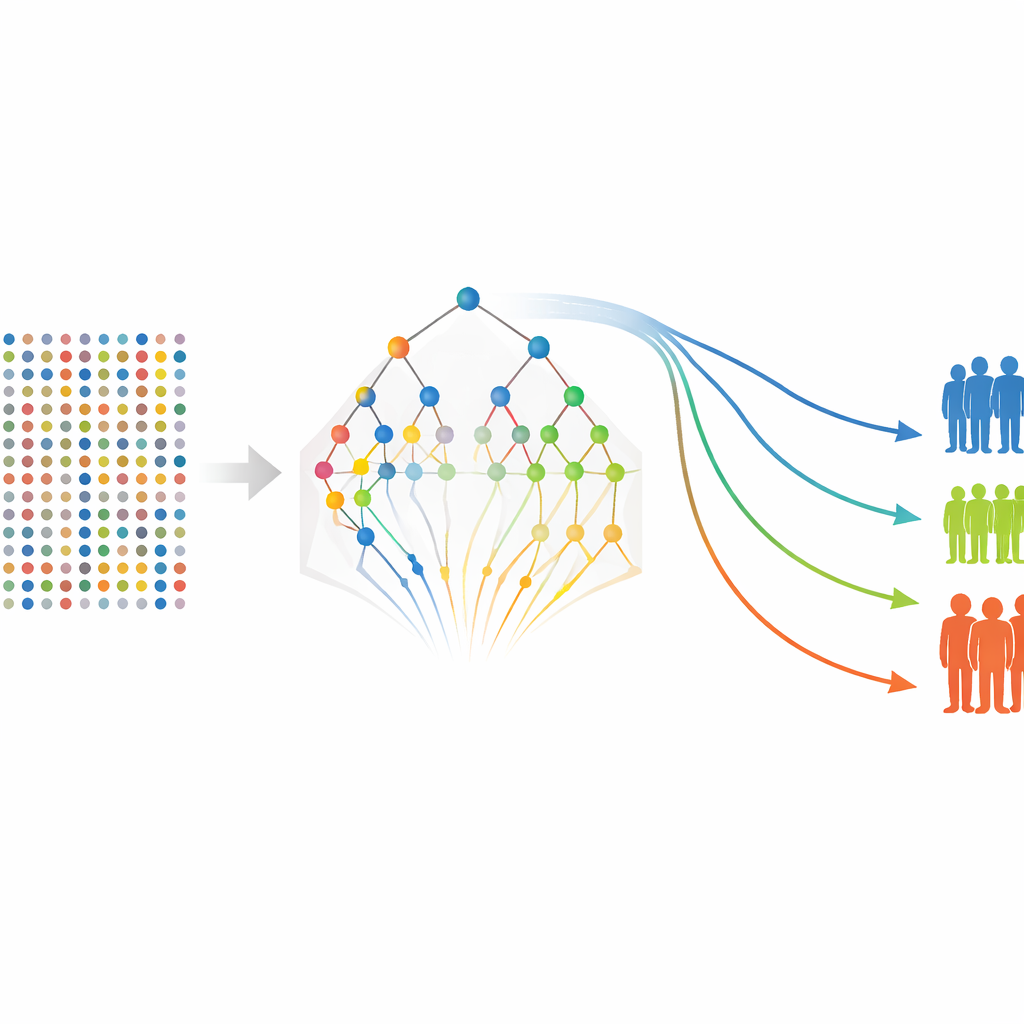
Com uma lista refinada de proteínas em mãos, os autores voltam a modelos de sobrevida mais tradicionais para estimar como cada marcador — e algumas características clínicas, como o estádio do tumor — se relaciona com as chances de permanecer livre de recidiva ou de disseminação à distância. Eles constroem modelos separadamente para sobrevida livre de recidiva e sobrevida livre de metástase, e então calculam uma pontuação de risco para cada paciente com base em seus níveis de proteína e características clínicas. Os pacientes são agrupados em categorias de baixo, médio e alto risco, e curvas de sobrevida padrão mostram separação clara entre esses grupos, apesar de o estudo incluir apenas 80 pacientes. Diversas proteínas, incluindo FGF-5, Neuropilin-2 e medidas relacionadas a Siglec-5, surgem repetidamente como fortes indicadores de piores desfechos, enquanto alguns marcadores parecem ter efeito protetor.
Testando o fluxo sob condições rigorosas
Para verificar que sua abordagem não está apenas ajustando demais esse conjunto pequeno de dados, os pesquisadores executam extensas simulações por computador que imitam estudos proteicos de alta dimensão com fortes violações das suposições comuns de modelagem e diferentes padrões de dados faltantes. Nesses testes de estresse, o mesmo fluxo ainda identifica um conjunto compacto de marcadores realmente importantes e separa grupos de baixo e alto risco, mesmo quando as suposições usuais por trás dos modelos clássicos de sobrevida não se mantêm. Eles também variam os limiares para dados faltantes e mostram que os marcadores-chave e as conclusões gerais permanecem amplamente estáveis.
O que isso significa para o futuro
Em vez de inventar um truque estatístico totalmente novo, este trabalho reúne e valida uma receita prática para transformar medições proteicas complexas em previsões de risco clinicamente relevantes. Ao lidar cuidadosamente com valores faltantes, concentrar-se em um conjunto estável de biomarcadores e checar o desempenho com validação interna robusta e simulações, o fluxo oferece uma maneira transparente de identificar marcadores promissores e construir pontuações de risco em estudos de câncer pequenos e ricos em dados. Os autores enfatizam que coortes maiores e independentes ainda são necessárias para confirmar proteínas específicas como testes clínicos de rotina, mas seu quadro fornece um plano sólido e reutilizável para pesquisas futuras de sobrevida orientadas por biomarcadores.
Citação: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Palavras-chave: biomarcadores de câncer, predição de sobrevida, proteômica, dados faltantes, medicina de precisão