Clear Sky Science · es
Mejorar la predicción de riesgo de supervivencia mediante imputación y selección de variables en datos proteómicos de alta dimensión
Por qué esto importa para los pacientes
Los médicos quieren cada vez más usar análisis de sangre para prever cómo se comportará el cáncer de una persona —si reaparecerá o se propagará— y así adecuar el tratamiento. Las pruebas proteicas modernas pueden medir cientos de moléculas a la vez, pero los datos resultantes son desordenados, presentan muchos valores faltantes y contienen muchas más mediciones que pacientes. Este artículo muestra cómo limpiar y analizar con cuidado esos datos complejos para que las predicciones de supervivencia sean más fiables y más fáciles de interpretar por los clínicos.
Convertir resultados de laboratorio desordenados en señales útiles
Los autores se centran en los biomarcadores proteicos, moléculas en la sangre cuyos niveles pueden indicar cómo crece un tumor, cómo responde el sistema inmunitario y cómo reacciona el paciente al tratamiento. En estudios del mundo real, estos marcadores se miden de forma repetida a lo largo del tiempo, pero a menudo faltan algunas lecturas por problemas técnicos o por abandono de los participantes. Simplemente descartar registros incompletos o rellenar huecos con promedios toscos puede distorsionar gravemente los resultados, especialmente cuando se siguen cientos de proteínas en un grupo pequeño de pacientes. Por ello, el estudio construye una canalización de análisis paso a paso diseñada para conservar la mayor cantidad de información posible evitando atajos engañosos.
Rellenar los huecos sin mirar los desenlaces
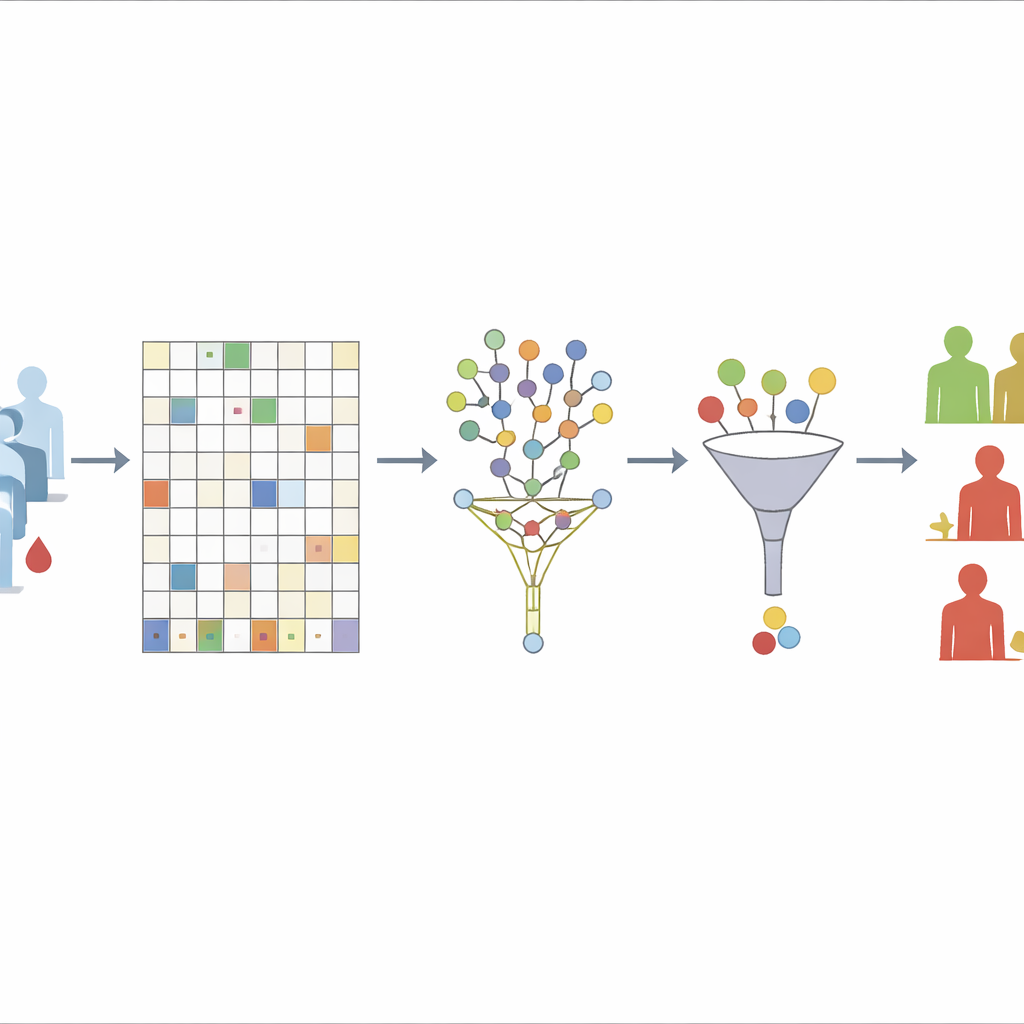
El primer reto que afronta el equipo es el de los datos faltantes. Comienzan descartando solo las proteínas que faltan en más del 30% de los pacientes, un umbral que muestran como buen equilibrio entre estabilidad y pérdida de información. Para las proteínas restantes usan un enfoque de bosque aleatorio “no supervisado” para estimar los valores ausentes. En esencia, el algoritmo construye repetidamente muchos árboles de decisión basándose únicamente en cómo se relacionan las proteínas entre sí, no en quién tuvo recaída o desarrolló metástasis. Las muestras que tienden a parecerse a lo largo de muchos árboles se tratan como vecinas; los valores conocidos en esas vecinas se usan luego para rellenar los huecos. Al excluir deliberadamente los desenlaces de supervivencia en este paso, los autores evitan introducir accidentalmente la respuesta en el proceso de limpieza de datos.
Reducir cientos de marcadores a unos pocos significativos
Una vez completa la tabla de proteínas, el siguiente paso es decidir qué marcadores importan realmente para predecir el tiempo hasta recaída o metástasis. Los autores usan primero una técnica que reduce los predictores débiles hacia cero mientras conserva los más fuertes, actuando efectivamente como un tamiz que deja pasar solo las proteínas más informativas. Dado que este método puede pasar por alto grupos de marcadores correlacionados o patrones no lineales sutiles, vuelven a examinar los supervivientes con una segunda herramienta basada en muchos árboles de decisión aleatorizados diseñados para datos de supervivencia. Esta segunda etapa no ajusta de nuevo la misma regresión sino que puntúa con qué frecuencia cada marcador ayuda a los árboles a separar a los pacientes con distintos desenlaces. Los marcadores que aparecen consistentemente cerca de la cima de los árboles se consideran más estables e importantes.
De los marcadores seleccionados a grupos de riesgo a nivel de paciente
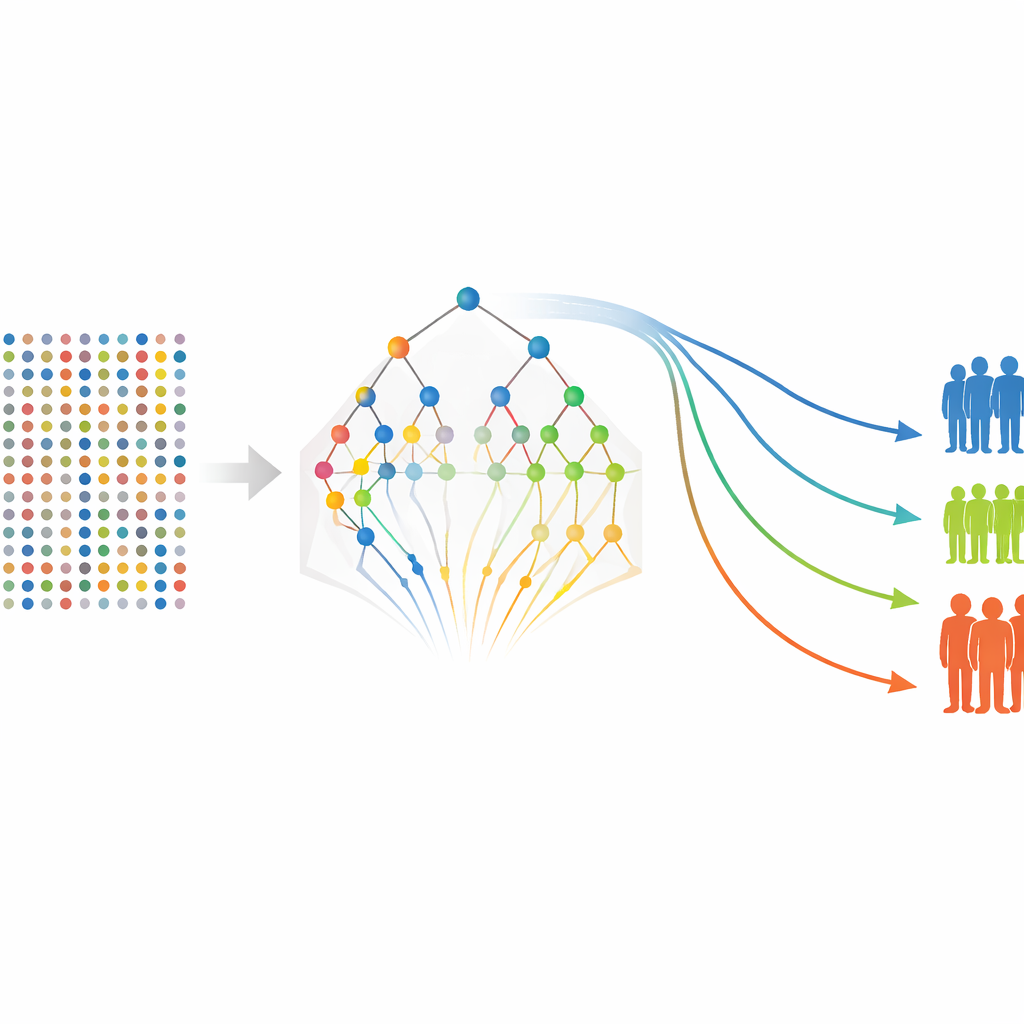
Con una lista refinada de proteínas, los autores vuelven a modelos de supervivencia más tradicionales para estimar cómo se relaciona cada marcador —y algunas características clínicas como el estadio tumoral— con las probabilidades de permanecer libres de recaída o de diseminación a distancia. Construyen modelos por separado para la supervivencia libre de recaída y la supervivencia libre de metástasis, y luego calculan una puntuación de riesgo para cada paciente basada en sus niveles proteicos y sus características clínicas. Los pacientes se agrupan en categorías de riesgo bajo, medio y alto, y las curvas de supervivencia estándar muestran una separación clara entre estos grupos, a pesar de que el estudio incluye solo 80 pacientes. Varias proteínas, incluidas FGF‑5, Neuropilina‑2 y medidas relacionadas con Siglec‑5, aparecen repetidamente como indicadores fuertes de peores resultados, mientras que algunos marcadores parecen ser protectores.
Probar la canalización en condiciones exigentes
Para comprobar que su enfoque no está simplemente sobreajustando este conjunto de datos pequeño, los investigadores ejecutan extensas simulaciones informáticas que imitan estudios proteómicos de alta dimensión con fuertes violaciones de supuestos de modelado comunes y distintos patrones de datos faltantes. En estas pruebas de resistencia, la misma canalización sigue identificando un conjunto compacto de marcadores realmente importantes y separa grupos de bajo y alto riesgo, incluso cuando las suposiciones habituales detrás de los modelos clásicos de supervivencia no se cumplen. También varían los umbrales de datos faltantes y muestran que los marcadores clave y las conclusiones generales se mantienen en gran medida estables.
Qué significa esto de cara al futuro
En lugar de inventar un truco estadístico completamente nuevo, este trabajo reúne y valida una receta práctica para convertir mediciones proteicas complejas en predicciones de riesgo clínicamente significativas. Al manejar con cuidado los valores faltantes, centrar el análisis en un conjunto estable de biomarcadores y comprobar el rendimiento con validación interna robusta y simulaciones, la canalización ofrece una vía transparente para identificar marcadores prometedores y construir puntuaciones de riesgo en estudios oncológicos pequeños pero ricos en datos. Los autores subrayan que todavía se necesitan cohortes independientes más grandes para confirmar proteínas específicas como pruebas de rutina en la clínica, pero su marco proporciona un plan sólido y reutilizable para futuras investigaciones de supervivencia guiadas por biomarcadores.
Cita: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Palabras clave: biomarcadores de cáncer, predicción de supervivencia, proteómica, datos faltantes, medicina de precisión