Clear Sky Science · fr
Améliorer la prédiction du risque de survie par imputation et sélection de caractéristiques dans des données protéiques haute-dimension
Pourquoi c’est important pour les patients
Les médecins souhaitent de plus en plus utiliser des analyses sanguines pour prévoir le comportement probable d’un cancer — s’il récidivera ou se propagera — et adapter les traitements en conséquence. Les tests protéiques modernes peuvent mesurer des centaines de molécules à la fois, mais les données obtenues sont désordonnées, pleines de valeurs manquantes et comportent bien plus de mesures que de patients. Cet article montre comment nettoyer et analyser soigneusement de telles données complexes afin que les prédictions de survie soient plus fiables et plus faciles à interpréter par les cliniciens.
Transformer des résultats de laboratoire brouillons en signaux utiles
Les auteurs se concentrent sur les biomarqueurs protéiques, des molécules dans le sang dont les taux peuvent donner des indications sur la croissance d’une tumeur, la réponse du système immunitaire et la réaction d’un patient au traitement. Dans les études en conditions réelles, ces marqueurs sont mesurés de façon répétée au fil du temps, mais certaines lectures sont souvent manquantes en raison de problèmes techniques ou d’abandons de patients. Se contenter d’écarter les dossiers incomplets ou de combler les vides avec des moyennes grossières peut fausser gravement les résultats, surtout lorsque des centaines de protéines sont suivies dans un petit groupe de patients. L’étude construit donc une chaîne d’analyse étape par étape conçue pour conserver autant d’information que possible tout en évitant des raccourcis trompeurs.
Combler les lacunes sans « regarder » les issues
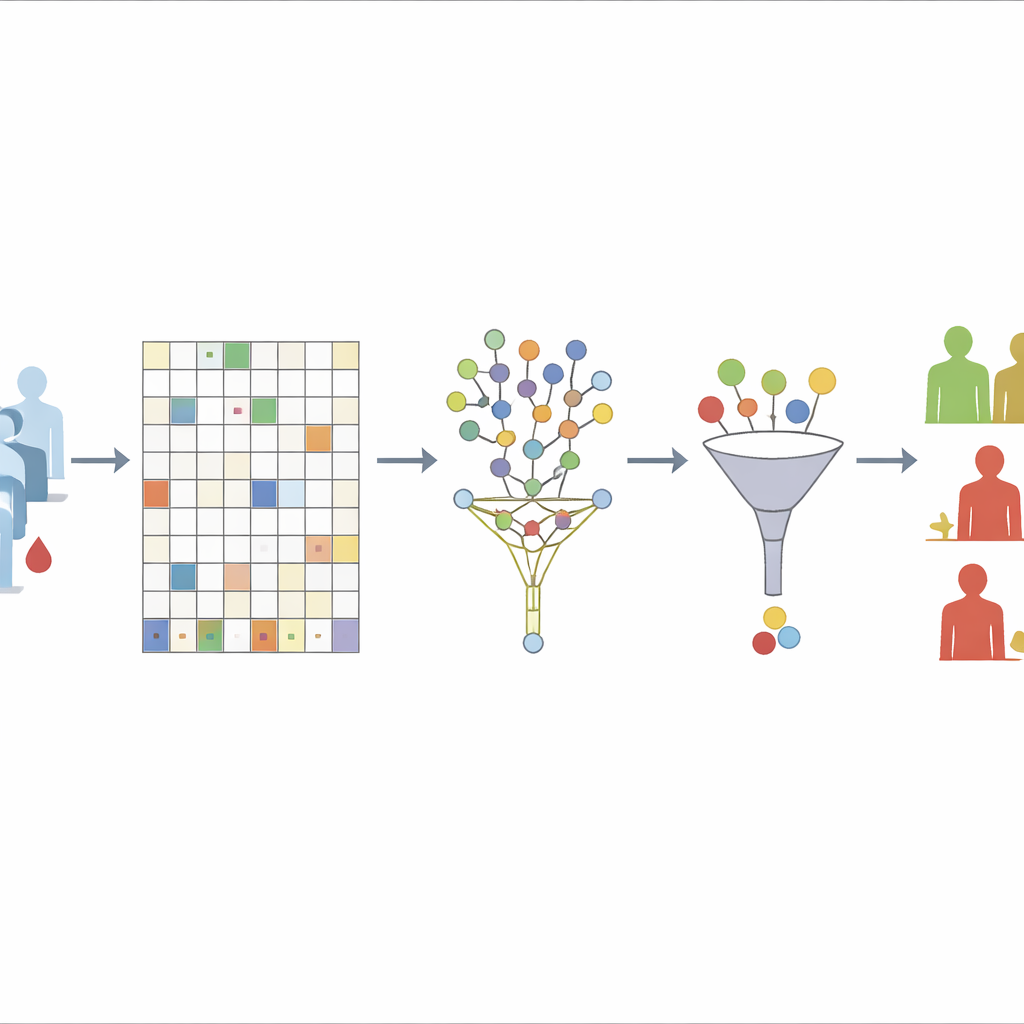
Le premier défi que l’équipe aborde est celui des données manquantes. Ils commencent par éliminer uniquement les protéines absentes chez plus de 30 % des patients, un seuil qu’ils montrent être un bon compromis entre stabilité et perte d’information. Pour les protéines restantes, ils utilisent une approche de forêt aléatoire « non supervisée » pour estimer les valeurs manquantes. Essentiellement, l’algorithme construit de nombreuses fois des arbres de décision en se basant uniquement sur les relations entre protéines, sans utiliser les informations de rechute ou de métastase. Les échantillons qui ont tendance à se ressembler à travers de nombreux arbres sont traités comme voisins ; les valeurs connues chez ces voisins servent ensuite à combler les vides. En excluant délibérément les issues de survie de cette étape, les auteurs évitent d’introduire accidentellement la réponse dans le processus de nettoyage des données.
Réduire des centaines de marqueurs à quelques-uns de pertinents
Une fois le tableau des protéines complété, l’étape suivante consiste à décider quels marqueurs importent réellement pour prédire le temps jusqu’à la rechute ou la métastase. Les auteurs utilisent d’abord une technique qui contraint les faibles prédicteurs vers zéro tout en conservant les prédicteurs plus forts, agissant en somme comme un tamis qui ne laisse passer que les protéines les plus informatives. Parce que cette méthode peut manquer des groupes de marqueurs corrélés ou des motifs non linéaires subtils, ils réexaminent ensuite les survivants avec un second outil basé sur de nombreux arbres de décision aléatoires construits pour des données de survie. Cette seconde étape ne refait pas la même régression mais évalue plutôt la fréquence à laquelle chaque marqueur aide les arbres à séparer des patients aux issues différentes. Les marqueurs qui apparaissent de façon récurrente en haut des arbres sont considérés comme plus stables et importants.
Des marqueurs sélectionnés aux groupes de risque au niveau du patient
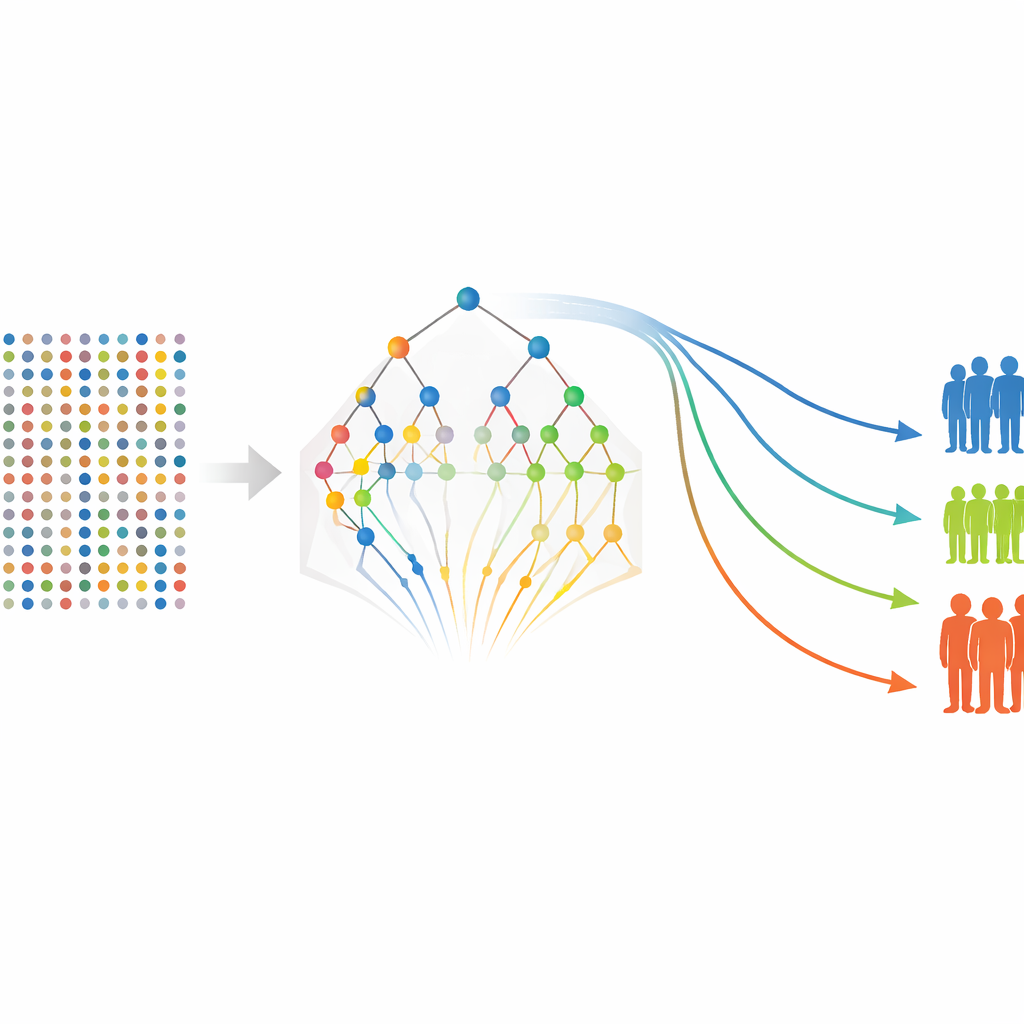
Avec une liste affinée de protéines en main, les auteurs reviennent à des modèles de survie plus traditionnels pour estimer comment chaque marqueur — et certaines caractéristiques cliniques comme le stade tumoral — se rapporte aux chances de rester indemne de rechute ou de propagation à distance. Ils construisent des modèles séparés pour la survie sans rechute et la survie sans métastase, puis calculent un score de risque pour chaque patient basé sur leurs niveaux protéiques et leurs caractéristiques cliniques. Les patients sont regroupés en catégories à risque faible, moyen et élevé, et les courbes de survie standard montrent une séparation nette entre ces groupes, même si l’étude ne comprend que 80 patients. Plusieurs protéines, dont FGF-5, Neuropilin-2 et des mesures liées à Siglec-5, émergent à plusieurs reprises comme des indicateurs forts d’un mauvais pronostic, tandis que certains marqueurs semblent protecteurs.
Tester la chaîne sous des conditions difficiles
Pour vérifier que leur approche ne se contente pas de sur-ajuster ce petit jeu de données, les chercheurs réalisent de vastes simulations informatiques qui imitent des études protéiques haute-dimension avec de fortes violations des hypothèses habituelles de modélisation et différents schémas de données manquantes. Dans ces tests de stress, la même chaîne identifie néanmoins un ensemble compact de marqueurs réellement importants et sépare les groupes à risque faible et élevé, même lorsque les hypothèses classiques des modèles de survie ne sont pas respectées. Ils varient également les seuils de données manquantes et montrent que les marqueurs clés et les conclusions générales restent en grande partie stables.
Ce que cela implique pour l’avenir
Plutôt que d’inventer une astuce statistique entièrement nouvelle, ce travail assemble et valide une recette pratique pour transformer des mesures protéiques complexes en prédictions de risque cliniquement significatives. En traitant soigneusement les valeurs manquantes, en réduisant le champ à un ensemble stable de biomarqueurs et en vérifiant les performances par une validation interne robuste et des simulations, la chaîne offre une méthode transparente pour identifier des marqueurs prometteurs et construire des scores de risque dans des études oncologiques petites mais riches en données. Les auteurs soulignent que des cohortes indépendantes plus larges sont encore nécessaires pour confirmer l’utilisation routinière de protéines spécifiques en clinique, mais leur cadre fournit un plan solide et réutilisable pour de futures recherches de survie axées sur les biomarqueurs.
Citation: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Mots-clés: biomarqueurs du cancer, prédiction de survie, protéomique, données manquantes, médecine de précision