Clear Sky Science · de
Verbesserung der Vorhersage des Überlebensrisikos durch Imputation und Merkmalsauswahl in hochdimensionalen Protein-Biomarker-Daten
Warum das für Patientinnen und Patienten wichtig ist
Ärztinnen und Ärzte möchten zunehmend Bluttests nutzen, um vorherzusagen, wie sich eine Krebserkrankung wahrscheinlich entwickelt – ob sie zurückkehrt oder sich ausbreitet – und die Therapie dementsprechend anzupassen. Moderne Protein-Tests können Hunderte von Molekülen gleichzeitig messen, doch die resultierenden Daten sind unordentlich, enthalten viele fehlende Werte und umfassen deutlich mehr Messgrößen als Patientinnen und Patienten. Diese Arbeit zeigt, wie man solche komplexen Daten sorgfältig bereinigt und analysiert, damit Überlebensvorhersagen zuverlässiger werden und für Klinikteams leichter interpretierbar sind.
Wie aus unordentlichen Laborergebnissen nützliche Signale werden
Die Autorinnen und Autoren konzentrieren sich auf Protein-Biomarker, Moleküle im Blut, deren Konzentrationen Hinweise darauf geben können, wie ein Tumor wächst, wie das Immunsystem reagiert und wie eine Patientin oder ein Patient auf eine Behandlung reagiert. In realen Studien werden diese Marker wiederholt über die Zeit gemessen, doch einige Messwerte fehlen oft aufgrund technischer Probleme oder weil Teilnehmende aus der Studie ausscheiden. Unvollständige Datensätze einfach zu verwerfen oder Lücken mit groben Durchschnittswerten zu füllen, kann die Ergebnisse stark verzerren – besonders wenn Hunderte von Proteinen in einer kleinen Patientengruppe verfolgt werden. Daher entwickelt die Studie eine schrittweise Analyse-Pipeline, die darauf abzielt, möglichst viel Information zu erhalten, ohne in die Irre führende Abkürzungen zu greifen.
Lücken füllen, ohne einen Blick auf die Endpunkte zu werfen
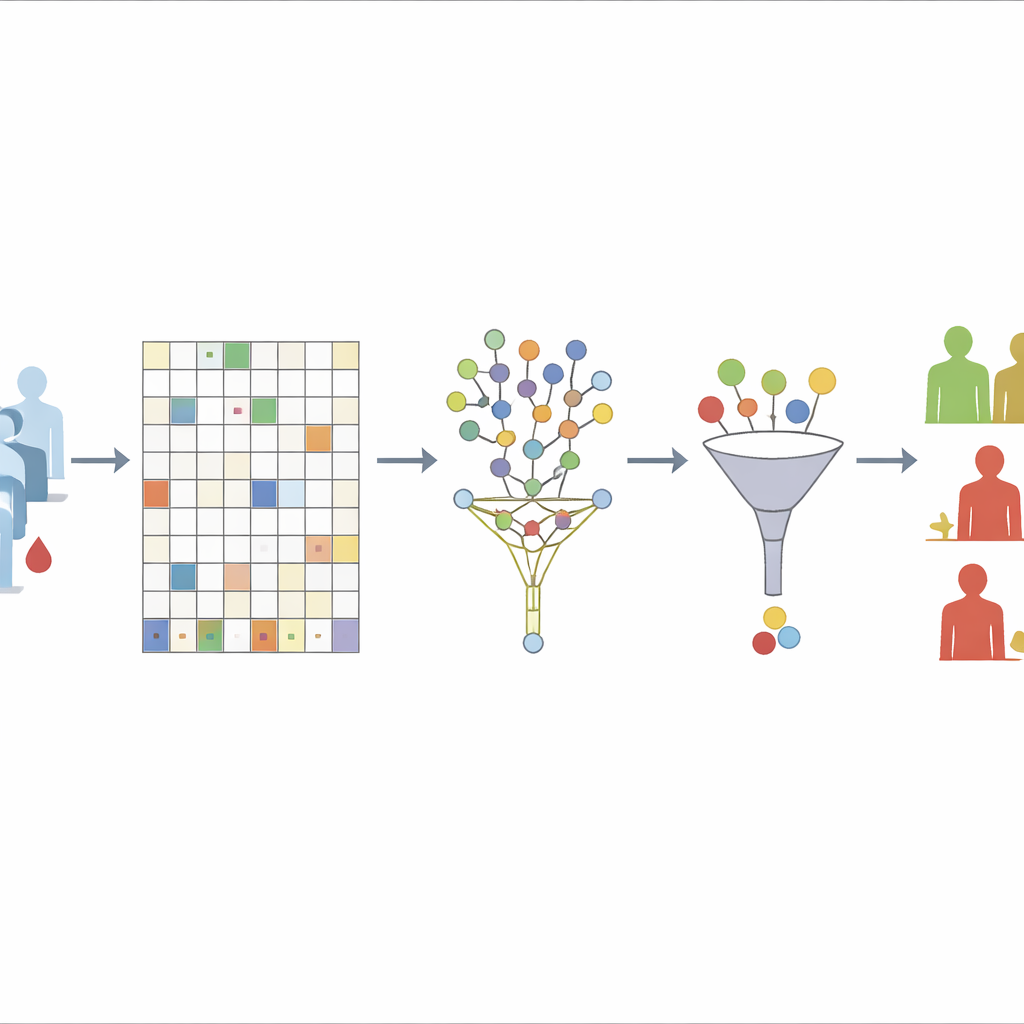
Die erste Herausforderung, die das Team angeht, sind fehlende Daten. Zunächst verwerfen sie nur jene Proteine, die bei mehr als 30 % der Patientinnen und Patienten fehlen – ein Schwellenwert, den sie als guten Kompromiss zwischen Stabilität und Informationsverlust belegen. Für die verbleibenden Proteine verwenden sie einen "unüberwachten" Random-Forest-Ansatz zur Schätzung der fehlenden Werte. Im Kern baut der Algorithmus wiederholt viele Entscheidungsbäume nur auf Basis der Beziehungen zwischen Proteinen, nicht auf Basis von Informationen darüber, wer ein Rezidiv oder Metastasen entwickelt hat. Proben, die über viele Bäume hinweg ähnlich erscheinen, werden als Nachbarn behandelt; die bekannten Werte dieser Nachbarn werden dann zur Lückenfüllung genutzt. Indem die Überlebensoutcomes in diesem Schritt absichtlich ausgeschlossen werden, vermeiden die Autorinnen und Autoren, die Antwort versehentlich in den Datenbereinigungsprozess einzubringen.
Aus Hunderten von Markern eine sinnvolle Auswahl treffen
Sobald die Proteintabelle vollständig ist, besteht der nächste Schritt darin zu entscheiden, welche Marker tatsächlich relevant sind, um die Zeit bis zum Rezidiv oder zur Metastasenbildung vorherzusagen. Die Autorinnen und Autoren nutzen zunächst eine Technik, die schwache Prädiktoren gegen null schrumpfen lässt, während stärkere erhalten bleiben – sie wirkt wie ein Sieb, das nur die informativsten Proteine durchlässt. Da diese Methode Gruppen korrelierter Marker oder subtile nichtlineare Muster übersehen kann, untersuchen sie die verbliebenen Kandidaten anschließend mit einem zweiten Werkzeug, das auf vielen randomisierten Entscheidungsbäumen für Überlebensdaten basiert. Diese zweite Stufe passt die gleiche Regression nicht erneut an, sondern bewertet, wie oft jeder Marker beim Aufteilen von Patientengruppen mit unterschiedlichen Ergebnissen hilft. Marker, die beständig nahe den Spitzen der Bäume erscheinen, gelten als stabiler und wichtiger.
Von ausgewählten Markern zu Patientengruppen mit Risikoabschätzung
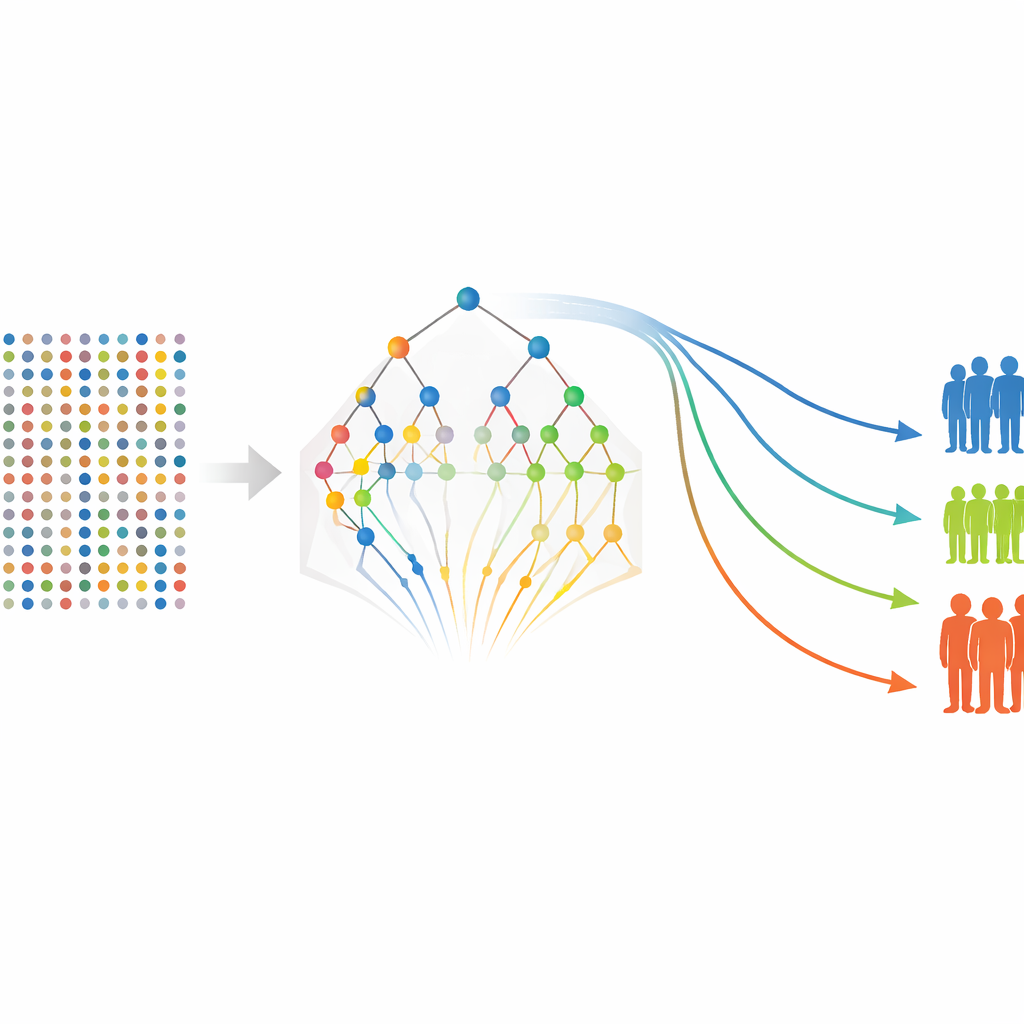
Mit einer verfeinerten Proteinauswahl kehren die Autorinnen und Autoren zu traditionelleren Überlebensmodellen zurück, um abzuschätzen, wie jeder Marker – und einige klinische Merkmale wie der Tumorstadium – mit der Wahrscheinlichkeit zusammenhängt, rezidiv- oder fernmetastasenfrei zu bleiben. Sie erstellen Modelle separat für rezidivfreies und metastasenfreies Überleben und berechnen dann für jede Patientin bzw. jeden Patienten einen Risikoscore auf Basis ihrer/seiner Proteinwerte und klinischen Merkmale. Die Patientinnen und Patienten werden in Niedrig-, Mittel- und Hochrisiko-Gruppen eingeteilt, und Standard-Überlebenskurven zeigen eine klare Trennung zwischen diesen Gruppen, obwohl die Studie nur 80 Teilnehmende umfasst. Mehrere Proteine, darunter FGF-5, Neuropilin-2 und Siglec-5-assoziierte Messgrößen, treten wiederholt als starke Indikatoren für schlechtere Ergebnisse auf, während einige Marker schützend zu wirken scheinen.
Die Pipeline unter harten Bedingungen testen
Um zu prüfen, dass ihr Ansatz nicht nur Überanpassung an diesen kleinen Datensatz ist, führen die Forschenden umfangreiche Computersimulationen durch, die hochdimensionale Proteinstudien mit starken Verletzungen gängiger Modellannahmen und unterschiedlichen Mustern fehlender Daten nachbilden. In diesen Stresstests identifiziert dieselbe Pipeline weiterhin eine kompakte Menge wirklich wichtiger Marker und trennt Niedrig- und Hochrisikogruppen, selbst wenn die üblichen Annahmen klassischer Überlebensmodelle nicht gelten. Sie variieren außerdem die Schwellenwerte für fehlende Daten und zeigen, dass die Schlüssmarker und die allgemeinen Schlussfolgerungen weitgehend stabil bleiben.
Was das für die Zukunft bedeutet
Anstatt einen völlig neuen statistischen Trick zu erfinden, stellt diese Arbeit ein praktisches Rezept zusammen und validiert es, um komplexe Proteinmessungen in klinisch bedeutungsvolle Risikoabschätzungen zu verwandeln. Durch sorgfältigen Umgang mit fehlenden Werten, Fokussierung auf einen stabilen Satz von Biomarkern und Überprüfung der Leistung mittels robuster interner Validierung und Simulationen bietet die Pipeline einen transparenten Weg, vielversprechende Marker zu identifizieren und Risikoscores in kleinen, datenreichen Krebsstudien zu erstellen. Die Autorinnen und Autoren betonen, dass größere, unabhängige Kohorten weiterhin nötig sind, um einzelne Proteine als routinemäßige klinische Tests zu bestätigen, doch ihr Rahmenwerk liefert eine solide, wiederverwendbare Blaupause für künftige biomarkergeleitete Überlebensforschung.
Zitation: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Schlüsselwörter: Krebs-Biomarker, Überlebensvorhersage, Proteomik, fehlende Daten, Präzisionsmedizin