Clear Sky Science · sv
Förbättrad prediktion av överlevnadsrisk genom imputering och variabelurval i högdimensionella proteinbiomarkördata
Varför detta är viktigt för patienter
Läkare vill i allt högre grad använda blodprover för att förutsäga hur en persons cancer sannolikt kommer att bete sig—om den kommer tillbaka eller sprida sig—och anpassa behandlingen därefter. Moderna proteintester kan mäta hundratals molekyler samtidigt, men de resulterande data är röriga, fulla av saknade värden och innehåller ofta betydligt fler mätningar än patienter. Denna artikel visar hur man noggrant kan rengöra och analysera sådana komplexa data så att överlevnadsprediktioner blir mer tillförlitliga och lättare för kliniker att tolka.
Att omvandla röriga labbresultat till användbara signaler
Författarna fokuserar på proteinbiomarkörer, molekyler i blodet vars nivåer kan antyda hur en tumör växer, hur immunförsvaret reagerar och hur en patient svarar på behandling. I studier från verkligheten mäts dessa markörer upprepade gånger över tid, men vissa mätningar saknas ofta på grund av tekniska problem eller att patienter hoppar av. Att utan vidare kasta bort ofullständiga poster eller fylla luckor med grova medelvärden kan snedvrida resultaten kraftigt, särskilt när hundratals proteiner följs i en liten patientgrupp. Studien bygger därför ett steg-för-steg-analysflöde utformat för att bevara så mycket information som möjligt samtidigt som missvisande genvägar undviks.
Fyll i luckorna utan att tjuvkika på utfallen
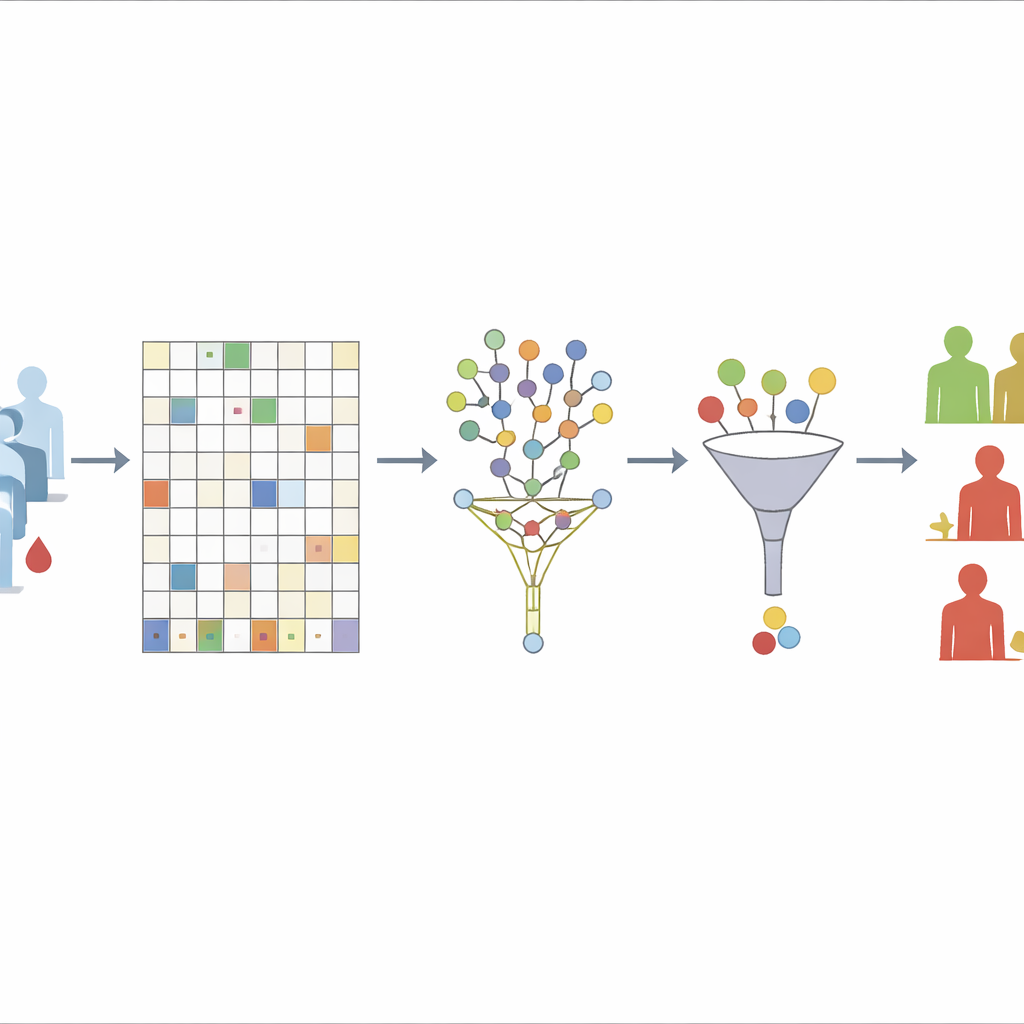
Det första problemet teamet tar itu med är saknade data. De börjar med att bara kassera de proteiner som saknas hos mer än 30 % av patienterna, en nivå de visar är en bra balans mellan stabilitet och informationsförlust. För de övriga proteinerna använder de en "osuperviserad" random forest-metod för att gissa de saknade värdena. I praktiken bygger algoritmen upprepade gånger många beslutsträd enbart baserat på hur proteiner relaterar till varandra, inte på vilka som återfallit eller utvecklat metastaser. Prover som tenderar att likna varandra i många träd behandlas som grannar; de kända värdena hos dessa grannar används sedan för att fylla i luckorna. Genom att medvetet utesluta överlevnadsutfall från detta steg undviker författarna att av misstag införliva svaret i datarengöringsprocessen.
Smalna ner hundratals markörer till ett meningsfullt fåtal
När proteinmatrisen är komplett är nästa steg att avgöra vilka markörer som verkligen är viktiga för att förutsäga tiden till återfall eller metastasering. Författarna använder först en teknik som krymper svaga prediktorer mot noll samtidigt som starkare behålls, vilket fungerar som en sikt som släpper igenom endast de mest informativa proteinerna. Eftersom denna metod kan missa grupper av korrelerade markörer eller subtila icke-linjära mönster, granskar de sedan de kvarvarande med ett andra verktyg baserat på många randomiserade beslutsträd anpassade för överlevnadsdata. Detta andra steg återanpassar inte samma regression utan poängsätter istället hur ofta varje markör hjälper träden att dela patienter med olika utfall. Markörer som konsekvent dyker upp högt upp i träden anses mer stabila och viktiga.
Från utvalda markörer till riskgrupper på patientnivå
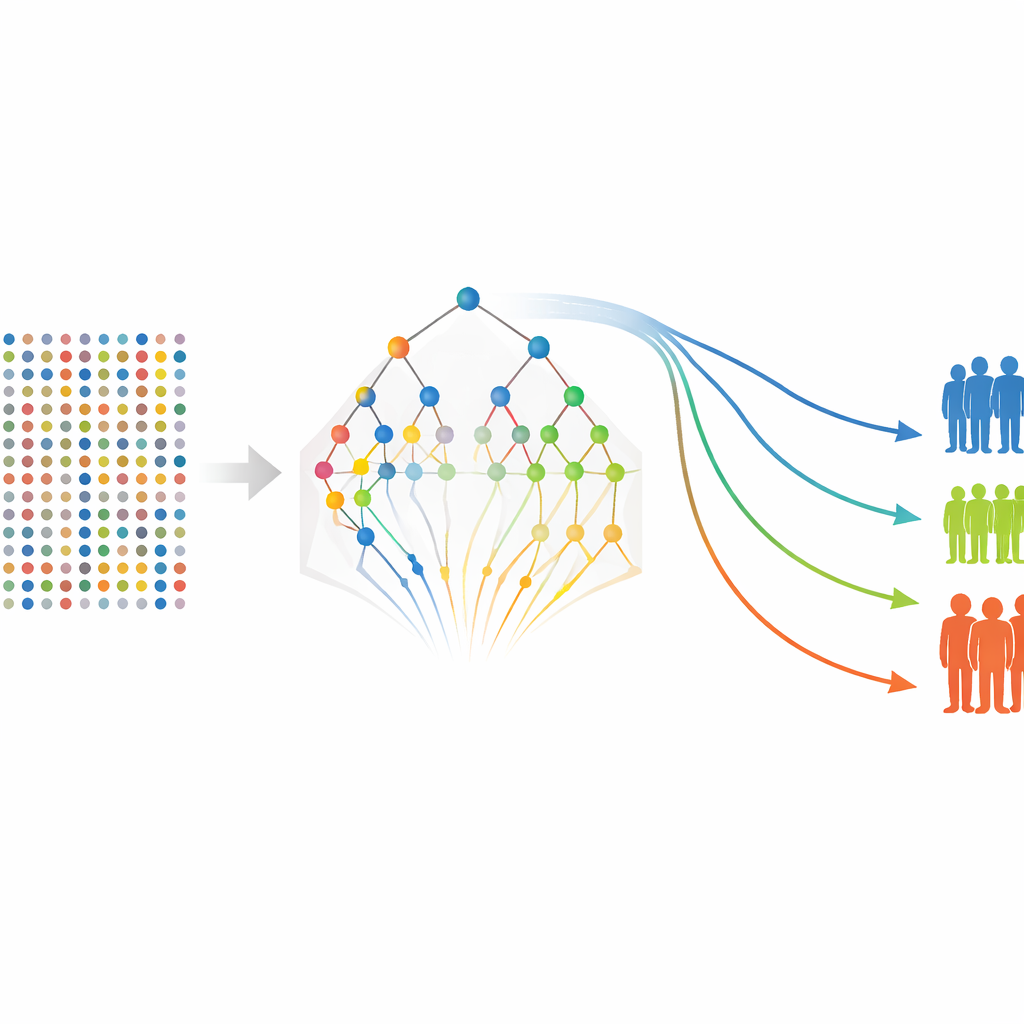
Med en förfinad lista proteiner i handen återgår författarna till mer traditionella överlevnadsmodeller för att uppskatta hur varje markör—och vissa kliniska variabler som tumörstadium—relaterar till chansen att förbli fri från återfall eller fjärrspridning. De bygger modeller separat för återfallsfri överlevnad och metastasfri överlevnad, och beräknar sedan en riskscore för varje patient baserat på deras proteinnivåer och kliniska egenskaper. Patienterna grupperas i låg-, medel- och högriskkategorier, och standardiserade överlevnadskurvor visar tydlig separation mellan dessa grupper, även om studien endast omfattar 80 patienter. Flera proteiner, inklusive FGF-5, Neuropilin-2 och Siglec-5-relaterade mått, framträder upprepade gånger som starka indikatorer på sämre utfall, medan vissa markörer tycks vara skyddande.
Testa flödet under tuffa förhållanden
För att kontrollera att deras angreppssätt inte bara överanpassar denna lilla dataset kör forskarna omfattande datorsimuleringar som efterliknar högdimensionella proteinstudier med starka brott mot vanliga modellantaganden och olika mönster av saknade data. I dessa stresstester identifierar samma analysflöde fortfarande en kompakt uppsättning verkligt viktiga markörer och separerar låg- och högriskgrupper, även när de vanliga antagandena bakom klassiska överlevnadsmodeller inte gäller. De varierar också trösklarna för saknade data och visar att nyckelmarkörerna och de övergripande slutsatserna förblir i stort sett stabila.
Vad detta innebär framöver
I stället för att uppfinna ett helt nytt statistiskt knep sammanställer och validerar detta arbete ett praktiskt recept för att omvandla komplexa proteinmätningar till kliniskt meningsfulla riskprediktioner. Genom att noggrant hantera saknade värden, begränsa fokus till en stabil uppsättning biomarkörer och kontrollera prestanda med robust intern validering och simuleringar erbjuder pipeline:en ett transparent sätt att identifiera lovande markörer och bygga riskscorer i små, dataintensiva cancerstudier. Författarna betonar att större, oberoende kohorter fortfarande behövs för att bekräfta specifika proteiner som rutinmässiga kliniska tester, men deras ramverk ger en solid, återanvändbar ritning för framtida biomarkördriven överlevnadsforskning.
Citering: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Nyckelord: cancerbiomarkörer, överlevnadsprediktion, proteomik, saknade data, precisionsmedicin