Clear Sky Science · nl
Verbeteren van voorspelling van overlevingsrisico via imputatie en selectie van kenmerken in hoog-dimensionele eiwit-biomarkergegevens
Waarom dit belangrijk is voor patiënten
Artsen willen steeds vaker bloedtesten gebruiken om te voorspellen hoe iemands kanker zich waarschijnlijk zal gedragen—of deze terugkeert of zich verspreidt—en de behandeling daarop af te stemmen. Moderne eiwittests kunnen honderden moleculen tegelijk meten, maar de resulterende gegevens zijn rommelig, bevatten veel missende waarden en omvatten vaak veel meer metingen dan er patiënten zijn. Dit artikel laat zien hoe je zulke complexe gegevens zorgvuldig kunt opschonen en analyseren, zodat voorspellingen over overleving betrouwbaarder worden en makkelijker te interpreteren zijn voor clinici.
Rommige laboratoriumresultaten omzetten in bruikbare signalen
De auteurs richten zich op eiwitbiomarkers, moleculen in het bloed waarvan de concentraties aanwijzingen kunnen geven over hoe een tumor groeit, hoe het immuunsysteem reageert en hoe een patiënt op therapie reageert. In studies uit de praktijk worden deze markers herhaaldelijk in de tijd gemeten, maar sommige metingen ontbreken vaak door technische problemen of doordat patiënten afhaken. Incomplete dossiers simpelweg weggooien of gaten opvullen met ruwe gemiddelden kan de resultaten ernstig vertekenen, vooral wanneer honderden eiwitten worden gevolgd in een kleine patiëntengroep. De studie bouwt daarom een stapsgewijze analysepijplijn die ontworpen is om zoveel mogelijk informatie te behouden terwijl misleidende shortcuts worden vermeden.
Gaten vullen zonder in de uitkomsten te koekeloeren
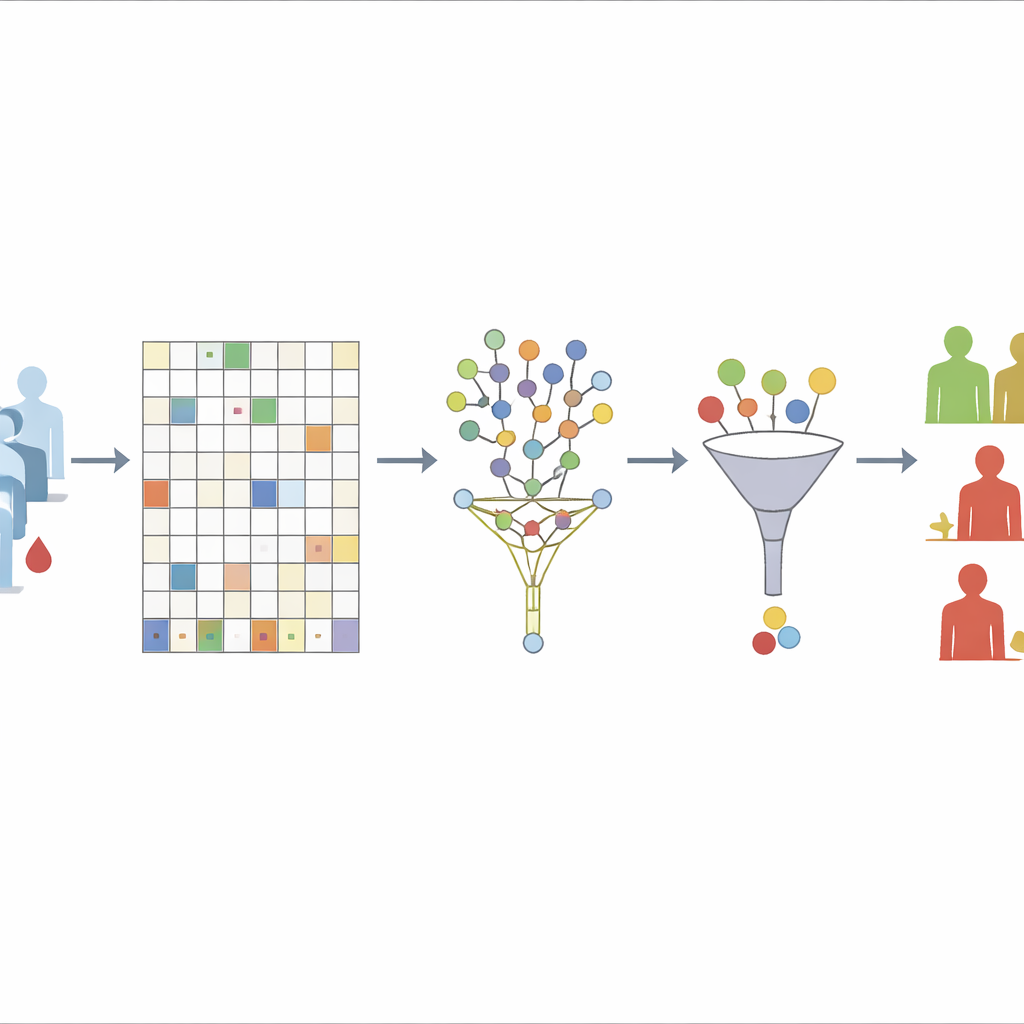
De eerste uitdaging die het team aanpakt is ontbrekende data. Ze beginnen met alleen die eiwitten weg te laten die bij meer dan 30% van de patiënten missen, een grens die ze laten zien een goede balans is tussen stabiliteit en informatieverlies. Voor de overgebleven eiwitten gebruiken ze een ‘onbegeleide’ random forest-benadering om de ontbrekende waarden te schatten. In wezen bouwt het algoritme herhaaldelijk vele beslisbomen op basis van hoe eiwitten zich onderling verhouden, niet op wie is teruggevallen of uitzaaiingen ontwikkelde. Monsters die in veel bomen op vergelijkbare wijze lijken te zijn, worden als buren behandeld; de bekende waarden in die buren worden vervolgens gebruikt om de gaten op te vullen. Door overlevingsuitkomsten bewust uit deze stap te houden, voorkomen de auteurs dat ze per ongeluk het antwoord in het opschoningsproces inbouwen.
Honderden markers terugbrengen tot een betekenisvolle paar
Als de eiwittabel eenmaal volledig is, is de volgende stap beslissen welke markers echt belangrijk zijn voor het voorspellen van de tijd tot terugval of uitzaaiing. De auteurs gebruiken eerst een techniek die zwakke voorspellers naar nul terugdringt terwijl sterkere behouden blijven, wat effectief werkt als een zeef die alleen de meest informatieve eiwitten doorlaat. Omdat deze methode groepen van gecorreleerde markers of subtiele niet-lineaire patronen kan missen, bekijken ze de overgebleven kandidaten daarna opnieuw met een tweede hulpmiddel gebaseerd op veel gerandomiseerde beslisbomen voor overlevingsdata. Deze tweede fase past niet dezelfde regressie opnieuw toe, maar scoort hoe vaak elke marker de bomen helpt patiënten met verschillende uitkomsten te splitsen. Markers die consequent hoog in de bomen verschijnen, worden als stabieler en belangrijker beschouwd.
Van geselecteerde markers naar risicogroepen op patiëntniveau
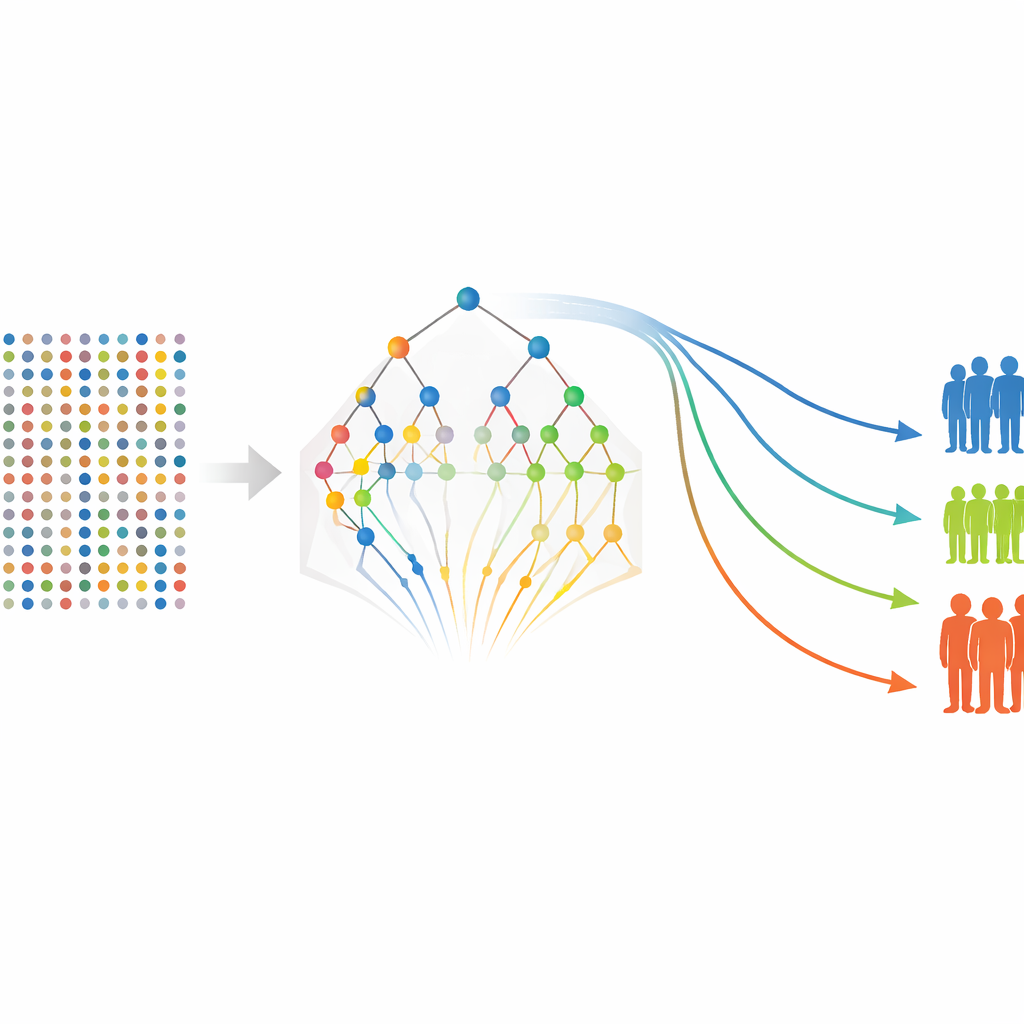
Met een verfijnde lijst eiwitten keren de auteurs terug naar meer traditionele overlevingsmodellen om te schatten hoe elke marker—en enkele klinische kenmerken zoals tumoraal stadium—relateren aan de kans om vrij te blijven van terugval of distant verspreiding. Ze bouwen afzonderlijke modellen voor vrij-van-terugvaloverleving en vrij-van-uitzaaiingoverleving, en berekenen vervolgens een risico-score voor elke patiënt op basis van hun eiwitniveaus en klinische kenmerken. Patiënten worden ingedeeld in laag-, midden- en hoogrisicocategorieën, en standaard overlevingscurven tonen duidelijke scheiding tussen deze groepen, zelfs al bevat de studie slechts 80 patiënten. Verschillende eiwitten, waaronder FGF-5, Neuropilin-2 en metingen gerelateerd aan Siglec-5, komen herhaaldelijk naar voren als sterke indicatoren van slechtere uitkomsten, terwijl sommige markers juist beschermend lijken.
De pijplijn testen onder zware omstandigheden
Om te controleren dat hun aanpak niet alleen overfit op deze kleine dataset, voeren de onderzoekers uitgebreide computersimulaties uit die hoog-dimensionele eiwitstudies nabootsen met sterke schendingen van gebruikelijke modelaannames en verschillende patronen van missende data. In deze stresstests identificeert dezelfde pijplijn nog steeds een compacte set van echt belangrijke markers en scheidt ze laag- en hoogrisicogroepen, zelfs wanneer de gebruikelijke aannames achter klassieke overlevingsmodellen niet gelden. Ze variëren ook de drempels voor ontbrekende data en tonen aan dat de belangrijkste markers en de algemene conclusies grotendeels stabiel blijven.
Wat dit betekent voor de toekomst
In plaats van een gloednieuwe statistische truc uit te vinden, stelt dit werk een praktisch recept samen en valideert het: een werkwijze om complexe eiwitmetingen om te zetten in klinisch zinvolle risicovoorspellingen. Door zorgvuldig om te gaan met ontbrekende waarden, de focus te vernauwen tot een stabiele set biomarkers en de prestaties te controleren met robuuste interne validatie en simulaties, biedt de pijplijn een transparante manier om veelbelovende markers te identificeren en risico-scores te bouwen in kleine, data-rijke kankeronderzoeken. De auteurs benadrukken dat grotere, onafhankelijke cohorten nog steeds nodig zijn om specifieke eiwitten als routinematige klinische tests te bevestigen, maar hun raamwerk biedt een solide, herbruikbaar blauwdruk voor toekomstig biomarker-gestuurd overlevingsonderzoek.
Bronvermelding: Kumar, N., Bhattacharjee, A., Vishwakarma, G.K. et al. Enhancing survival risk prediction through imputation and feature selection in high-dimensional protein biomarker data. Sci Rep 16, 14490 (2026). https://doi.org/10.1038/s41598-026-43072-z
Trefwoorden: kankerbiomarkers, overlevingsvoorspelling, proteomica, ontbrekende gegevens, precisiegeneeskunde