Clear Sky Science · tr
XKR8 tarafından lipid asimetrisinin bozulması nötrofil ekstrasellüler ağ oluşumunu yönlendirir ve mantar enfeksiyonunu engeller
Birinci hattımızın savunucuları gizli bir tuzak kurduğunda
Zararlı mikroorganizmalar saldırıya geçtiğinde, vücudun en hızlı yanıt veren hücrelerinden biri nötrofildir; bu beyaz kan hücresi mikropları yakalamak için DNA’dan yapışkan ağlar fırlatabilir. Nötrofil ekstrasellüler tuzaklar (NET'ler) olarak adlandırılan bu yapılar, enfeksiyonla mücadelede güçlü müttefiklerdir fakat yanlış zamanda açığa çıktıklarında kendi dokularımızı da zarar verebilirler. Bu çalışma, nötrofilin dış zarında DNA ağlarının ne zaman atılacağına karar veren şaşırtıcı bir “ana anahtar”ı ortaya koyuyor ve bu anahtarın akciğerleri tehlikeli mantar istilacılardan nasıl koruduğunu gösteriyor.
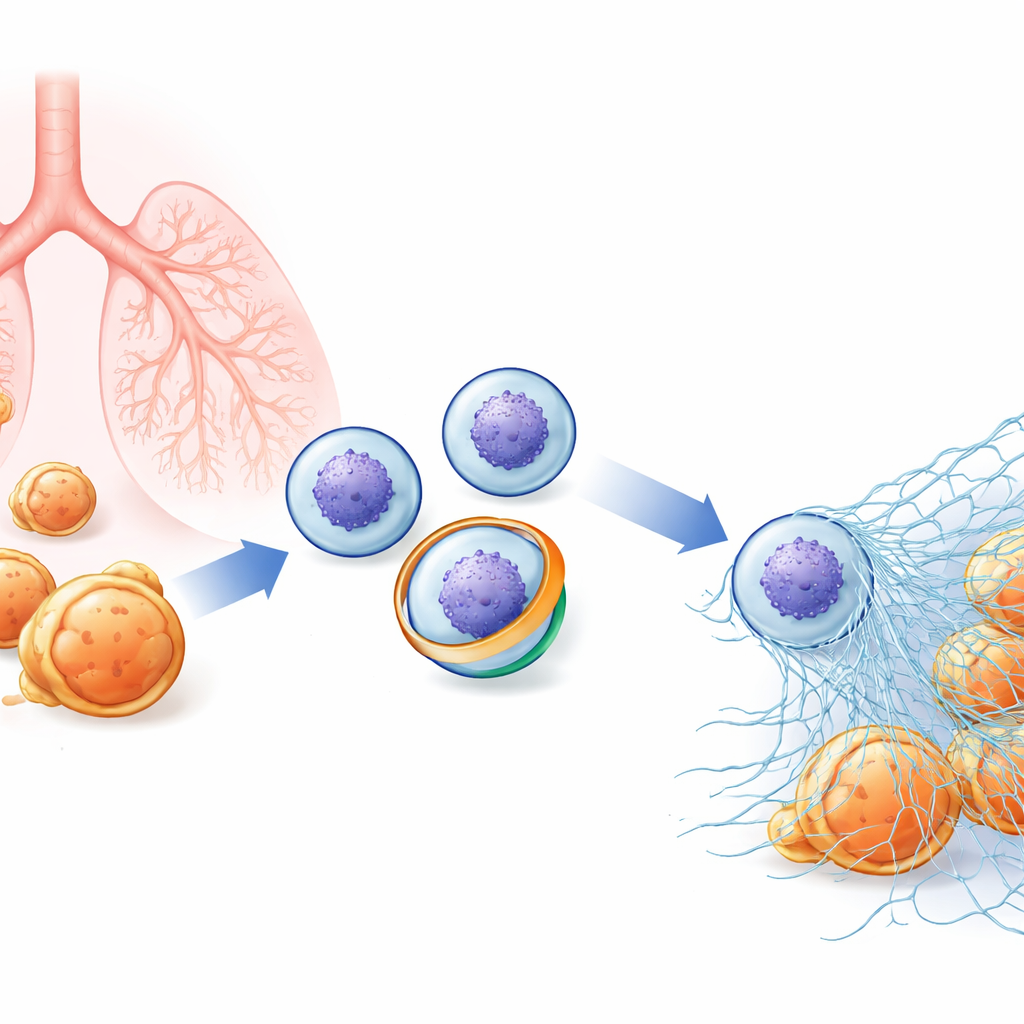
Bağışıklık hücrelerinin içindeki gizli ağ
Nötrofiller, bakteri ve mantarlara saldırmak için kanı devriye gezer. Mikropları yutmanın yanı sıra, dışarı doğru patlayarak decondense olmuş kromatini (kromozomları oluşturan maddeyi) antimikrobiyal enzimlerle kaplanmış şekilde serbest bırakabilirler. Bu yapışkan lifler, patojenleri birbirine dolayarak yerel olarak öldürülmelerini sağlayan NET’leri oluşturur. NET’ler çok etkili olduklarından, salınımları sıkı kontrol altında olmalıdır: çok az olursa enfeksiyonlar kontrolden çıkabilir; çok fazla olursa aynı ağlar otoimmün hastalıkları, akciğer hasarını ve kan pıhtılarını körükleyebilir. Araştırmacılar, nötrofilin dış zarındaki ince değişikliklerin bir hücrenin bu dramatik “NETosis”i geçirip geçirmeyeceğine karar verilmesinde erken bir adım olabileceğinden şüpheleniyordu, ancak bu süreçteki anahtar moleküler oyuncular bilinmiyordu.
XKR8 adlı bir zar anahtarı
Araştırma ekibi, özellikle nötrofillerde yüksek düzeyde bulunan XKR8 adlı bir proteine odaklandı. XKR8 bir “skramblesi”dir — hücre zarının iç ve dış katmanları arasında lipidleri çevirebilen, iki taraf arasındaki olağan asimetrinin silinmesine neden olan bir protein. Programlı hücre ölümü gibi diğer bağlamlarda, XKR8’in hücre yüzeyinde ölmekte olan hücreleri işaretleyen bir lipid sinyalini açığa çıkardığı biliniyordu. Bu çalışmada yazarlar, NET oluşumu sırasında bu lipid sinyalinin zar geçirgen hale gelmeden ve DNA salınmadan önce ortaya çıktığını, NET oluşturması öngörülen nötrofilleri işaretlediğini gösterdiler. Fare ve insan nötrofillerinden XKR8’i kaldırdıklarında, hücreler bu erken skramblling adımını artık gerçekleştiremiyor ve birçok kimyasal ve mikrobiyal tetikleyiciye yanıt olarak neredeyse hiç NET üretemiyordu.
Zar yeniden düzenlenmesinden kalsiyum dalgasına
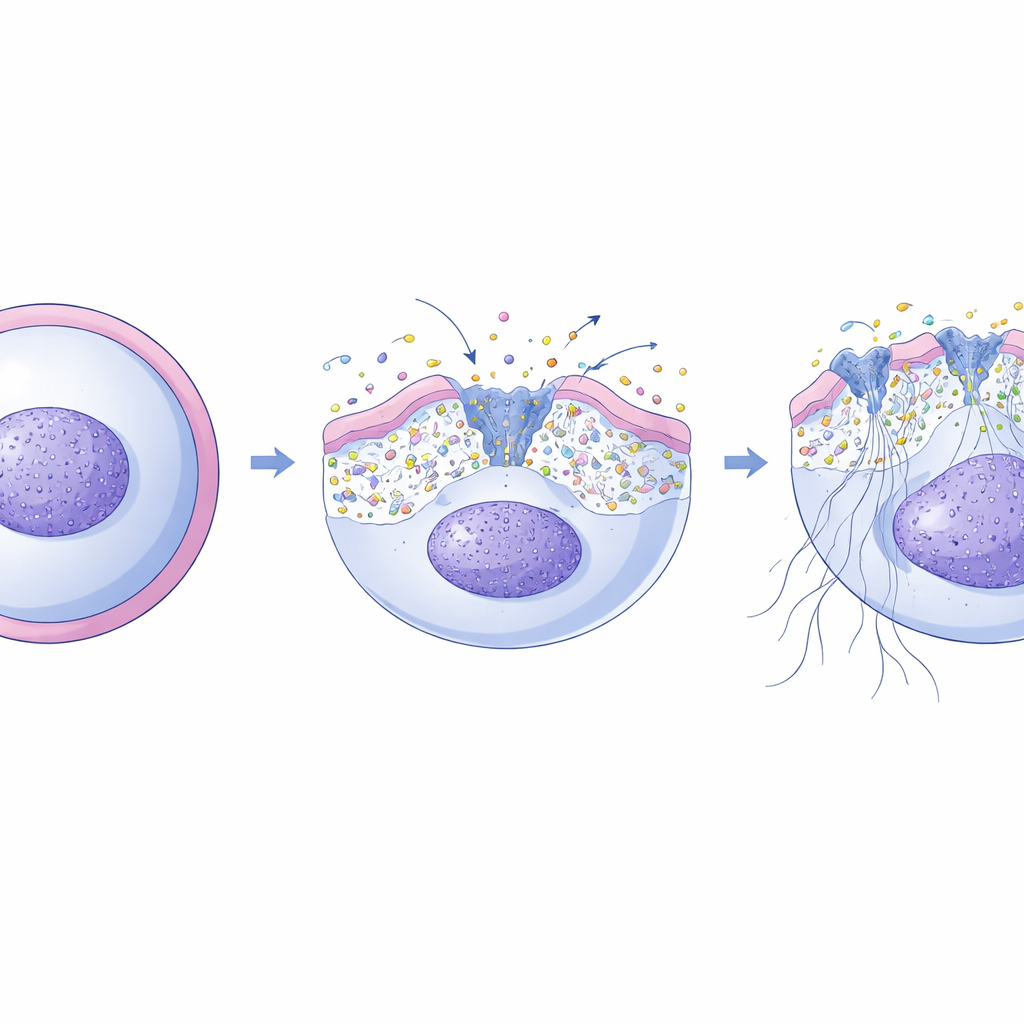
NET oluşumunun nötrofiller içinde kalsiyum artışına bağlı olduğu, bunun kromatini gevşeten ve DNA’nın dışarı akmasına izin veren enzimleri aktive ettiği bilinmektedir. Araştırmacılar XKR8’in bu sürecin merkezinde yer aldığını keşfettiler. Nötrofildeki oksidatif patlamanın ardından, kaspaz-3 adlı bir uygulatıcı enzim XKR8’i kesip aktive ediyor. Bir kez açıldığında XKR8, sadece tek bir “beni ye” sinyali değil, birkaç lipid türünü hızla zar boyunca yeniden dağıtıyor. Floresan problarla ekibin gösterdiği üzere bu yeniden dağılım zarın fiziksel gerilimini değiştiriyor. Bu mekanik gerilim de zar içine gömülü mekanosensitif kalsiyum kanallarını açıyor ve NET oluşumu sırasında tam bu pencerede kalsiyum iyonlarının hücre içine akmasını sağlıyor. Araştırmacılar bu kanalları bloke ettiklerinde NET’ler büyük ölçüde ortadan kalktı; kanalları özel aktivatörlerle uyardıklarında ise XKR8 eksik hücrelerde bile NET oluşumunu geri getirebildiler.
Tuzaklar başarısız olduğunda: akciğer hasarı ve mantar enfeksiyonu
Bu zar anahtarının canlı hayvanlarda ne anlama geldiğini anlamak için ekip, ya tamamen XKR8’den yoksun ya da kaspaz-3 tarafından kesilemeyen mutant bir versiyon taşıyan fareleri inceledi. Bakteriyel bileşenlerin tetiklediği akut akciğer hasarı modellerinde, normal fareler akciğerlerinde bolca NET, akciğer sıvısında yüksek serbest DNA düzeyleri ve belirgin doku hasarı geliştirdiler. XKR8 aktivitesi bozulmuş fareler aynı sayıda nötrofil topladı ancak çok daha az NET üretti ve daha az akciğer hasarı yaşadı; bu da XKR8 anahtarının bu bağlamda zararlı NET salınımının önemli bir sürücüsü olduğunu düşündürüyor. Buna karşılık, akciğerler Candida albicans mantarıyla enfekte edildiğinde, çalışır durumda XKR8 anahtarı olmayan fareler ciddi bir dezavantajdaydı: çok daha az NET oluşturdular, akciğerlerinde ve diğer organlarda daha yüksek mantar yükleri taşıdılar, hava boşluklarına daha fazla kanama oldu ve aşırı enfeksiyondan daha sık öldüler. Dikkate değer şekilde, mekanosensitif kalsiyum kanallarından birini aktive eden bir ilaç, nötrofilleri XKR8’den yoksun farelerde mantar kontrolünü kısmen kurtardı.
İki yüzü olan tek bir merkezi kaldıraç
Bu çalışma, birçok farklı tehlike sinyalinin nötrofillerde tek bir zar tabanlı karar noktasında birleştiği birleştirici bir mekanizmayı ortaya koyuyor. Oksidatif patlamalar kaspaz-3 aktivasyonuna yol açıyor, bu da XKR8’i açarak zar lipidlerini karıştırıyor, zar gerilimini değiştiriyor ve kalsiyum kanallarını açıyor; sonuç olarak NET’lerin başlatılması gerçekleşiyor. Herkese yönelik bir özetle, bağışıklık sistemimizin nötrofillerin yüzeyindeki hassas ayarlanmış bir “lipid kaldıraç” kullanarak DNA ağlarını ne zaman atacağına karar verdiği mesajı çıkarılabilir. Bu kaldıraç bir yönde savrulduğunda büyük mantar istilacılar temizlenirken; çok sık ya da yanlış zamanda savrulduğunda steril inflamasyonları, örneğin akciğer hasarı ya da artriti kötüleştirebilir. Bu yolak koruma ve zarar arasında bir kavşağa yerleştiği için kaspaz-3–XKR8–kalsiyum eksenini hedef almak, klinik ihtiyaca bağlı olarak zararlı NET’leri dizginlemek veya yararlı NET’leri güçlendirmek için yeni stratejiler sağlayabilir.
Atıf: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Anahtar kelimeler: nötrofil ekstrasellüler tuzaklar, XKR8 skramblesi, doğal bağışıklık, mantar akciğer enfeksiyonu, akut akciğer hasarı