Clear Sky Science · pl
Zakłócenie asymetrii lipidów przez XKR8 kieruje tworzeniem neutrofilowych sieci zewnątrzkomórkowych i hamuje zakażenie grzybicze
Jak nasi pierwsi obrońcy zastawiają ukryte sidła
Gdy zarazki atakują, jednym z najszybszych żołnierzy organizmu jest neutrofil — krwinka biała, która potrafi wyrzucać lepkie sieci z DNA, by schwytać mikroby. Struktury te, zwane neutrofilowymi sieciami zewnątrzkomórkowymi, czyli NET-ami, są potężnymi sojusznikami w walce z infekcjami, ale mogą też uszkadzać własne tkanki, gdy aktywowane są nie w porę. W badaniu odkryto zaskakujący „główny wyłącznik” w błonie zewnętrznej neutrofilu, który pomaga zdecydować, kiedy te sieci DNA zostaną wyrzucone, i pokazano, jak ten przełącznik chroni płuca przed groźnymi grzybicznymi najeźdźcami.
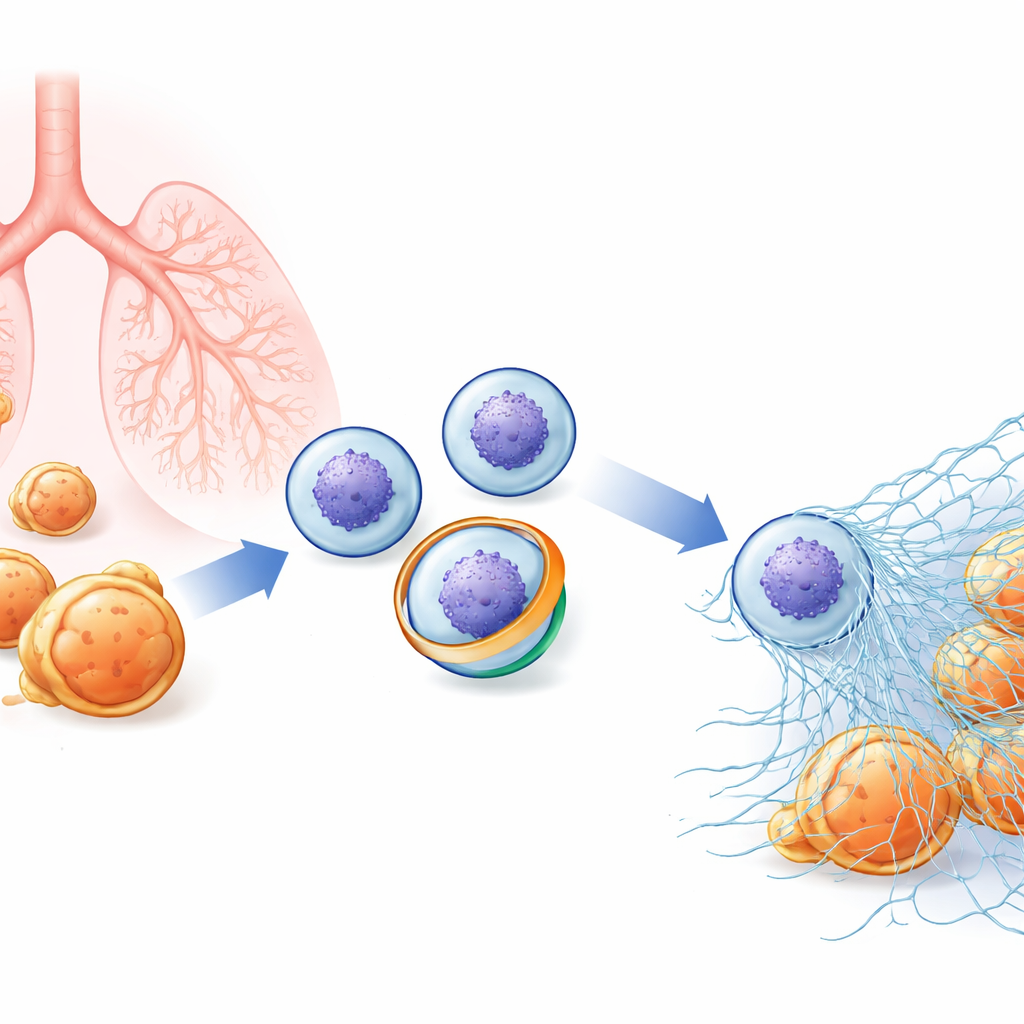
Ukryta sieć wewnątrz komórek odpornościowych
Neutrofile patrolują krew, gotowe atakować bakterie i grzyby. Oprócz fagocytozy mogą wybuchać na zewnątrz, uwalniając zdezkondensowany chromatynę (materiał tworzący chromosomy) pokrytą enzymami przeciwmikrobiologicznymi. Te lepkie włókna tworzą NET-y, które plączą patogeny, umożliwiając ich lokalne zabijanie. Ponieważ NET-y są tak silne, ich uwalnianie musi być ściśle kontrolowane: zbyt mało — infekcje wymykają się spod kontroli; zbyt dużo — te same sieci mogą napędzać choroby autoimmunologiczne, uszkodzenie płuc i zakrzepy. Naukowcy podejrzewali, że subtelne zmiany w błonie zewnętrznej neutrofila mogą być wczesnym krokiem w decyzji, czy komórka przejdzie przez dramatyczne „NETozę”, lecz kluczowi gracze molekularni pozostawali nieznani.
Przełącznik błonowy o nazwie XKR8
Zespół skupił się na białku o nazwie XKR8, występującym w szczególnie dużych ilościach w neutrofilach. XKR8 jest „scramblazą” — białkiem, które może przestawiać lipidy między wewnętrzną i zewnętrzną warstwą błony komórkowej, niwelując zwykłą asymetrię między tymi stronami. W innych kontekstach, na przykład podczas zaprogramowanej śmierci komórki, wiadomo, że XKR8 ujawnia sygnał lipidowy na powierzchni komórki, oznaczając komórki do usunięcia. W tym badaniu autorzy wykazali, że podczas formowania NET-ów ekspozycja tego sygnału lipidowego pojawia się zanim błona stanie się przepuszczalna i zanim uwolnione zostanie DNA, oznaczając neutrofile skazane na wytworzenie NET-ów. Kiedy usunęli XKR8 z mysich i ludzkich neutrofili, komórki nie mogły przeprowadzić tego wczesnego etapu przestawiania lipidów i niemal całkowicie zawodziły w tworzeniu NET-ów w odpowiedzi na wiele chemicznych i mikrobiologicznych bodźców.
Od przestawienia błony do fali wapnia
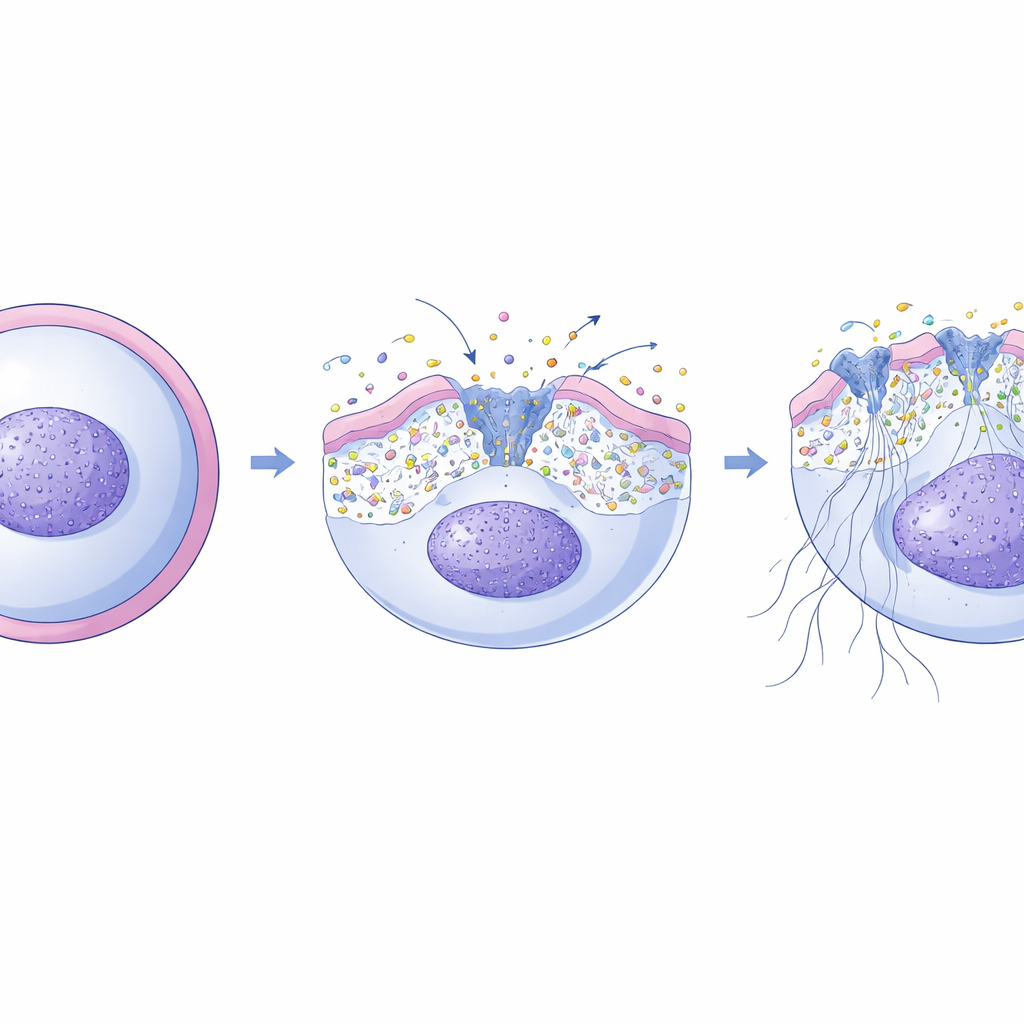
Wiadomo, że tworzenie NET-ów zależy od wzrostu stężenia wapnia wewnątrz neutrofili, co aktywuje enzymy rozluźniające chromatynę i pozwalające DNA wydostać się na zewnątrz. Badacze odkryli, że XKR8 leży w sercu tego procesu. Po oksydacyjnym wybuchu wewnątrz neutrofila, egzekucyjny enzym kaspaza-3 przecina i aktywuje XKR8. Gdy XKR8 jest włączony, szybko przemieszcza kilka typów lipidów przez błonę, nie tylko pojedynczy sygnał „zjedz mnie”. Za pomocą sond fluorescencyjnych zespół wykazał, że to przetasowanie zmienia fizyczne napięcie błony. Z kolei ten mechaniczny stres otwiera zestaw mechanosensytywnych kanałów wapniowych osadzonych w błonie, pozwalając jonům wapnia napłynąć do komórki dokładnie w oknie, gdy formowanie NET-ów jest w toku. Jeśli badacze zablokowali te kanały, NET-y były w dużej mierze zniesione; jeśli stymulowali kanały specjalnymi aktywatorami, mogli przywrócić tworzenie NET-ów nawet w komórkach pozbawionych XKR8.
Gdy sidła zawodzą: uszkodzenie płuc i zakażenie grzybicze
Aby zrozumieć, co ten błonowy przełącznik oznacza u żywych zwierząt, zespół badał myszy zmodyfikowane genetycznie tak, by albo nie miały XKR8 wcale, albo miały zmienioną wersję, której kaspaza-3 nie może przeciąć. W modelach ostrego uszkodzenia płuc wywołanego składnikami bakteryjnymi, normalne myszy rozwijały obfite NET-y w płucach, wysokie poziomy wolnego DNA w płynie płucnym i wyraźne uszkodzenie tkanek. Myszy z upośledzoną aktywnością XKR8 rekrutowały taką samą liczbę neutrofili, ale produkowały znacznie mniej NET-ów i doznały mniejszego uszkodzenia płuc, co sugeruje, że przełącznik XKR8 jest głównym napędem szkodliwego uwalniania NET-ów w tym ustawieniu. Przeciwnie, gdy płuca były zakażone grzybem Candida albicans, myszy bez sprawnego przełącznika XKR8 znalazły się w poważnej niekorzyści: wytwarzały znacznie mniej NET-ów, miały większe obciążenie grzybicze w płucach i innych narządach, krwawiły bardziej do przestrzeni powietrznych i częściej umierały z powodu przytłaczającej infekcji. Co godne uwagi, lek aktywujący jeden z mechanosensytywnych kanałów wapniowych częściowo przywrócił kontrolę nad grzybem u myszy, których neutrofile nie miały XKR8.
Jeden centralny dźwigni z dwoma twarzami
Ta praca ujawnia jedną spójną zasadę, dzięki której wiele różnych sygnałów zagrożenia koncentruje się na jednym błonowym punkcie decyzyjnym w neutrofilach. Wybuchy oksydacyjne prowadzą do aktywacji kaspazy-3, która włącza XKR8, aby przetasować lipidy błonowe, zmienić napięcie błony i otworzyć kanały wapniowe, co ostatecznie uruchamia NET-y. Dla czytelnika nieprofesjonalnego przekaz jest taki: nasz układ odpornościowy używa wyrafinowanej „lipidowej dźwigni” na powierzchni neutrofili, by zdecydować, kiedy rozpościerać sieci z DNA. Przekręcenie tej dźwigni w jedną stronę pomaga oczyścić duże grzybowe najeźdźce; przekręcanie jej zbyt często lub w niewłaściwym momencie może pogorszyć nieskażone zapalenie, takie jak uszkodzenie płuc czy zapalenie stawów. Ponieważ ta ścieżka stoi na rozdrożu ochrony i szkody, celowanie w oś kaspaza-3–XKR8–wapń może dać nowe strategie albo do ograniczania szkodliwych NET-ów, albo do wzmacniania tych korzystnych, w zależności od potrzeb klinicznych.
Cytowanie: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Słowa kluczowe: neutrofilowe sieci zewnątrzkomórkowe, scramblaza XKR8, odporność wrodzona, grzybicze zakażenie płuc, ostra niewydolność płuc