Clear Sky Science · pt
Disrupção da assimetria lipídica por XKR8 orquestra a formação de armadilhas extracelulares de neutrófilos e inibe infecção fúngica
Como nossos defensores de primeira linha armam uma armadilha oculta
Quando germes invadem, um dos respondedores mais rápidos do corpo é o neutrófilo, um glóbulo branco capaz de lançar teias pegajosas de DNA para capturar micróbios. Essas estruturas, chamadas armadilhas extracelulares de neutrófilos, ou NETs, são aliadas poderosas no combate à infecção, mas também podem danificar nossos próprios tecidos quando liberadas no momento inadequado. Este estudo revela um surpreendente “interruptor mestre” na membrana externa do neutrófilo que ajuda a decidir quando essas teias de DNA são lançadas, e mostra como esse interruptor protege os pulmões de invasores fúngicos perigosos.
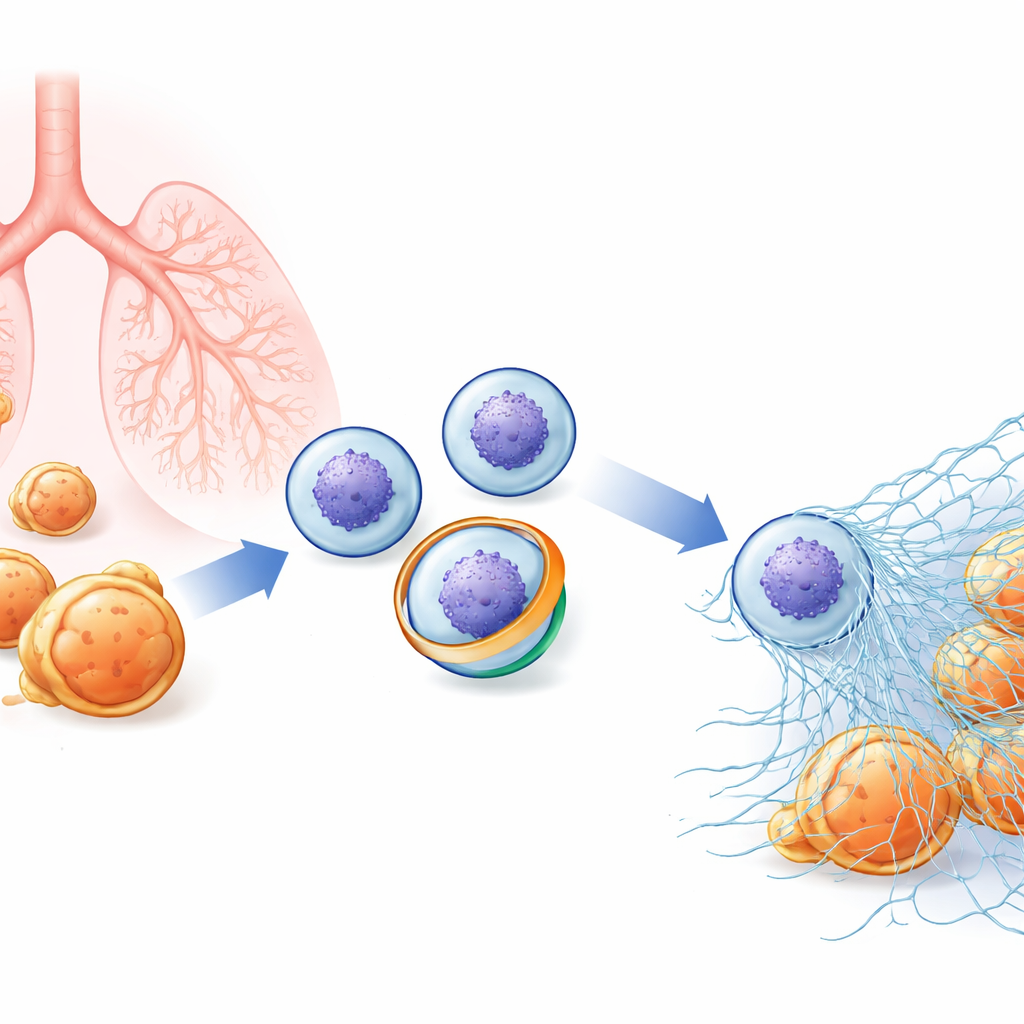
Uma teia oculta dentro das células imunes
Neutrófilos patrulham o sangue prontos para atacar bactérias e fungos. Além de engolir micróbios, eles podem explodir para fora, liberando cromatina descondensada (o material que compõe os cromossomos) revestida por enzimas antimicrobianas. Essas fibras pegajosas formam NETs que enredam patógenos para que sejam mortos localmente. Como os NETs são muito potentes, sua liberação precisa ser controlada de forma rigorosa: pouco NETs e as infecções podem sair do controle; NETs em excesso e as mesmas teias podem alimentar doenças autoimunes, lesão pulmonar e coágulos sanguíneos. Pesquisadores suspeitavam que mudanças sutis na membrana externa do neutrófilo poderiam ser um passo inicial na decisão de a célula sofrer essa dramática “NETose”, mas os principais atores moleculares eram desconhecidos.
Um interruptor de membrana chamado XKR8
A equipe concentrou-se em uma proteína chamada XKR8, encontrada em níveis especialmente altos nos neutrófilos. XKR8 é uma “escramblase” — uma proteína capaz de movimentar lipídios entre as camadas interna e externa da membrana celular, apagando a assimetria habitual entre os dois lados. Em outros contextos, como a morte celular programada, sabe-se que o XKR8 expõe um sinal lipídico na superfície celular que marca células morrendo para remoção. Aqui, os autores mostraram que, durante a formação de NETs, a exposição desse sinal lipídico aparece antes de a membrana se tornar permeável e antes da liberação de DNA, sinalizando aqueles neutrófilos destinados a formar NETs. Quando removeram XKR8 de neutrófilos de camundongos e humanos, as células não conseguiram realizar esse passo inicial de scrambling e praticamente falharam em produzir NETs em resposta a muitos estímulos químicos e microbianos.
Da reorganização da membrana ao surto de cálcio
Sabe-se que a formação de NETs depende de um aumento de cálcio dentro dos neutrófilos, o que ativa enzimas que afrouxam a cromatina e permitem que o DNA vaze. Os pesquisadores descobriram que o XKR8 está no centro desse processo. Após uma explosão oxidativa dentro do neutrófilo, uma enzima executora chamada caspase-3 cliva e ativa o XKR8. Uma vez ativado, o XKR8 redistribui rapidamente vários tipos de lipídios através da membrana, não apenas um único sinal de “me coma”. Usando sondas fluorescentes, a equipe mostrou que essa reorganização altera a tensão física da membrana. Por sua vez, esse estresse mecânico abre um conjunto de canais de cálcio mecanossensíveis embutidos na membrana, permitindo que íons cálcio entrem na célula precisamente durante a janela em que a formação de NETs está em andamento. Se os pesquisadores bloquearam esses canais, os NETs foram em grande parte abolidos; se estimularam os canais com ativadores especiais, puderam restaurar a formação de NETs mesmo em células sem XKR8.
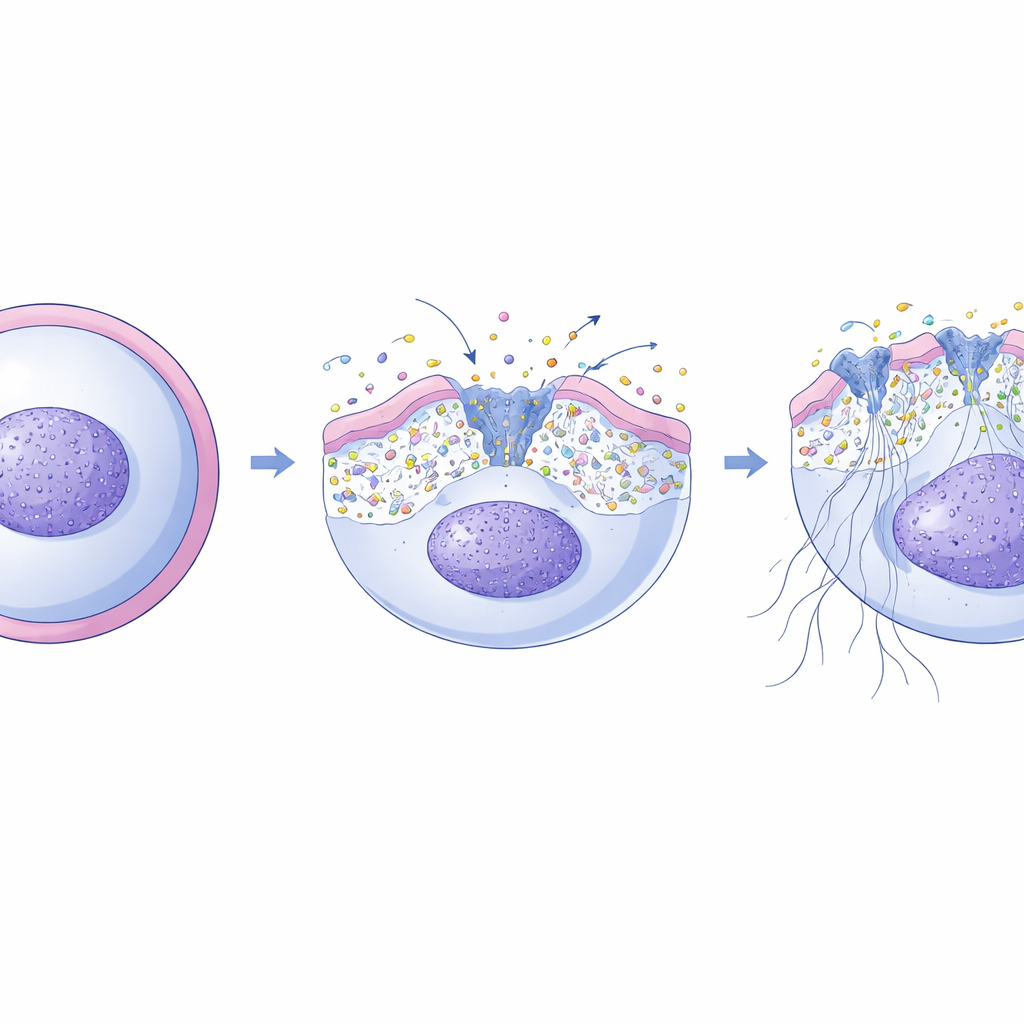
Quando as armadilhas falham: lesão pulmonar e infecção fúngica
Para entender o que esse interruptor de membrana significa em animais vivos, a equipe estudou camundongos geneticamente modificados para não expressar XKR8 ou para portar uma versão mutada que não pode ser cortada pela caspase-3. Em modelos de lesão pulmonar aguda desencadeada por componentes bacterianos, camundongos normais desenvolveram NETs abundantes nos pulmões, altos níveis de DNA livre no líquido pulmonar e dano tecidual marcado. Camundongos com atividade de XKR8 comprometida recrutaram o mesmo número de neutrófilos, mas produziram muito menos NETs e sofreram menos lesão pulmonar, sugerindo que o interruptor XKR8 é um motor importante da liberação nociva de NETs nesse contexto. Em contraste, quando os pulmões foram infectados com o fungo Candida albicans, camundongos sem um interruptor XKR8 funcional ficaram em séria desvantagem: formaram bem menos NETs, apresentaram cargas fúngicas maiores nos pulmões e em outros órgãos, sangraram mais nos espaços aéreos e morreram com mais frequência por infecção avassaladora. Notavelmente, um fármaco que ativa um dos canais de cálcio mecanossensíveis resgatou em parte o controle fúngico em camundongos cujos neutrófilos não tinham XKR8.
Uma alavanca central com duas faces
Este trabalho revela um mecanismo unificador pelo qual muitos sinais de perigo convergem em um único ponto de decisão baseado na membrana dos neutrófilos. Explosões oxidativas levam à ativação da caspase-3, que liga o XKR8 para embaralhar lipídios da membrana, alterar a tensão da membrana e abrir canais de cálcio, culminando no lançamento de NETs. Para o leitor leigo, a mensagem é que nosso sistema imunológico usa uma “alavanca lipídica” afinada na superfície dos neutrófilos para decidir quando lançar teias de DNA. Inclinar essa alavanca para um lado ajuda a eliminar grandes invasores fúngicos; incliná‑la com muita frequência ou no momento errado pode agravar inflamação estéril, como lesão pulmonar ou artrite. Como essa via fica na encruzilhada entre proteção e dano, direcionar o eixo caspase-3–XKR8–cálcio pode oferecer novas estratégias para conter NETs prejudiciais ou potencializar NETs benéficos, dependendo da necessidade clínica.
Citação: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Palavras-chave: armadilhas extracelulares de neutrófilos, escramblase XKR8, imunidade inata, infecção fúngica pulmonar, lesão pulmonar aguda