Clear Sky Science · nl
Verstoring van lipidasymmetrie door XKR8 orkestreert de vorming van neutrofiele extracellulaire vallen en remt schimmelinfecties
Hoe onze eerste verdedigingslinie een verborgen val zet
Wanneer ziekteverwekkers binnendringen, is een van de snelste responders in het lichaam de neutrofiel, een witte bloedcel die kleverige DNA-webben kan uitwerpen om microben te verstrikken. Deze structuren, neutrofiele extracellulaire vallen of NETs genoemd, zijn krachtige bondgenoten in de bestrijding van infecties, maar kunnen ook eigen weefsels beschadigen als ze op het verkeerde moment worden losgelaten. Deze studie onthult een verrassende “hoofdschakelaar” in het buitenmembraan van de neutrofiel die mee helpt beslissen wanneer deze DNA-webben worden gegooid, en laat zien hoe die schakelaar de longen beschermt tegen gevaarlijke schimmelindringers.
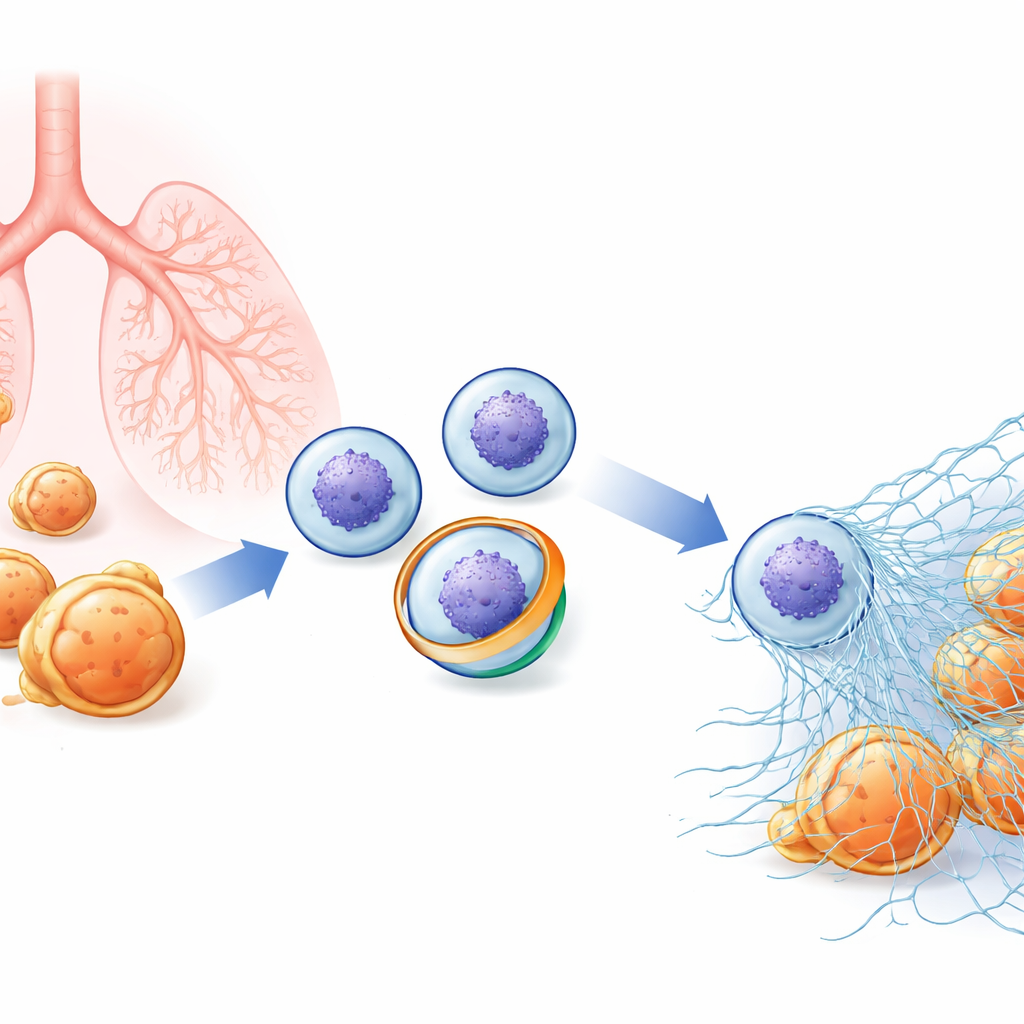
Een verborgen web binnen immuuncellen
Neutrofielen patrouilleren in het bloed en staan klaar om bacteriën en schimmels aan te vallen. Naast het insluiten van microben kunnen ze naar buiten exploderen en gedecondenseerd chromatine (het materiaal waaruit chromosomen bestaan) vrijgeven, omhuld met antimicrobiële enzymen. Deze kleverige vezels vormen NETs die pathogenen verstrikken zodat ze lokaal kunnen worden gedood. Omdat NETs zo potent zijn, moet hun vrijgave nauwkeurig worden gecontroleerd: te weinig en infecties kunnen uit de hand lopen; te veel en dezelfde webben kunnen auto-immuunziekten, longschade en bloedstolsels aanwakkeren. Onderzoekers vermoeden dat subtiele veranderingen in het buitenmembraan van de neutrofiel een vroeg stadium kunnen zijn in de beslissing of een cel deze dramatische “NETose” ondergaat, maar de sleutelspelers op moleculair niveau waren onbekend.
Een membraanschakelaar genaamd XKR8
Het team richtte zich op een eiwit genaamd XKR8, dat bijzonder veel voorkomt in neutrofielen. XKR8 is een “scramblase” — een eiwit dat lipiden kan omwisselen tussen de binnenste en buitenste laag van het celmembraan en zo de gebruikelijke asymmetrie tussen beide zijden uitwist. In andere contexten, zoals geprogrammeerde celdood, is bekend dat XKR8 een lipidesignaal op het celoppervlak blootlegt dat stervende cellen markeert voor verwijdering. Hier toonden de auteurs aan dat tijdens NET-vorming de blootlegging van dit lipidesignaal optreedt voordat het membraan lek wordt en voordat DNA vrijkomt, en zo die neutrofielen markeert die bestemd zijn om NETs te vormen. Toen ze XKR8 verwijderden uit muis- en humane neutrofielen, konden de cellen deze vroege scramblingstap niet meer uitvoeren en slaagden ze er vrijwel niet in NETs te vormen als reactie op veel chemische en microbiële triggers.
Van membraanherverdeling naar calciumsurge
Bekend is dat NET-vorming afhankelijk is van een stijging van calcium in neutrofielen, wat enzymen activeert die chromatine losser maken en DNA laten ontsnappen. De onderzoekers ontdekten dat XKR8 centraal staat in dit proces. Na een oxidatieve uitbarsting binnen de neutrofiel knipt en activeert een executoreiwit, caspase-3, XKR8. Eenmaal geactiveerd herverdeelt XKR8 snel meerdere typen lipiden over het membraan, niet slechts één enkel “eet me”-signaal. Met behulp van fluorescente probes toonde het team aan dat deze herschikking de fysieke spanning van het membraan verandert. Deze mechanische stress opent op haar beurt een set mechanogevoelige calciumkanalen in het membraan, waardoor calciumionen tijdens het venster waarin NET-vorming plaatsvindt de cel instromen. Als de onderzoekers deze kanalen blokkeerden, verdween de NET-vorming grotendeels; als ze de kanalen stimuleerden met speciale activatoren, konden ze de NET-vorming herstellen zelfs in cellen zonder XKR8.
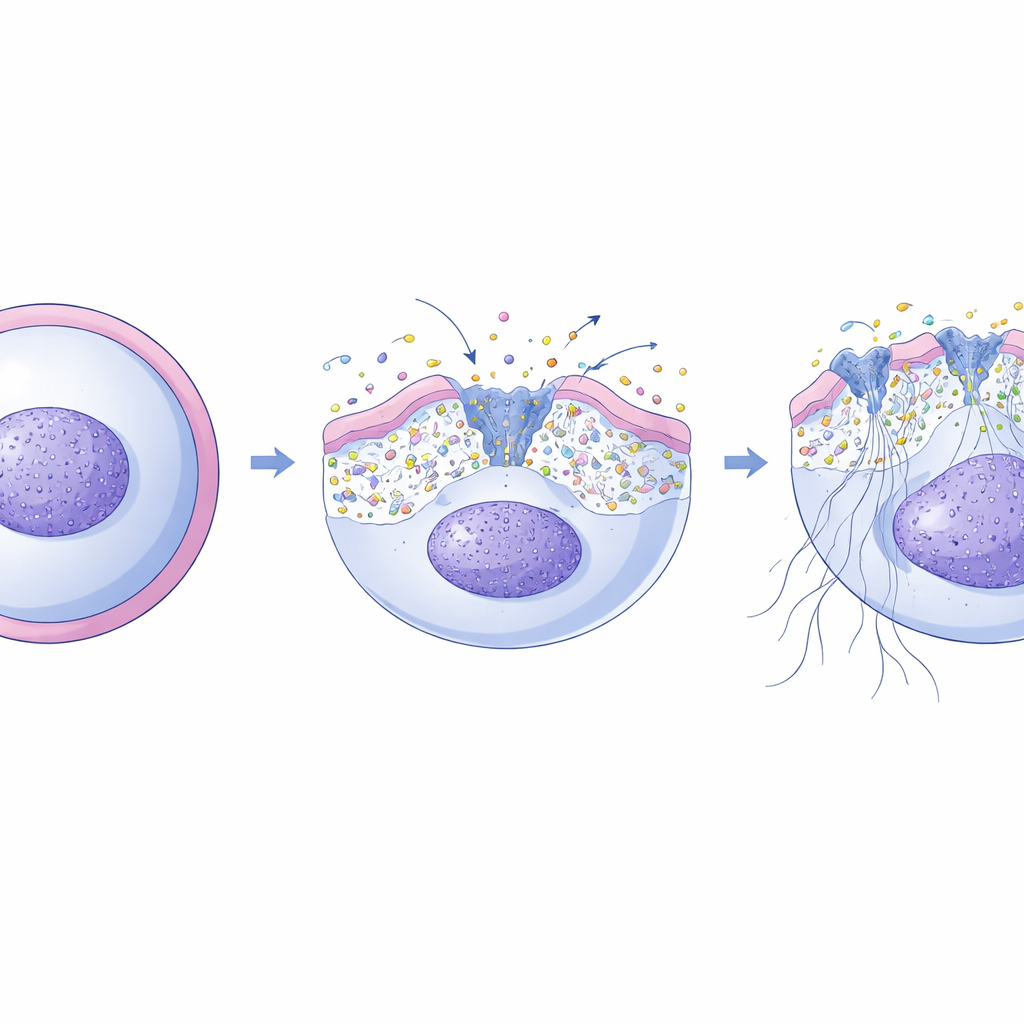
Wanneer vallen falen: longschade en schimmelinfectie
Om te begrijpen wat deze membraanschakelaar betekent in levende dieren, bestudeerde het team muizen die ofwel geen XKR8 hadden of een gemuteerde versie droegen die niet door caspase-3 kan worden geknipt. In modellen van acute longschade veroorzaakt door bacteriële componenten ontwikkelden normale muizen overvloedige NETs in hun longen, hoge niveaus van vrij DNA in longvocht en duidelijke weefselschade. Muizen met verminderde XKR8-activiteit rekruteerden hetzelfde aantal neutrofielen, maar produceerden veel minder NETs en ondervonden minder longschade, wat suggereert dat de XKR8-schakelaar een belangrijke aanjager is van schadelijke NET-vrijgave in deze context. Daarentegen waren muizen zonder een werkende XKR8-schakelaar bij longinfectie met de schimmel Candida albicans in ernstig nadeel: zij vormden veel minder NETs, hadden zwaardere schimmelbelastingen in longen en andere organen, kregen meer bloedingen in de luchtwegen en overleden vaker aan overweldigende infectie. Opmerkelijk was dat een geneesmiddel dat een van de mechanogevoelige calciumkanalen activeert de schimmelbestrijding deels herstelde bij muizen waarvan de neutrofielen XKR8 misten.
Een centraal hefboompunt met twee gezichten
Dit werk onthult een verenigend mechanisme waarbij veel verschillende gevaarssignalen samenkomen op één membraan-gebaseerd beslispunt in neutrofielen. Oxidatieve uitbarstingen leiden tot caspase-3-activatie, die XKR8 inschakelt om membraanlipiden te herschikken, de membraanspanning te veranderen en calciumkanalen te openen, culminerend in de lancering van NETs. Voor de niet-specialistische lezer is de kernboodschap dat ons immuunsysteem een fijn afgestelde “lipidehefboom” op het oppervlak van neutrofielen gebruikt om te bepalen wanneer DNA-webben moeten worden uitgeslagen. Het kantelen van die hefboom in de ene richting helpt grote schimmelindringers te verwijderen; te vaak of op het verkeerde moment kantelen kan steriele ontsteking zoals longschade of artritis verergeren. Omdat deze route op het kruispunt ligt tussen bescherming en schade, zou het richten op de caspase-3–XKR8–calciumas nieuwe strategieën kunnen bieden om schadelijke NETs te beteugelen of nuttige NETs te versterken, afhankelijk van de klinische behoefte.
Bronvermelding: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Trefwoorden: neutrofiele extracellulaire vallen, XKR8 scramblase, aangeboren immuniteit, schimmelinfectie van de long, acute longschade