Clear Sky Science · it
La perdita di asimmetria lipidica mediata da XKR8 orchestra la formazione di trappole extracellulari dei neutrofili e inibisce l’infezione fungina
Come i nostri primi difensori tendono una trappola nascosta
Quando i germi invadono, uno dei rispondenti più rapidi dell’organismo è il neutrofilo, un globulo bianco che può lanciare reti appiccicose di DNA per intrappolare i microbi. Queste strutture, chiamate trappole extracellulari dei neutrofili, o NET, sono alleate potenti nella lotta contro le infezioni ma possono anche danneggiare i tessuti quando vengono attivate al momento sbagliato. Questo studio svela un sorprendente “interruttore maestro” nella membrana esterna del neutrofilo che contribuisce a decidere quando queste reti di DNA vengono dispiegate, e mostra come tale interruttore protegga i polmoni da pericolosi invasori fungini.
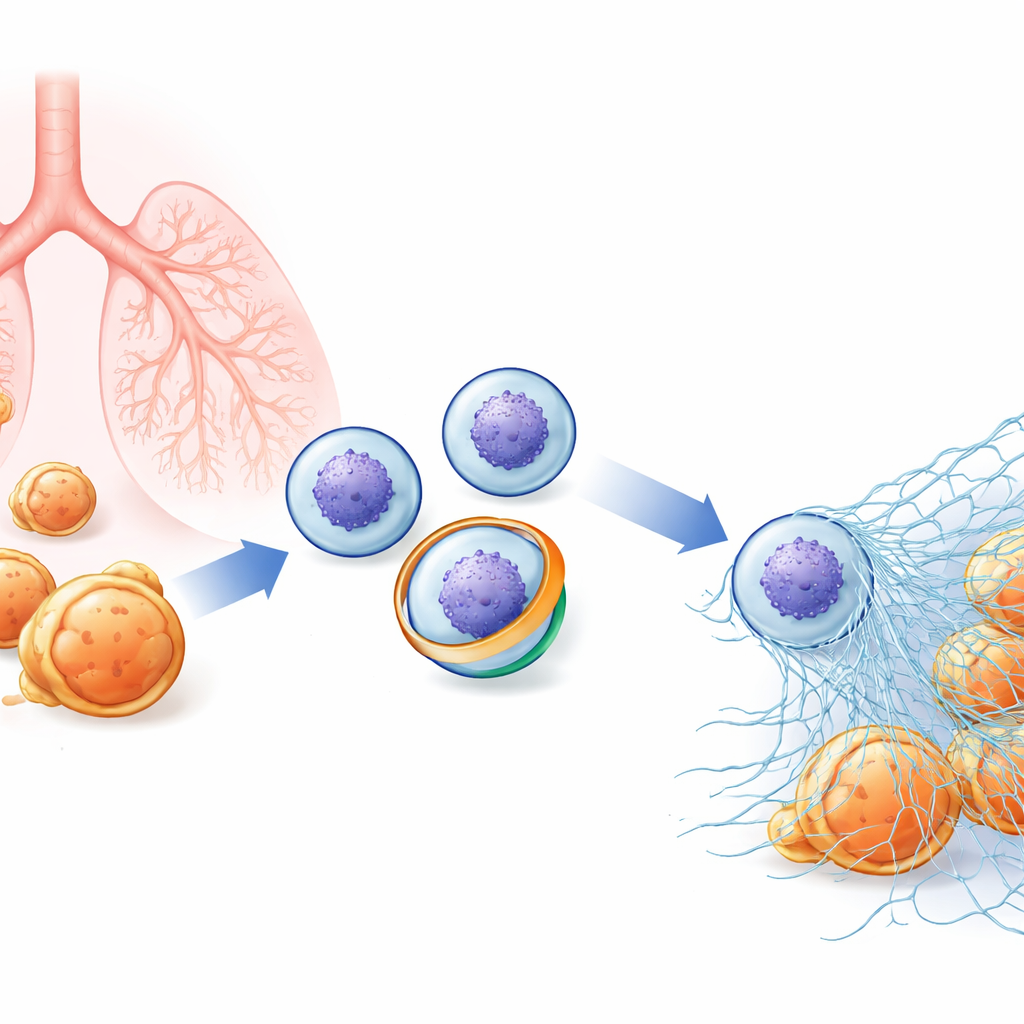
Una rete nascosta all’interno delle cellule immunitarie
I neutrofili pattugliano il sangue pronti ad attaccare batteri e funghi. Oltre a ingerire i microbi, possono esplodere all’esterno rilasciando cromatina decondensata (il materiale che compone i cromosomi) rivestita di enzimi antimicrobici. Queste fibre appiccicose formano NET che aggrovigliano i patogeni in modo che possano essere uccisi localmente. Poiché i NET sono così potenti, il loro rilascio deve essere strettamente controllato: troppo pochi e le infezioni possono sfuggire al controllo; troppo frequenti e le stesse reti possono alimentare malattie autoimmuni, lesioni polmonari e coaguli sanguigni. I ricercatori sospettavano che sottili cambiamenti nella membrana esterna del neutrofilo potessero essere un primo passo nella decisione se una cellula debba sottoporsi a questa drammatica “NETosi”, ma i principali attori molecolari erano sconosciuti.
Un interruttore di membrana chiamato XKR8
Il team si è concentrato su una proteina chiamata XKR8, presente in quantità particolarmente elevate nei neutrofili. XKR8 è una “scramblasi”: una proteina in grado di spostare i lipidi tra gli strati interno ed esterno della membrana cellulare, cancellando la consueta asimmetria tra i due lati. In altri contesti, come la morte cellulare programmata, si sa che XKR8 espone un segnale lipidico in superficie che segnala le cellule morenti per la rimozione. Qui, gli autori hanno mostrato che durante la formazione dei NET l’esposizione di questo segnale lipidico compare prima che la membrana diventi permeabile e prima del rilascio del DNA, segnando quei neutrofili destinati a formare NET. Quando hanno rimosso XKR8 da neutrofili murini e umani, le cellule non sono più state in grado di effettuare questo primo passaggio di scrambling e hanno quasi completamente fallito nel creare NET in risposta a molti stimoli chimici e microbici.
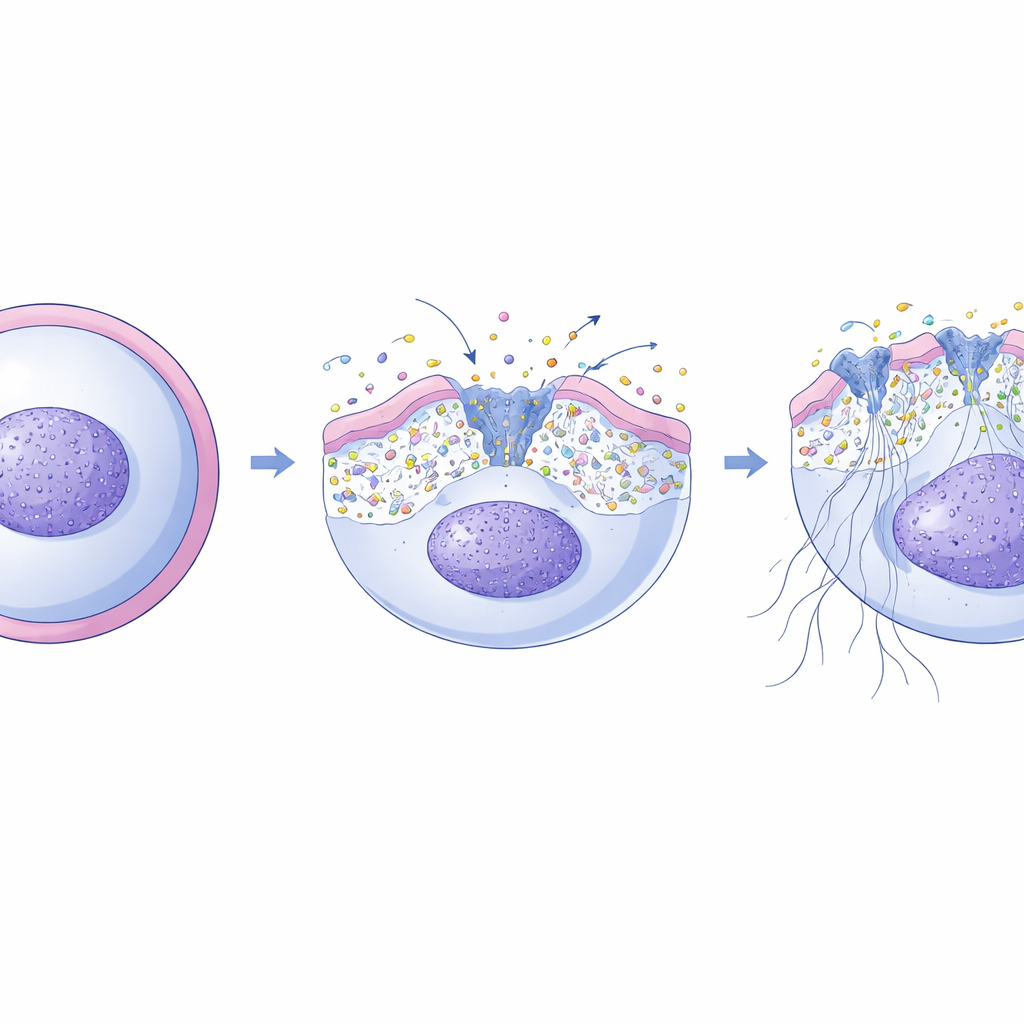
Dallo scompiglio di membrana all’ondata di calcio
Si sa che la formazione dei NET dipende da un aumento del calcio all’interno dei neutrofili, che attiva enzimi che allentano la cromatina e consentono al DNA di fuoriuscire. I ricercatori hanno scoperto che XKR8 è al centro di questo processo. Dopo un’esplosione ossidativa all’interno del neutrofilo, un enzima esecutore chiamato caspasi-3 taglia e attiva XKR8. Una volta attivato, XKR8 ridistribuisce rapidamente diversi tipi di lipidi attraverso la membrana, non solo un singolo segnale “mangiami”. Usando sonde fluorescenti, il team ha mostrato che questo rimescolamento modifica la tensione fisica della membrana. A sua volta, questo stress meccanico apre una serie di canali del calcio meccanosensibili incorporati nella membrana, permettendo agli ioni calcio di affluire nella cellula proprio nella finestra temporale in cui la formazione dei NET è in corso. Se i ricercatori bloccavano questi canali, i NET venivano per lo più aboliti; se stimolavano i canali con attivatori speciali, potevano ripristinare la formazione di NET anche in cellule prive di XKR8.
Quando le trappole falliscono: lesione polmonare e infezione fungina
Per comprendere cosa significhi questo interruttore di membrana negli organismi viventi, il team ha studiato topi progettati per essere privi di XKR8 o portare una versione mutata che non può essere tagliata dalla caspasi-3. In modelli di lesione polmonare acuta indotta da componenti batteriche, i topi normali sviluppavano abbondanti NET nei polmoni, alti livelli di DNA libero nel liquido polmonare e danni tissutali marcati. I topi con attività XKR8 compromessa reclutavano lo stesso numero di neutrofili ma producevano molti meno NET e subivano meno lesioni polmonari, suggerendo che l’interruttore XKR8 sia un importante motore del rilascio dannoso di NET in questo contesto. Al contrario, quando i polmoni erano infettati dal fungo Candida albicans, i topi privi di un interruttore XKR8 funzionante erano in grave svantaggio: formavano molti meno NET, portavano carichi fungini maggiori nei polmoni e in altri organi, sanguinavano di più negli spazi aerei e morivano più spesso per infezione travolgente. È significativo che un farmaco che attiva uno dei canali del calcio meccanosensibili abbia parzialmente ripristinato il controllo fungino in topi i cui neutrofili erano privi di XKR8.
Una leva centrale con due facce
Questo lavoro rivela un meccanismo unificante attraverso il quale molti diversi segnali di pericolo convergono su un singolo punto decisionale basato sulla membrana nei neutrofili. Le esplosioni ossidative portano all’attivazione della caspasi-3, che accende XKR8 per rimescolare i lipidi di membrana, modificare la tensione della membrana e aprire i canali del calcio, culminando nel lancio dei NET. Per il lettore non specialistico, il messaggio è che il nostro sistema immunitario usa una “leva lipidica” finemente regolata sulla superficie dei neutrofili per decidere quando tessere reti di DNA. Spostare quella leva in una direzione aiuta a eliminare grandi invasori fungini; spostarla troppo spesso o al momento sbagliato può peggiorare l’infiammazione sterile come la lesione polmonare o l’artrite. Poiché questa via si trova all’incrocio tra protezione e danno, mirare l’asse caspasi-3–XKR8–calcio potrebbe offrire nuove strategie per reprimere i NET dannosi o potenziare quelli benefici, a seconda del bisogno clinico.
Citazione: Liu, W., Ping, J., Deng, L. et al. Lipid asymmetry disruption by XKR8 orchestrates neutrophil extracellular trap formation and inhibits fungal infection. Nat Immunol 27, 949–960 (2026). https://doi.org/10.1038/s41590-026-02456-z
Parole chiave: trappole extracellulari dei neutrofili, scramblase XKR8, immunità innata, infezione fungina polmonare, lesione polmonare acuta